上海市金山中学2019-2020学年高一下学期化学期中考试试卷
试卷更新日期:2021-04-12 类型:期中考试
一、单选题
-
1. 汽车在剧烈碰撞后,安全气囊会弹出并充满一种保护气体。该气体在空气中含量最高,其分子式为( )A、O2 B、CO C、N2 D、CO22. 化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )A、镁离子的电子式: B、Cl-的结构示意图:
 C、二氧化碳的电子式:
D、质量数为37的氯原子:
3. 下列物质的水溶液因为盐的水解而呈酸性的是( )A、NH4HSO4 B、Al2(SO4)3 C、Na2S D、CH3COOH4. 下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )A、二氧化硅和生石灰的熔化 B、加热氯化铵和水 C、碘和干冰的升华 D、氯化钠和硫的汽化5. 酸雨形成的主要原因是( )A、过度砍伐 B、工业排放二氧化碳 C、含氮、磷洗衣粉的使用 D、大量燃烧煤和石油6. 下列反应中,起了氮的固定作用的是( )A、N2和H2在一定条件下合成氨 B、由氨制成碳酸氢铵或硫酸铵 C、NO和O2反应生成NO2 D、NO2与H2O反应生成HNO37. 具有漂白作用的物质有:①84 消毒液 ②二氧化硫 ③过氧化氢 ④漂白粉,其漂白原理相同的是( )A、①③ B、②③ C、①③④ D、①②④8. 下列物质在水溶液中的电离方程式错误的是( )A、NaHCO3=Na++H+ +CO32- B、NaHSO4=Na+ +H+ +SO42- C、MgCl2=Mg2++2Cl- D、Ba(OH)2=Ba2+ +2OH-9. 关于氮肥的说法正确的是( )A、硫铵与石灰混用肥效增强 B、所有铵态氮肥中,氮元素化合价都是 -3 价 C、使用碳铵应深施盖土 D、尿素属于氨态氮肥10. 反应O2(g)+2SO2(g)⇌2SO3(g) ΔH<0,若在恒容绝热容器中发生,下列选项表明该反应一定已达平衡状态的是( )A、容器内的密度不再变化 B、容器内的温度不再变化 C、容器内气体的反应速率υ正(O2)=2υ逆(SO2) D、容器内气体的浓度c(O2)∶c(SO2)∶c(SO3)=1∶2∶211. 100mL 浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是( )A、加入少量浓盐酸 B、加入几滴氯化铜溶液 C、加入适量蒸馏水 D、加入适量的氯化钠溶液12. 实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )A、
C、二氧化碳的电子式:
D、质量数为37的氯原子:
3. 下列物质的水溶液因为盐的水解而呈酸性的是( )A、NH4HSO4 B、Al2(SO4)3 C、Na2S D、CH3COOH4. 下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )A、二氧化硅和生石灰的熔化 B、加热氯化铵和水 C、碘和干冰的升华 D、氯化钠和硫的汽化5. 酸雨形成的主要原因是( )A、过度砍伐 B、工业排放二氧化碳 C、含氮、磷洗衣粉的使用 D、大量燃烧煤和石油6. 下列反应中,起了氮的固定作用的是( )A、N2和H2在一定条件下合成氨 B、由氨制成碳酸氢铵或硫酸铵 C、NO和O2反应生成NO2 D、NO2与H2O反应生成HNO37. 具有漂白作用的物质有:①84 消毒液 ②二氧化硫 ③过氧化氢 ④漂白粉,其漂白原理相同的是( )A、①③ B、②③ C、①③④ D、①②④8. 下列物质在水溶液中的电离方程式错误的是( )A、NaHCO3=Na++H+ +CO32- B、NaHSO4=Na+ +H+ +SO42- C、MgCl2=Mg2++2Cl- D、Ba(OH)2=Ba2+ +2OH-9. 关于氮肥的说法正确的是( )A、硫铵与石灰混用肥效增强 B、所有铵态氮肥中,氮元素化合价都是 -3 价 C、使用碳铵应深施盖土 D、尿素属于氨态氮肥10. 反应O2(g)+2SO2(g)⇌2SO3(g) ΔH<0,若在恒容绝热容器中发生,下列选项表明该反应一定已达平衡状态的是( )A、容器内的密度不再变化 B、容器内的温度不再变化 C、容器内气体的反应速率υ正(O2)=2υ逆(SO2) D、容器内气体的浓度c(O2)∶c(SO2)∶c(SO3)=1∶2∶211. 100mL 浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是( )A、加入少量浓盐酸 B、加入几滴氯化铜溶液 C、加入适量蒸馏水 D、加入适量的氯化钠溶液12. 实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )A、 是氨气发生装置
B、
是氨气发生装置
B、 是氨气发生装置
C、
是氨气发生装置
C、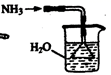 是氨气吸收装置
D、
是氨气吸收装置
D、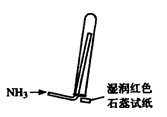 是氨气收集、检验装置
13. 下列溶液中离子检验的结论错误的是( )A、滴入AgNO3溶液有白色沉淀产生,说明原溶液中一定含有Cl- B、先加入稀盐酸,无明显现象,再滴入BaCl2溶液,有白色沉淀产生,说明原溶液中一定含有SO42- C、加入稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊,说明原溶液中可能含有CO32- D、加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明原溶液中一定含有NH4+14. 能用H++OH-=H2O来表示的化学反应是( )A、固体Cu(OH)2和H2SO4溶液反应 B、澄清石灰水和HNO3溶液反应 C、KOH溶液和醋酸溶液反应 D、Ba(OH)2溶液和H2SO4溶液反应15. 火药是中国古代四大发明之一,由硫磺、火硝和木炭粉均匀混合而成,点燃后可能发生的反应: (已配平),则反应中作氧化剂的是( )A、S和KNO3 B、S C、C D、KNO316. 在pH=1的无色透明溶液中能大量共存的离子组是( )A、Fe3+、Cu2+、 B、Na+、 、S2- C、K+、 、Cl- D、Mg2+、 、Cl-17. 醋酸的下列性质中,可以证明它是弱电解质的是( )A、1 mol/L的醋酸溶液中c(H+)=0.01mol/L B、醋酸与水以任意比互溶 C、10mL1 mol/L的醋酸溶液恰好与10mL1 mol/L的 溶液完全反应 D、醋酸溶液的导电性比盐酸弱18. 下列事实中不能用勒夏特列原理来解释的是( )A、高压有利于合成氨的反应 B、往硫化氢水溶液中加碱有利于S2-的增多 C、打开啤酒瓶盖有大量的气体冒出 D、加入催化剂有利于氨氧化的反应19. 《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )A、蒸馏 B、升华 C、分液 D、过滤20. 经检验,某酸雨的成分除含有少量H+和极少量OH﹣外,还有Na+、Cl﹣、 、 等离子,已知:c(Na+)=7×10﹣6 mol•L﹣1 , c(Cl-)=3.5×10﹣5 mol•L﹣1 , c( )=2.3×10﹣5 mol•L﹣1 , c( )=2.5×10﹣6 mol•L﹣1 , 则该酸雨的pH为( )A、3 B、4 C、5 D、6
是氨气收集、检验装置
13. 下列溶液中离子检验的结论错误的是( )A、滴入AgNO3溶液有白色沉淀产生,说明原溶液中一定含有Cl- B、先加入稀盐酸,无明显现象,再滴入BaCl2溶液,有白色沉淀产生,说明原溶液中一定含有SO42- C、加入稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊,说明原溶液中可能含有CO32- D、加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明原溶液中一定含有NH4+14. 能用H++OH-=H2O来表示的化学反应是( )A、固体Cu(OH)2和H2SO4溶液反应 B、澄清石灰水和HNO3溶液反应 C、KOH溶液和醋酸溶液反应 D、Ba(OH)2溶液和H2SO4溶液反应15. 火药是中国古代四大发明之一,由硫磺、火硝和木炭粉均匀混合而成,点燃后可能发生的反应: (已配平),则反应中作氧化剂的是( )A、S和KNO3 B、S C、C D、KNO316. 在pH=1的无色透明溶液中能大量共存的离子组是( )A、Fe3+、Cu2+、 B、Na+、 、S2- C、K+、 、Cl- D、Mg2+、 、Cl-17. 醋酸的下列性质中,可以证明它是弱电解质的是( )A、1 mol/L的醋酸溶液中c(H+)=0.01mol/L B、醋酸与水以任意比互溶 C、10mL1 mol/L的醋酸溶液恰好与10mL1 mol/L的 溶液完全反应 D、醋酸溶液的导电性比盐酸弱18. 下列事实中不能用勒夏特列原理来解释的是( )A、高压有利于合成氨的反应 B、往硫化氢水溶液中加碱有利于S2-的增多 C、打开啤酒瓶盖有大量的气体冒出 D、加入催化剂有利于氨氧化的反应19. 《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )A、蒸馏 B、升华 C、分液 D、过滤20. 经检验,某酸雨的成分除含有少量H+和极少量OH﹣外,还有Na+、Cl﹣、 、 等离子,已知:c(Na+)=7×10﹣6 mol•L﹣1 , c(Cl-)=3.5×10﹣5 mol•L﹣1 , c( )=2.3×10﹣5 mol•L﹣1 , c( )=2.5×10﹣6 mol•L﹣1 , 则该酸雨的pH为( )A、3 B、4 C、5 D、6二、综合题
-
21. 将高温水蒸气通到硫氰化钾的表面,会发生反应: 。完成下列填空:(1)、写出上述反应所涉及的金属阳离子的结构示意图;(2)、上述反应所涉及的各物质中,属于非电解质的是。(3)、写出CO₂的电子式 , 其熔沸点低的原因是。(4)、已知物质的量浓度均为0.10mol/L的Na2CO3溶液pH如下:
溶液
Na2CO3
pH
11.6
热的Na2CO3溶液是清洗油污的效果更好,请从水解平衡的角度分析其原因
(5)、K2S接触潮湿银器表面,会出现黑色斑点(Ag2S),其原理如下:请配平上述反应。
22. 任何物质的水溶液都存在水的电离平衡,其电离方程式可表示为: 。下表是不同温度下水的离子积数据:温度(℃)
25
水的离子积常数
a
完成下列填空:
(1)、25℃时,向100mL纯水中加入0.01mol的 固体,(选填“促进”或“抑制”)了水的电离平衡,所得溶液呈性(选填“酸”、“碱”或“中”),原因是(用离子反应方程式表示)。(2)、若 ,则a (选填“ ”、“ ”或“=”),理由是。(3)、 ℃时,测得纯水的 ,则 mol/L;该温度下某盐酸溶液的 ,该溶液的 mol/L。(4)、 ℃时,0.01mol/L的NaOH溶液的 。23. 工业废气中氮氧化物(NO、NO2等,以通式NOx表示)是主要的大气污染物之一。利用甲烷可消除NO2污染,CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和0.80molNO2 , 测得n(CH4)随时间变化的有关实验数据见下表:
组别
温度
时间/min
0
10
20
40
50
60
①
T1
n(CH4)/mol
0.50
0.35
0.25
0.10
0.10
0.10
②
T2
n(CH4)/mol
0.50
0.30
0.18
……
0.15
0.15
回答下列问题:
(1)、组别①中,0~10min内NO2的平均降解速率为v(NO2)= 。(2)、由实验数据可知实验控制的温度T2T1(填“>”或“<”),请简述理由。(3)、组别②中,T2温度下40min时n(CH4)=mol。该反应正反应为反应(填“吸热”或“放热”),理由是。(4)、温度T1时CO2物质的量随时间的变化如下图,在图中画出温度T2时CO2物质的量随时间的变化曲线。 (5)、汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为。
(5)、汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为。三、实验题
-
24. 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
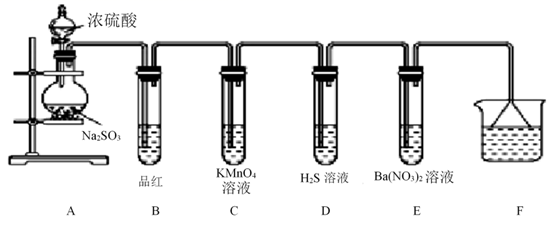
已知: 。回答下列问题:
(1)、装置A中盛放浓硫酸的仪器名称是。(2)、装置B的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象。(3)、装置C中表现了SO2的性;装置D中表现了SO2的性,装置D 中发生反应的化学方程式为。(4)、F装置的作用是 , 漏斗的作用是。(5)、E中产生白色沉淀,该白色沉淀的化学成分为(填编号)。A.BaSO3 B.BaSO4 C.BaSO3和BaSO4
设计实验证明你的判断。
(6)、工厂煤燃烧产生的烟气若直接排放到空气中,引发的主要环境问题有_________。A、温室效应 B、粉尘污染 C、水体富营养化(7)、工业上为实现燃煤脱硫,常通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,与烟气中SO2反应从而将硫固定,其产物可作建筑材料。写出其中将硫固定的化学方程式是。