吉林省延边州2021年高考理综-化学2月模拟试卷
试卷更新日期:2021-04-07 类型:高考模拟
一、单选题
-
1. 2020年11月24日,嫦娥五号探测器发射圆满成功,开启我国首次地外天体采样返回之旅。探月工程所选用的新材料与化学有密切相关。下列叙述正确的是( )A、登月中,所用北斗系统的导航卫星,其计算机的芯片材料是高纯度二氧化硅 B、用于光学望远镜的高致密碳化硅特种陶瓷材料,是一种传统无机非金属材料 C、面对高空低压的环境,所使用的碳纤维是一种有机高分子材料 D、嫦娥五号探测器在月球表面展示的国旗,其材料要求具有耐高低温、防静电等多种特性,所用的高性能芳纶纤维材料是复合材料2. 下列实验装置或操作能达到相应实验的的是( )
选项
A
B
C
D
装置或操作




预期目的
检验乙醇催化氧化产物中有乙醛
用于实验室里制备氨气
蒸干FeCl3溶液制备无水FeCl3
探究氧化性:KMnO4>Cl2>I2
A、A B、B C、C D、D3. 硫酸盐(含SO 、HSO )气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下。下列说法错误的是( ) A、该过程中有H2O参与反应 B、硫酸盐气溶胶呈酸性 C、NO2是生成硫酸盐的催化剂 D、该过程中有氧氢键断裂4. 有机物N具有抗肿瘤、镇痛等生物活性,可由M合成。下列说法错误的是( )
A、该过程中有H2O参与反应 B、硫酸盐气溶胶呈酸性 C、NO2是生成硫酸盐的催化剂 D、该过程中有氧氢键断裂4. 有机物N具有抗肿瘤、镇痛等生物活性,可由M合成。下列说法错误的是( ) A、M中所有碳原子不可能共面 B、N可以与NaOH溶液反应 C、M生成N的反应为加成反应 D、M、N的一氯代物数目相同5. 海水中锂资源非常丰富,但是海水中的锂浓度低,很难被提取出来。我国科学家设计了一种太阳能驱动下,利用选择性固体陶瓷膜电解海水提取金属锂的装置(示意图如下),该装置工作时,下列说法错误的是( )
A、M中所有碳原子不可能共面 B、N可以与NaOH溶液反应 C、M生成N的反应为加成反应 D、M、N的一氯代物数目相同5. 海水中锂资源非常丰富,但是海水中的锂浓度低,很难被提取出来。我国科学家设计了一种太阳能驱动下,利用选择性固体陶瓷膜电解海水提取金属锂的装置(示意图如下),该装置工作时,下列说法错误的是( )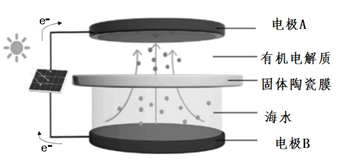 A、该装置主要涉及的能量变化:太阳能→电能→化学能 B、电极B上的电极反应式:4OH−-4e−=O2↑+2H2O C、选择性固体陶瓷膜不允许H2O通过 D、工作时,电极A为阴极6. 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其结构示意图如下(实线代表共价键,其他重复单元的W、X未标注),W、X、Z分别位于不同周期,Z的原子半径在同周期中最大。下列说法错误的是( )
A、该装置主要涉及的能量变化:太阳能→电能→化学能 B、电极B上的电极反应式:4OH−-4e−=O2↑+2H2O C、选择性固体陶瓷膜不允许H2O通过 D、工作时,电极A为阴极6. 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其结构示意图如下(实线代表共价键,其他重复单元的W、X未标注),W、X、Z分别位于不同周期,Z的原子半径在同周期中最大。下列说法错误的是( ) A、Y单质的氧化性在同周期元素形成的单质中最强 B、Z与Y可能组成多种离子化合物 C、ZW与水反应生成W2的反应中,ZW为还原剂 D、Y的最简单氢化物热稳定性大于X7. 含锌黄铜矿(CuFeS2、ZnS、FeS2及SiO2等)焙烧制海绵铜和锌矾(ZnSO4·7H2O)的工艺流程如下。下列说法正确的是( )
A、Y单质的氧化性在同周期元素形成的单质中最强 B、Z与Y可能组成多种离子化合物 C、ZW与水反应生成W2的反应中,ZW为还原剂 D、Y的最简单氢化物热稳定性大于X7. 含锌黄铜矿(CuFeS2、ZnS、FeS2及SiO2等)焙烧制海绵铜和锌矾(ZnSO4·7H2O)的工艺流程如下。下列说法正确的是( ) A、“焙烧”过程中FeS2发生的反应为4FeS2+11O2 2Fe2O3+8SO2 B、“滤渣3”的主要成分为Fe(OH)3 C、漂白粉可用CaCl2代替 D、将“滤液3”直接蒸发结晶即可得到ZnSO4·7H2O晶体
A、“焙烧”过程中FeS2发生的反应为4FeS2+11O2 2Fe2O3+8SO2 B、“滤渣3”的主要成分为Fe(OH)3 C、漂白粉可用CaCl2代替 D、将“滤液3”直接蒸发结晶即可得到ZnSO4·7H2O晶体二、填空题
-
8. CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。请回答下列问题:
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
CO2(mol)
H2(mol)
CH3OH(mol)
H2O(mol)
反应a(恒温恒容)
1
3
0
0
反应b(绝热恒容)
0
0
1
1
(1)、达到平衡时,反应a,b对比:CO2的体积分数φ(a)φ(b)(填“>”、“<”或“=”))。(2)、下列能说明反应a达到平衡状态的是_______(填字母)。A、v正(CO2)=3v逆(H2) B、混合气体的平均摩尔质量不再改变 C、c(CH3OH)=c(H2O) D、容器内压强不再改变(3)、II.我国科学家研究了不同反应温度对含碳产物组成的影响。已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2 , 分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。
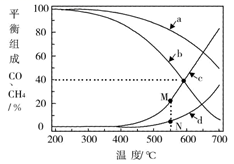
1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是和。M点平衡组成含量高于N点的原因是。
(4)、图中当CH4和和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为。(5)、III.在在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和和H2 , 发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。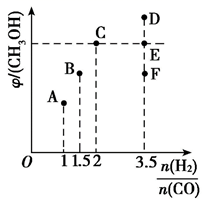
当 时,达到平衡后,CH3OH的体积分数可能是图像中的(填“D”、“E”或“F”)点。
(6)、 =时,CH3OH的体积分数最大。三、实验题
-
9. 乙醇酸钠(HOCH2COONa)又称羟基乙酸钠,它是一种有机原料,其相对分子质量98。羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。实验室拟用氯乙酸(ClCH2COOH)和NaOH溶液制备少量羟基乙酸钠,此反应为剧烈放热反应。具体实验步骤如下:
步骤1:如图所示装置的三颈烧瓶中,加入132.3g氯乙酸(ClCH2COOH)、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9至10之间。

步骤2:蒸出部分水至液面有薄膜,加少量热水,操作1。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,操作2 , 分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,操作3、过滤、干燥,得羟基乙酸钠。
请回答下列问题:
(1)、仪器A的名称为。步骤1中,发生反应的化学方程式是。(2)、如图所示的装置中仪器B为球形冷凝管,下列说法错误的是_______(填字母)。A、球形冷凝管与直形冷凝管相比,冷却面积更大,效果更好 B、球形冷凝管既可以做倾斜式蒸馏装置,也可用于垂直回流装置,应用广泛 C、在使用冷凝管进行蒸馏操作时,一般蒸馏物的沸点越高,蒸气越不易冷凝(3)、逐步加入40%NaOH溶液的目的是 , 。(4)、步骤2中,三颈烧瓶中如果忘加磁转子该如何操作:。(5)、上述步骤中,操作1、2、3的名称分别是_______(填字母)。A、过滤,过滤,冷却结晶 B、趁热过滤,过滤,蒸发结晶 C、趁热过滤,趁热过滤,冷却结晶(6)、步骤4中,得纯净羟基乙酸钠1.1mol,则实验产率为%(结果保留1位小数)。四、原理综合题
-
10. 硒(Se)元素位于元素周期表第四周期第VIA族。请回答下列问题:
I.工业上用精炼铜的阳极泥(硒主要以CuSe形式存在,还含有少量Ag、Au)为原料与浓硫酸混合焙烧,将产生的SO2、SeO2混合气体用水吸收即可得Se固体。
(1)、写出“混合气体用水吸收”时发生反应的化学方程式。(2)、下列说法正确的是_______(填字母)。A、SeO2可以氧化H2S,但遇到强氧化剂时可能表现还原性 B、热稳定性:H2Se>H2S C、“焙烧”时的主要反应为:CuSe+4H2SO4(浓) CuSO4+SeO2↑+3SO2↑+4H2O(3)、II.硒及其氢化物H2Se在新型光伏太阳能电池和金属硒化物方面有重要应用。已知:①H2Se(g)+1/2O2(g)⇌Se(s)+H2O(l) ΔH1=mKJ•mol−1
②2H2(g)+O2(g)=2H2O(g) ΔH2=nKJ•mol−1
③H2O(g)=H2O(l) ΔH3=pKJ•mol−1
反应H2(g)+Se(s)⇌H2Se(g)的反应热ΔH=kJ•mol−1(用含m、n、p的代数式表示)。
(4)、已知常温H2Se的电离平衡常数K1=1.3×10−4 , K2=5.0×10−11 , 则NaHSe溶液的离子浓度由大到小的顺序为。Ag2SO4在一定条件下可以制备Ag2SeO4已知该条件下Ag2SeO4的Ksp=5.7×10−8 , Ag2SO4的的Ksp=1.4×10−5 , 则反应Ag2SO4(s)+SeO (aq)⇌Ag2SeO4(s)+SO (aq)的化学平衡常数K=(保留两位有效数字)。(5)、用惰性电极电解弱电解质亚硒酸(H2SeO3)溶液可制得强酸H2SeO4 , 电解过程中阳极生成2mol产物时,阴极析出标准状态下的气体L。(6)、木炭包覆纳米零价铁除硒法是一种改良的含硒废水处理方法。制备纳米零价铁时,以木炭和FeCl3·6H2O为原料,在N2氛围中迅速升温至600℃,保持2小时,该过程中木炭的作用有吸附和。木炭包覆纳米零价铁在碱性含硒废水中形成许多微电池,加速SeO 的还原过程。已知SeO 转化为单质Se,写出其对应的电极反应式。11. 我国已经形成对全球稀土产业链的统治力,在稀土开采技术方面,我国遥遥领先。同时也是最早研究稀土—钴化合物结构的国家。请回答下列问题:(1)、钴原子的价层电子排布图为 , 其M层上共有个不同运动状态的电子。Fe和Co的第四电离能I4(Fe)I4(Co)(填“>”、“<”或“=”)。(2)、①为某含钴配合物的组成为CoCl3·5NH3·H2O,是该配合物中钴离子的配位数是6。1mol该配合物可以与足量的硝酸银反应生成3molAgCl沉淀,则该配合物的配体是 , 其中氮原子的杂化类型为。试判断NH3分子与钴离子形成配合物后,H—N—H键角会 (填“变大”、“变小”或“不变”),并说明理由。②某含钴配合物化学式为CoCl3·3NH3 , 该配合物在热NaOH溶液中发生反应产生絮状沉淀,并释放出气体,该反应的化学方程式为。该配合物中存在的化学键有(填字母)。
A.共价键 B.σ键 C.π键 D.配位键
(3)、一种铁氮化合物具有高磁导率,其结构如图所示: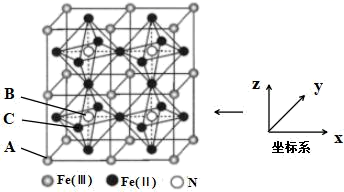
①该结构中单纯分析铁的堆积,其堆积方式为。
②已知A点的原子坐标参数为(0,0,0),B点的原子坐标参数为( ),则C点的原子坐标参数为。
12. 有机物F是一种治疗H1N1流感的常见药物,可按下列路线合成:
已知:

请回答下列问题:
(1)、C的分子式为。(2)、物质A—F中,互为同分异构体的是(填字母),A的一氯代物有种。(3)、上述反应中,属于加成反应的是(填序号)。(4)、反应①的化学反应方程式为。(5)、化合物G(如图所示)与D空间结构相似,将甲醛(HCHO)水溶液与氨水混合蒸发可制得。若原料完全反应生成G和水,则甲醛与氨的物质的量之比应为。 (6)、D的一种芳香族衍生物的结构简式为
(6)、D的一种芳香族衍生物的结构简式为 。这种衍生物满足以下条件的所有同分异构体有种,其中苯环上含有两个甲基的结构简式为。
。这种衍生物满足以下条件的所有同分异构体有种,其中苯环上含有两个甲基的结构简式为。 a.属于芳香族化合物,但不能和FeCl3溶液发生显色反应
b.1mol该有机物能与2molNaOH恰好完全反应
c.核磁共振氢谱峰面积之比为1:6:2:3
-
-