黑龙江省大庆市2020年中考化学三模试卷
试卷更新日期:2021-04-07 类型:中考模拟
一、单选题
-
1. 下列做法不符合“低碳环保”理念的是( )A、为了节约用纸,两面使用草稿纸 B、为了用热水方便,热水器长期在保温状态 C、为了提高资源利用率,将垃圾分类回收 D、减少使用私家车次数,多乘公交车2. 下列做法中一定发生化学变化的是( )A、石油分馏制汽油和柴油 B、氢氧化钠溶液制“叶脉书签 C、汽油清洗衣服上的油污 D、海水晒盐3. 下列实验操作正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、 过滤
C、
过滤
C、 测定溶液pH
D、
测定溶液pH
D、 称量氢氧化钠固体
4. 下列化学方程式与事实相符且书写正确的是( )A、炼铁高炉中生成铁: B、铝放入稀硫酸中: C、向氢氧化钠溶液中加入硫酸铜溶液: D、向小苏打中滴加稀硫酸:5. 下列对某一主题的知识归纳,完全正确的一组是( )
称量氢氧化钠固体
4. 下列化学方程式与事实相符且书写正确的是( )A、炼铁高炉中生成铁: B、铝放入稀硫酸中: C、向氢氧化钠溶液中加入硫酸铜溶液: D、向小苏打中滴加稀硫酸:5. 下列对某一主题的知识归纳,完全正确的一组是( )A.化学与环境
B.化学与安全
①减少化石燃料燃烧可控制雾霾产生
②鼓励生活垃圾焚烧处理
①房间里着火应立即打开门窗
②天然气泄漏应立即打开排气扇换气
C.化学与营养
D.化学与材料
①蔬菜、水果中富含维生素
②老年人缺钙会造成骨质疏松
①塑料、纤维、橡胶都是合成材料
②纯金属、合金都是金属材料
A、A B、B C、C D、D6. 下列叙述错误的是( )A、用pH试纸测定雨水的pH为5.6 B、食用苏打饼干可缓解因胃酸过多引起的不良症状 C、空气的成分按体积分数计算,氧气约占21% D、活性炭可用于除去水中的颜色和异味7. 下列各组依据实验目的设计的实验方案中合理的是( )选项
实验目的
实验操作
A
验证可燃性气体中含有H2
点燃气体,在火焰上方罩干冷烧杯,观察烧杯内壁是否出现液滴
B
除去NaCl中的Na2SO4
加水溶解,再加过量BaCl2溶液后过滤、蒸发、结晶
C
检验NaOH是否完全变质
取样加水后滴加无色酚酞溶液,观察溶液颜色是否变红
D
鉴别化肥KNO3和NH4Cl
取样与熟石灰混合研磨,闻气味
A、A B、B C、C D、D8. 下列图象分别与选项中的操作相对应,其中合理的是()A、 向pH为13的氢氧化钠溶液中加水
B、
向pH为13的氢氧化钠溶液中加水
B、 向一定质量二氧化锰固体中加一定质量过氧化氢溶液
C、
向一定质量二氧化锰固体中加一定质量过氧化氢溶液
C、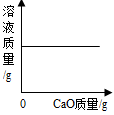 温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D、
温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D、 向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液
9. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液
9. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( ) A、甲物质的溶解度大于乙物质的溶解度 B、t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g C、t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 D、t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙10. 在天平两端的托盘上各放一个烧杯,均盛有等质量的足量的稀硫酸,天平平衡。然后向左边烧杯中加入18g镁粉,向右边的烧杯加入8.5g铜粉天平失去平衡。要使天平再次平衡,应向右边的烧杯中加入铝的质量为 ( )A、18g B、16.5g C、9g D、1.5g
A、甲物质的溶解度大于乙物质的溶解度 B、t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g C、t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 D、t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙10. 在天平两端的托盘上各放一个烧杯,均盛有等质量的足量的稀硫酸,天平平衡。然后向左边烧杯中加入18g镁粉,向右边的烧杯加入8.5g铜粉天平失去平衡。要使天平再次平衡,应向右边的烧杯中加入铝的质量为 ( )A、18g B、16.5g C、9g D、1.5g二、填空题
-
11. 化学源于生活,生活中蕴含化学。(1)、空气中含量最多的物质是 (填化学式)(2)、标出氧化铁中铁元素的化合价(3)、喝了汽水以后,常常会打嗝,这是因为(4)、厨房里做饭用的燃料主要是天然气,它的优点是(5)、家中养的绿色植物,发现叶片发黄,可以为该植物补充的化肥种类是12. 元素周期表是学习和研究化学的重要工具。下面是元素周期表的部分信息:

认真分析信息, 回答:
(1)、地壳中含量最多的元素的原子序数是;
(2)、分析上表规律, 可推知,表中X=;(3)、 表示的是(写粒子符号); (4)、写出一个由1、7、8、16号四种元素组成的化合物的化学式。
表示的是(写粒子符号); (4)、写出一个由1、7、8、16号四种元素组成的化合物的化学式。
三、实验题
-
13. 如图是实验室常用的部分实验装置,请按要求回答问题
 (1)、写出标有编号的仪器名称:① , ②。(2)、实验室用加热高锰酸钾的方法制取氧气,所选择的发生装置是 (填字母序号),写出反应的化学方程式;若用E收集氧气,检验氧气收集满的方法是。(3)、将装置B、E、F相连接用于制取二氧化碳气体并验证其化学性质,若E装置中装有饱和碳酸氢钠溶液,则F装置中可观察到的现象:试管中石蕊溶液 , 烧杯中澄清石灰水。
(1)、写出标有编号的仪器名称:① , ②。(2)、实验室用加热高锰酸钾的方法制取氧气,所选择的发生装置是 (填字母序号),写出反应的化学方程式;若用E收集氧气,检验氧气收集满的方法是。(3)、将装置B、E、F相连接用于制取二氧化碳气体并验证其化学性质,若E装置中装有饱和碳酸氢钠溶液,则F装置中可观察到的现象:试管中石蕊溶液 , 烧杯中澄清石灰水。四、流程题
-
14. 某化学兴趣小组欲分离KCl和CaCl2混合溶液,得到都含单一溶质的两种溶液。他们设计了如图所示的实验流程:

供选试剂:K2SO4溶液、Na2CO3溶液、K2CO3溶液、稀盐酸、稀硫酸
(1)、步骤①中,分离A、B的实验操作名称是 ,试剂a是 。(2)、沉淀B表面残留少量滤液,需用蒸馏水多次洗涤,为了检验沉淀B是否洗涤干净,可向步骤②的最后一次洗涤液中加入的试剂是 (双选,填序号)A NaOH溶液 B CaCl2溶液 C NaCl溶液 D AgNO3和HNO3混合溶液
(3)、步骤③中,发生反应的化学方程式为(4)、要达到预期的目的,还需要改进的方法为五、推断题
-
15. 下列图示中 A 为生活中使用最多的金属,C 为胃酸的主要成分,G 为蓝色沉淀。各 物质间的反应均在溶液中进行,相互转化关系如下图所示。

请回答以下问题:
(1)、B 溶液中的阴离子是 , E 的化学式为(2)、反应②的化学方程式(3)、①②③④四个反应中属于复分解反应的是(4)、H 的一种用途六、科学探究题
-
16. 洋洋同学做将浓硫酸滴到一块小布上的实验,发现生成的炭上冒白烟,推测炭能与浓硫酸反应。欲探究其生成物成分,通过简单分析及实验确定无H2和O2 , 因此继续进行如下探究。
(查阅资料)
①SO2性质:能使品红溶液褪色,能被高锰酸钾溶液吸收,能使澄清石灰水变浑浊;
②CO可与PdCl2溶液反应:PdCl2+CO+H2O Pd(黑) +2HCl+CO2;不与KMnO4溶液反应。
(提出猜想)生成物的成分可能为:I.H2O、CO、SO2;
Ⅱ.H2O、CO2、SO2
Ⅲ.H2O、CO、CO2、SO2
(实验验证)洋洋同学设计了如下实验:

(分析讨论)
请根据实验目的,按气流从左到右的方向将实验仪器组装完整:
(1)、A→ → →D→(2)、装置E中所加药品是 , 作用是(3)、装置C中②的作用是除去SO2气体,则③试管中品红溶液的作用是(4)、若D中澄清石灰水变浑浊,则D中发生反应的化学方程式为(5)、实验结束冷却后,从实验安全角度考虑,清洗装置A中试管时不能直接向其中加水冲洗,原因是(6)、(实验结论)实验观察到的部分现象是:B中未见黑色沉淀,则猜想 正确。写出炭与浓硫酸在加热条件下反应的化学方程式17. 甲同学在厨房中发现一袋白色粉末状的食用物,包装袋上表示化学成分的字迹看不清楚,于是他把该食用物带到实验室探究其成分。[猜想与假设]猜想 1:可能是苏打(Na2CO3);
猜想 2:可能是小苏打(NaHCO3);
猜想 3:可能是食盐;
猜想 4:可能是淀粉。
[查阅资料]碳酸氢钠溶液显碱性; ;
(1)、[实验探究]实验操作
实验现象
实验结论
①取样,加适量的水溶解
得到无色溶液
原物质不是
②取少量品尝
有苦涩味
原物质不是
③向上面①的溶液中滴加几滴酚酞溶液
溶液由无色变为红色
原物质是碳酸氢钠
乙同学认为,上表中实验③的结论不准确,因为。
(2)、于是乙同学进行了下面的实验:实验操作
实验现象
实验结论
④取样,滴加足量的稀盐酸
有大量气泡产生
原物质是碳酸钠
⑤向上面③中的溶液中滴加足量的
原物质是碳酸氢钠
(3)、[反思与评价]上表中实验⑷得出的结论也不严密,因为 (用化学方程式表示)。
七、计算题
-
18. 小明同学在完成实验室制取二氧化碳后,对回收的盐酸和CaCl2混合溶液(不考虑其他杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10.6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
 (1)、生成沉淀的质量为 g(2)、回收液中HCl的质量分数是多少?
(1)、生成沉淀的质量为 g(2)、回收液中HCl的质量分数是多少?
-
-
-