江苏省宜兴市丁蜀学区七校2015-2016学年九年级下学期化学一模联考考试试卷
试卷更新日期:2017-11-21 类型:中考模拟
一、选择题
-
1. 下列自然资源的利用过程中,一定发生了化学变化的是( )A、水力发电 B、将石油加热炼制,得到不同的产品 C、海水晒盐 D、利用铁矿石炼铁2. 人体内元素失衡容易导致疾病。下列疾病可能与缺铁有关的( )A、佝偻病 B、贫血症 C、侏儒症 D、甲状腺肿大3. 取少量下列物质分别放入水中,充分搅拌后能形成溶液的是( )A、石蜡 B、面粉 C、蔗糖 D、植物油4. 下列化学用语正确的是( )A、N5:5个氮原子 B、FeO:氧化铁 C、Zn2+:正二价的锌元素 D、2C:二个碳原子5. 物质都是由微粒构成的.下列物质由分子构成的是( )A、二氧化碳 B、氯化钠 C、金刚石 D、铜6. 下列物质属于合金的是( )A、青铜 B、塑料 C、合成纤维 D、合成橡胶7. 宏观与微观相联系是化学最特征的思维方式。下列对宏观现象的微观解释错误的是( )
A、温度计受热时水银柱上升,是因为汞原子受热时体积变大 B、稀盐酸和稀硫酸都能使紫色石蕊试液变红,是因为它们溶液中的阳离子都是H+ C、20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔 D、缉毒犬能根据气味发现毒品,是因为分子在不断地运动8. 除去下列物质中的少量杂质(括号内为杂质),使用的方法错误的是( )A、MnO2(KCl):加水过滤 B、N2(O2):通过灼热的铜网 C、CaO(CaCO3):高温煅烧 D、NH3(H2O):用浓硫酸洗气9. 下列各组物质投入水中,搅拌后能得到无色、澄清溶液的是( )A、KNO3、HCl、CuCl2 B、Ca(OH)2、BaCl2、Na2SO4 C、Na2CO3、NaCl、Ca(OH)2 D、NaOH、KCl、H2SO410. 下面是小青同学对部分化学知识的归纳,其中正确的一组是( )A、实验记录:①用10mL量筒量取7.025mL水;②用托盘天平称取5.6g氯化钠 B、安全常识:①酒精灯打翻起火,用湿抹布扑灭;②冬天用煤炉取暖,应保证室内通风 C、化学与健康:①人体缺维生素A会引起夜盲症;②禁止使用任何食品添加剂 D、化学与生活:①用钢丝球擦洗铝锅上的污垢;②用食醋除水垢11. 类推是学习中常用的思维方法.现有以下类推结果,其中错误的是( )①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应:②氯化钠的水溶液显中性,所以盐溶液一定显中性;③分子可以构成物质,物质一定是由分子构成的;④碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的一定是碳酸盐.
A、①②③④ B、只有①②③ C、只有②③④ D、只有①12. 下列图示与对应的叙述相符的是( )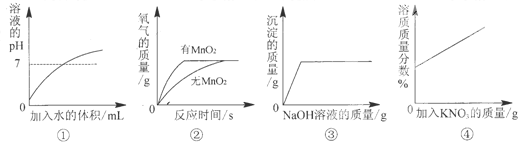 A、图①表示向稀盐酸中不断加水 B、图②表示探究过氧化氢制氧气的反应中二氧化锰的作用 C、图③表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 D、图④表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体13. 下列图示的实验操作正确的是( )A、
A、图①表示向稀盐酸中不断加水 B、图②表示探究过氧化氢制氧气的反应中二氧化锰的作用 C、图③表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 D、图④表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体13. 下列图示的实验操作正确的是( )A、 过滤
B、
过滤
B、 称取氯化钠
C、
称取氯化钠
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 测溶液的pH
14. 下图是三种物质的溶解度曲线,下列说法正确的是( )
测溶液的pH
14. 下图是三种物质的溶解度曲线,下列说法正确的是( ) A、丙物质的饱和溶液升温后,将变成不饱和溶液 B、t1℃时,甲、乙饱和溶液的溶质质量分数相等 C、t2℃时将70g甲物质加入100g水中,可得到170g溶液 D、将甲、乙饱和溶液从t2℃降到t1℃,析出甲的质量大
A、丙物质的饱和溶液升温后,将变成不饱和溶液 B、t1℃时,甲、乙饱和溶液的溶质质量分数相等 C、t2℃时将70g甲物质加入100g水中,可得到170g溶液 D、将甲、乙饱和溶液从t2℃降到t1℃,析出甲的质量大二、填空题
-
15. 过氧化苯甲酰是面粉增白剂,可以改变面粉外观,却能破坏面粉中叶酸等微量营养素,增加人的肝脏负担,过氧化苯甲酰的分子式为C14H10O4。下列关于过氧化苯甲酰的说法错误的是( )A、过氧化苯甲酰由三种元素组成 B、过氧化苯甲酰属于有机物 C、过氧化苯甲酰中含有14个碳原子、10个氢原子和4个氧原子 D、过氧化苯甲酰中碳元素的质量分数为69.4%16. 根据问题填空;
(1)、(1)人们常说:①高原上缺氧 ②生理盐水 ③胃酸过多 ④发酵粉中的小苏打。请用H、C、O、Na、Cl四种常见的元素,写出其中的化学式:①中的“氧”;②中的“盐”③中的“酸”;④中的小苏打。
(2)、(2)无土栽培是利用营养液栽培作物的一种方法。表中是栽培绿叶菜营养液配方。
①化学肥料成分中属于复合肥的肥料名称是。
②该营养液中存在的一种金属离子符号。
③硫酸镁的化学式是:。
④若在实验里配制2升该营养液,需要称取的硫酸钾的质量是毫克。
17. 写出下列反应的化学方程式,并在括号内注明基本反应类型:(1)、氢氧化钠吸收空气中的CO2:(2)、熟石灰处理硫酸厂的废水: , ( )反应。(3)、氨气在氧气中燃烧生成氮气和水( )反应18. 某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题: (1)、A中反应的化学方程式;B中白磷不燃烧,原因是。(2)、C,D中看到的现象分别是、。(3)、用化学方程式表示E中颜色变化的原因;用F装置收集气体的依据是。
(1)、A中反应的化学方程式;B中白磷不燃烧,原因是。(2)、C,D中看到的现象分别是、。(3)、用化学方程式表示E中颜色变化的原因;用F装置收集气体的依据是。三、推断题
-
19. 某工厂综合加工海水的主要步骤如图所示.

请根据图示回答下列问题:
(1)、操作I的名称是。(2)、试剂1是(写化学式,下同),白色沉淀D是。(3)、溶液B中含有的溶质是。向溶液B加入试剂2后,在溶液中可观察到的现象。(4)、在熔融状态下电解无水氯化镁会产生一种金属单质和一种双原子分子的气体单质,该反应的化学方程式是。四、探究题
-
20. 氮化镁是一种应用范围非常广泛的无机化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等。某校化学研究小组用镁与氮气反应制备氮化镁(Mg3N2),并用实验方法测定氮化镁的纯度。
I.制备氮化镁
【查阅资料】
①(NH4)2SO4+2NaNO2 2N2↑+Na2SO4+4H2O,该反应为放热反应。
②饱和硫酸亚铁溶液能吸收氧气;稀硫酸能吸收氨气。
③在常温下或温度不高的条件下镁几乎与水不反应。
【实验】
制备氮化镁的装置示意图如下
 (1)、D装置的作用是 , G装置的作用是。(2)、E装置中发生反应的化学方程式为。(3)、实验时先进行(选填“A”或“E”)处加热,理由是。(4)、II.测定氮化镁的含量
(1)、D装置的作用是 , G装置的作用是。(2)、E装置中发生反应的化学方程式为。(3)、实验时先进行(选填“A”或“E”)处加热,理由是。(4)、II.测定氮化镁的含量氮化镁是浅黄色粉末,极易与水反应生成Mg(OH)2沉淀和NH3 , 反应的化学方程式为 , 氮化镁(Mg3N2)中氮元素的化合价是。
(5)、【定性分析】,步骤一:取少量氮化镁样品于试管中加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成。
步骤二:弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡。该步骤中产生气泡的化学方程式为。
(6)、【定量测定】按下图实验装置进行实验 :
:取氮化镁样品16g进行实验,I装置增重3.4g,求该样品中氮化镁的质量分数(请写出计算过程)。
(7)、球形干燥管的作用是。
-