广东省汕头市澄海区2015-2016学年九年级化学学业考试模拟试卷
试卷更新日期:2017-11-20 类型:中考模拟
一、选择题
-
1. 生活中常常会发生一些变化,下列变化属于化学变化的是( )A、樟脑球在衣柜中逐渐消失 B、吃进的食物一段时间后被消化 C、给电熨斗通电产生热能 D、在晾干的咸菜表面出现白色晶体2. 下列物质分类正确的是( )A、食盐水、空气、石油——混合物 B、金刚石、石墨、石灰石——氧化物 C、生铁、焊锡、金——合金 D、棉花、蚕丝、聚乙烯——合成材料3. 下列物质的用途与化学性质无关的是( )A、用氮气作食品包装袋的填充气 B、用熟石灰改良酸性土壤 C、用干冰人工降雨 D、用含氢氧化铝药物治疗胃酸过多4. 下列事实的结论或解释正确的是 ( )A、桂花开放时满园飘香——说明分子在不断运动 B、气体可压缩储存于钢瓶中——因为分子压缩后体积变小 C、水通电能产生氧气——说明水中含有氧分子 D、金刚石和石墨物理性质差异很大——因为它们组成的元素不同5. 某种电池的正极材料由锂(Li)、钴(Co)和氧元素组成,三种元素的化合价分别是+1、+3、-2,则该物质的化学式为( )A、LiCoO4 B、LiCoO3 C、LiCoO2 D、LiCoO6. 下列有关水的说法正确的是( )A、电解水时产生的气体的质量比是1:2 B、可用水区分CaO和CaCO3 C、硬水经过活性炭吸附变为纯净水 D、海洋有大量的水,所以不必节约用水7. 右图是加碘盐标签上的部分内容,对该加碘盐的有关说法正确的是( )
 A、食用该加碘盐能防止骨质疏松 B、这包加碘盐最少含碘酸钾10mg C、该加碘盐中的“碘”是指碘分子 D、该加碘盐易溶于水并且高温加热会发生变化8. 下列实验的先后顺序正确的是( )A、称量物质的质量时,先加质量大的砝码,后加质量小的砝码 B、向试管中滴加少量液体药品时,先把滴管伸入试管内,后捏橡胶头向试管中滴入液体药品 C、测定溶液的pH时,先用水润湿pH试纸,后蘸取溶液滴在pH试纸上 D、稀释浓硫酸时,先在烧杯倒入浓硫酸,后向烧杯中缓慢注入水9. 化肥能促进农作物的生长发育。对化肥的一些认识,你认为不正确的是( )A、NH4HCO3有刺激性氨味 B、CO(NH2)2与熟石灰混合研磨会产生氨气 C、KNO3属于复合肥料 D、要合理施用化肥,防止土壤、水体等的污染10. 下列实验设计不能达到目的的是( )A、用带火星的木条鉴别氧气和空气 B、用BaCl2溶液鉴别稀H2SO4和稀HCl C、用NaOH溶液除去CO2中少量的CO D、用适量的稀盐酸除去NaCl溶液中少量的Na2CO311. 加油站应张贴的警示标志是( )A、
A、食用该加碘盐能防止骨质疏松 B、这包加碘盐最少含碘酸钾10mg C、该加碘盐中的“碘”是指碘分子 D、该加碘盐易溶于水并且高温加热会发生变化8. 下列实验的先后顺序正确的是( )A、称量物质的质量时,先加质量大的砝码,后加质量小的砝码 B、向试管中滴加少量液体药品时,先把滴管伸入试管内,后捏橡胶头向试管中滴入液体药品 C、测定溶液的pH时,先用水润湿pH试纸,后蘸取溶液滴在pH试纸上 D、稀释浓硫酸时,先在烧杯倒入浓硫酸,后向烧杯中缓慢注入水9. 化肥能促进农作物的生长发育。对化肥的一些认识,你认为不正确的是( )A、NH4HCO3有刺激性氨味 B、CO(NH2)2与熟石灰混合研磨会产生氨气 C、KNO3属于复合肥料 D、要合理施用化肥,防止土壤、水体等的污染10. 下列实验设计不能达到目的的是( )A、用带火星的木条鉴别氧气和空气 B、用BaCl2溶液鉴别稀H2SO4和稀HCl C、用NaOH溶液除去CO2中少量的CO D、用适量的稀盐酸除去NaCl溶液中少量的Na2CO311. 加油站应张贴的警示标志是( )A、 B、
B、 C、
C、 D、
D、 12. 下列实验操作或实验设计正确的是( )A、点燃酒精灯
12. 下列实验操作或实验设计正确的是( )A、点燃酒精灯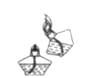 B、闻气体的气味
B、闻气体的气味 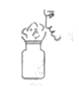 C、检查气密性
C、检查气密性 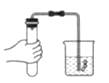 D、测定空气中氧气的含量
D、测定空气中氧气的含量 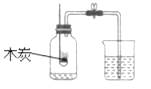 13. 下列实验操作、现象与结论对应关系正确的是( )
13. 下列实验操作、现象与结论对应关系正确的是( )选项 实验操作 现象 结论 A 用黄铜片在铜片上刻画 铜片上有划痕 黄铜的硬度比铜大 B 将两根铁丝分别伸到CuSO4溶液和AgNO3溶液中 两根铁丝表面均有固体附着 金属的活动性是Fe>Cu>Ag C 向某溶液中滴入无色酚酞试液 无色酚酞试液不变色 无色溶液一定是酸 D 向某物质加入稀硫酸 有气泡产生 该物质一定含CO32- A、A B、B C、C D、D14. 下列曲线能正确表达对应的反应或过程的是( )A、 固体溶于水 B、煅烧石灰石
B、煅烧石灰石 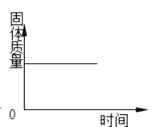 C、等质量等浓度的稀H2SO4加入金属
C、等质量等浓度的稀H2SO4加入金属 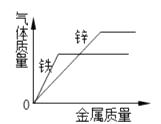 D、 混合液中加入NaOH
D、 混合液中加入NaOH
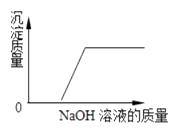
二、填空题
-
15. 回答下列问题
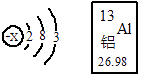 (1)、用数字和式子表示:①2个氧原子 , ②2个氮分子。(2)、右图是铝的结构示意图和在周期表中的位置图,则铝元素的相对原子质量是 , 铝离子的符号是。16. 回答生活、生产中的有关问题:(1)、厨房中的下列物质加入足量的水,能形成溶液的是 (选填序号)A、食用油 B、味精 C、面粉(2)、生活中的下列做法你认为安全的是 (选填序号)A、用甲醛溶液浸泡保鲜海鲜品 B、用碳酸氢钠焙制糕点 C、酒精着火燃烧时应立即浇水灭火 D、煤气泄漏时要马上关闭阀门,打开窗户(3)、多吃水果、蔬菜能补充的营养素是。(4)、ClO2常用于饮用水消毒,制取ClO2的化学方程式是:2NaClO2+X=2ClO2+2NaCl,则X的化学式是。17. 常见的铁矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2),用
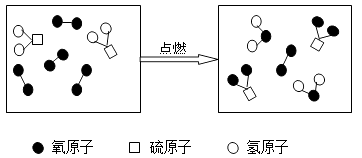
(1)、用数字和式子表示:①2个氧原子 , ②2个氮分子。(2)、右图是铝的结构示意图和在周期表中的位置图,则铝元素的相对原子质量是 , 铝离子的符号是。16. 回答生活、生产中的有关问题:(1)、厨房中的下列物质加入足量的水,能形成溶液的是 (选填序号)A、食用油 B、味精 C、面粉(2)、生活中的下列做法你认为安全的是 (选填序号)A、用甲醛溶液浸泡保鲜海鲜品 B、用碳酸氢钠焙制糕点 C、酒精着火燃烧时应立即浇水灭火 D、煤气泄漏时要马上关闭阀门,打开窗户(3)、多吃水果、蔬菜能补充的营养素是。(4)、ClO2常用于饮用水消毒,制取ClO2的化学方程式是:2NaClO2+X=2ClO2+2NaCl,则X的化学式是。17. 常见的铁矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2),用矿炼铁会产生形成酸雨的有害气体。下图微观示意图表示的反应也会产生有害气体,该反应的化学方程式是
 18. 氯化铵和硝酸钾的溶解度曲线如右图所示,回答下列问题:
18. 氯化铵和硝酸钾的溶解度曲线如右图所示,回答下列问题: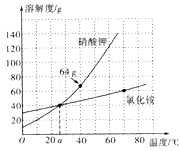 (1)、40℃时将40g硝酸钾投入到50g水中,充分搅拌,得到的溶液的质量是g。(2)、60℃时将60g硝酸钾完全溶解100g水中,冷却到a℃,析出晶体g。(3)、将a℃硝酸钾和氯化铵饱和溶液分别升高温度至60℃,此时溶液中溶质的质量分数是硝酸钾溶液(填“大于”、“等于”、“小于”)氯化铵溶液。(4)、硝酸钾中含有少量氯化铵,提纯硝酸钾的方法是。19. 根据下图回答有关问题:
(1)、40℃时将40g硝酸钾投入到50g水中,充分搅拌,得到的溶液的质量是g。(2)、60℃时将60g硝酸钾完全溶解100g水中,冷却到a℃,析出晶体g。(3)、将a℃硝酸钾和氯化铵饱和溶液分别升高温度至60℃,此时溶液中溶质的质量分数是硝酸钾溶液(填“大于”、“等于”、“小于”)氯化铵溶液。(4)、硝酸钾中含有少量氯化铵,提纯硝酸钾的方法是。19. 根据下图回答有关问题: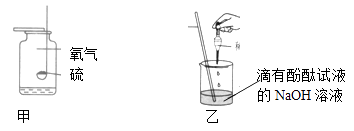 (1)、甲实验中,硫在氧气中燃烧比在空气中燃烧更剧烈,说明物质反应的剧烈程度与有关。(2)、乙实验中,向烧杯中滴入盐酸至过量,发生反应的化学方程式是。以下证明盐酸过量的操作及对现象的叙述正确的是(填序号)。
(1)、甲实验中,硫在氧气中燃烧比在空气中燃烧更剧烈,说明物质反应的剧烈程度与有关。(2)、乙实验中,向烧杯中滴入盐酸至过量,发生反应的化学方程式是。以下证明盐酸过量的操作及对现象的叙述正确的是(填序号)。A.加入蒸馏水,搅拌后溶液颜色不变 B.另加入NaOH溶液,搅拌后溶液颜色不变
C.加入AgNO3溶液,有白色沉淀产生 D.加入铁粉,有气泡产生
20. 兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿 [化学式为Cu2(OH)2CO3],能与稀硫酸反应产生硫酸铜、水和二氧化碳,加热产生氧化铜、水和二氧化碳。下面是小组同学回收铜的实验流程:
回答下列问题:
(1)、Ⅰ、Ⅱ、Ⅲ都需要进行过滤的操作,过滤用到的玻璃仪器是烧杯、玻璃棒和。溶液A所含的溶质有(填化学式)(2)、写出下列反应的化学方程式:步骤Ⅲ , 步骤Ⅴ。(3)、同一久置铜片分别通过途径甲和途径乙最终得到的铜的质量是:途径甲(选填“大于”、“等于”或“小于”)途径乙。(4)、途径甲比途径乙更好的理由是(答一点)。21. 实验室有下列的仪器装置,请回答下列问题。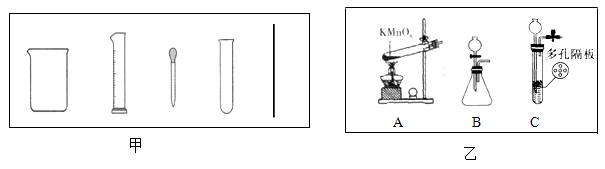 (1)、配制50g质量分数5%的氯化钠溶液,不需要甲图中的仪器是(填名称),还缺少的仪器是;在量取水时,若仰视量筒凹液面的最低处,其他操作规范,则配制的溶液的质量分数(选填“大于”、“等于”或“小于”)5%。(2)、乙图A用于实验室制取氧气,请指出中的一处错误;若用乙图B来制取氧气,则反应的化学方程式是。(3)、实验室用可图B或C来制取CO2 , C装置相对于B操作上的优点是;用排空气法收集CO2 , 检验CO2集满的操作是。(4)、右图是用排水法收集氧气的实验装置,请把下图补充完整。
(1)、配制50g质量分数5%的氯化钠溶液,不需要甲图中的仪器是(填名称),还缺少的仪器是;在量取水时,若仰视量筒凹液面的最低处,其他操作规范,则配制的溶液的质量分数(选填“大于”、“等于”或“小于”)5%。(2)、乙图A用于实验室制取氧气,请指出中的一处错误;若用乙图B来制取氧气,则反应的化学方程式是。(3)、实验室用可图B或C来制取CO2 , C装置相对于B操作上的优点是;用排空气法收集CO2 , 检验CO2集满的操作是。(4)、右图是用排水法收集氧气的实验装置,请把下图补充完整。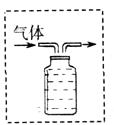 (5)、实验室用锌粒与稀硫酸反应制取氢气,发生装置如乙图图C所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,为不影响生成的气体量,则下列物质中,最适宜从长颈漏斗中添加的是 (填字母)。A、水 B、碳酸钠溶液 C、硫酸钠溶液 D、澄清石灰水MnO2
(5)、实验室用锌粒与稀硫酸反应制取氢气,发生装置如乙图图C所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,为不影响生成的气体量,则下列物质中,最适宜从长颈漏斗中添加的是 (填字母)。A、水 B、碳酸钠溶液 C、硫酸钠溶液 D、澄清石灰水MnO2三、推断题
-
22. A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钠和碳酸钠六种物质中的某一种,A、B都是黑色固体,E属于盐,它们之间的相互关系如右图所示(实连线“—”表示
 物质间能反应, 虚
物质间能反应, 虚  连线“虚线”表示物质间不能反应)。请回答下列问题:
连线“虚线”表示物质间不能反应)。请回答下列问题: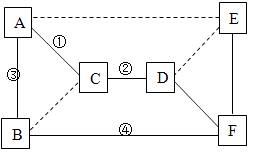 (1)、C的化学式是。(2)、A与B反应的化学方程式为。(3)、E与F反应的化学方程式为 , 该反应与上图关系中(从①~④中选填序号)的反应都属于复分解反应。(4)、在上图中,三个虚线连接中存在转化关系的有(填物质化学式): → , → 。
(1)、C的化学式是。(2)、A与B反应的化学方程式为。(3)、E与F反应的化学方程式为 , 该反应与上图关系中(从①~④中选填序号)的反应都属于复分解反应。(4)、在上图中,三个虚线连接中存在转化关系的有(填物质化学式): → , → 。四、探究题
-
23. 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如右图),为确认其中的溶质,同学们进行了如下的探究活动。请你参与到其中去,回答有关问题。
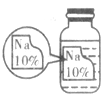
【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想IV:该溶液的溶质是NaHCO3.
(1)、【查阅资料】常温下物质的相关信息如下表:物质
NaCl
NaOH
Na2CO3
NaHCO3
常温下的溶解度/g
36
109
21.5
9.6
常温下稀溶液的pH
7
13
11
9
从物质的相关信息可知,该溶液的溶质不是NaHCO3 , 因为常温下NaHCO3溶液溶质的质量分数最大是(精确到01.%)。
(2)、【进行实验】①测定溶液的pH大于7,该溶液的溶质不是(填化学式)。
②同学们又进行了如下实验,实验过程如下:
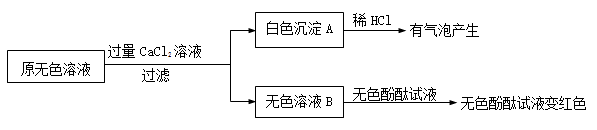
①产生白色沉淀的化学方程式是。
②实验可以判断原无色溶液中含有的溶质有。
(3)、【获得结论】该瓶原来装的无色溶液的溶质是NaOH,并且(填“没有”、“部分”或“全部”)变质。
(4)、【拓展】提纯该无色溶液的步骤是:先向无色溶液中加入适量的 , 然后过滤。反应化学方程式是。
五、计算题
-
24. 蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收。丙氨酸(化学式为C3H7O2N)就是其中的一种。请回答下列问题:(1)、丙氨酸分子中H、O的原子个数比为。(2)、丙氨酸的相对分子质量是 , 氮元素的质量分数为(计算结果精确到0.1%)。(3)、合格奶粉每100g中含蛋白质约18g,蛋白质中氮元素的平均质量分数为16%。现测定某奶粉每100g中含有氮元素的质量为2g,则该奶粉属于(填“合格”或“不合格”)奶粉。25. 某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如下图所示。
 (1)、该同学能收集到的二氧化碳的质量多少?(写出计算过程)(2)、该同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
(1)、该同学能收集到的二氧化碳的质量多少?(写出计算过程)(2)、该同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:Na2CO3溶液质量/g
10
20
30
40
50
60
70
沉淀质量/g
0
1
n
3
4
5
m
则m=。加入10gNa2CO3溶液时发生反应的化学方程式是。
请在下图中画出向废液中加入Na2CO3溶液时加入的Na2CO3溶液与产生的沉淀的曲线。

-
-