北京市昌平区2015-2016学年九年级二模化学考试试卷
试卷更新日期:2017-11-20 类型:中考模拟
一、选择题
-
1. 下列变化中,属于化学变化的是( )A、纸张燃烧 B、冰雪融化 C、水分蒸发 D、矿石粉碎2. 地壳中含量最多的非金属元素是( )A、氧 B、硅 C、铝 D、铁3. 下列物质在氧气中燃烧,火星四射、生成黑色固体的是( )A、红磷 B、铁丝 C、蜡烛 D、木炭4. 农业生产需要合理使用肥料。下列化肥中,属于磷肥的是( )A、NH4Cl B、K2SO4 C、KNO3 D、Ca(H2PO4)25. 下列气体中,有毒的是( )A、N2 B、O2 C、CO D、CO26. 废弃的易拉罐和塑料瓶属于( )A、厨余垃圾 B、可回收物 C、有害垃圾 D、其他垃圾7. 下列物质放入水中,能形成溶液的是( )A、面粉 B、牛奶 C、白糖 D、植物油8. 下列物质中,属于纯净物的是( )A、加碘食盐 B、干冰 C、硬水 D、食醋9. 下列材料中,属于合金的是( )A、玻璃 B、合成橡胶 C、生铁 D、陶瓷10. 下列数据是相应物质的pH,其中呈碱性的是( )A、液体肥皂(9.5~10.5) B、菠萝汁(3.3~5.2) C、柠檬汁(2.0~3.0) D、酱油(4.0~5.0)11. 镁有“国防金属”的美誉。在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是
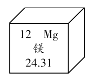 ( )A、原子序数为12 B、核外电子数为24 C、元素符号为Mg D、相对原子质量为24.3112. 能用于治疗胃酸过多症的物质是( )A、蔗糖 B、食盐 C、食醋 D、小苏打13. 下列物质露置于空气中,一段时间后,质量减小的是( )A、碳酸钙 B、氯化钠 C、浓盐酸 D、氢氧化钠14. 下列物质的用途中,利用其化学性质的是( )A、液氮用作冷冻剂 B、干冰用于人工降雨 C、氧气用于气焊 D、浓硫酸用作干燥剂15. 下列微粒中,能表示2个氢分子的是( )A、2H B、2H+ C、H2O D、2H216. 在铁制品上连接比铁活泼的金属是防止铁生锈的方法之一。下列金属中,可行的是( )A、银 B、金 C、铜 D、锌17. 向100 g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是 ( )
( )A、原子序数为12 B、核外电子数为24 C、元素符号为Mg D、相对原子质量为24.3112. 能用于治疗胃酸过多症的物质是( )A、蔗糖 B、食盐 C、食醋 D、小苏打13. 下列物质露置于空气中,一段时间后,质量减小的是( )A、碳酸钙 B、氯化钠 C、浓盐酸 D、氢氧化钠14. 下列物质的用途中,利用其化学性质的是( )A、液氮用作冷冻剂 B、干冰用于人工降雨 C、氧气用于气焊 D、浓硫酸用作干燥剂15. 下列微粒中,能表示2个氢分子的是( )A、2H B、2H+ C、H2O D、2H216. 在铁制品上连接比铁活泼的金属是防止铁生锈的方法之一。下列金属中,可行的是( )A、银 B、金 C、铜 D、锌17. 向100 g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是 ( )
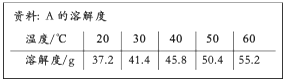 A、②中A的质量分数最大 B、③⑤中A的质量分数相等 C、②④⑤的溶液为饱和溶液 D、①③④⑤中没有固体存在18. 甲和乙在点燃条件下反应生成丙和丁。反应前后分子变化的微观示意图如下:
A、②中A的质量分数最大 B、③⑤中A的质量分数相等 C、②④⑤的溶液为饱和溶液 D、①③④⑤中没有固体存在18. 甲和乙在点燃条件下反应生成丙和丁。反应前后分子变化的微观示意图如下:
甲 乙 丙 丁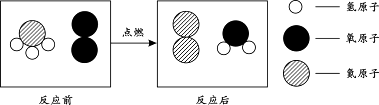
下列说法中,不正确的是( )A、一个甲分子中含有4个原子 B、该反应的基本类型为置换反应 C、生成物丙和丁的质量比为14:9 D、4种物质中,属于化合物的是甲和丁19. 下列实验方法中,一定能达到实验目的的是( )选项
实验目的
实验方法
A
检验一瓶气体是否为CO2
将带火星的木条伸入瓶中
B
鉴别NaCl溶液和稀盐酸
滴加无色酚酞溶液
C
分离碳酸钠和氢氧化钠的混合物
加入过量氢氧化钙溶液,过滤
D
验证物质燃烧条件之一是温度达到着火点
用导管分别对准浸没在热水和冷水中的白磷通氧气
A、A B、B C、C D、D20. 已知:C+2CuO 2Cu+CO2↑。如图表示一定质量的CuO和C固体混合物在受热过程中各物质质量随时间的变化趋势。下列说法中,不正确的是( )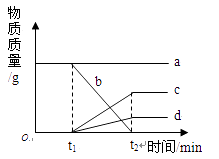 A、t1时,开始发生反应 B、t1和t2时,固体中铜元素质量保持不变 C、b是固体混合物的质量 D、d二氧化碳的质量
A、t1时,开始发生反应 B、t1和t2时,固体中铜元素质量保持不变 C、b是固体混合物的质量 D、d二氧化碳的质量二、填空题
-
21. 走进食堂。能闻到香味,说明分子具有的性质是。22. 合理膳食。副食中,富含蛋白质的是。23. 健康饮品。
(1)、白开水容易解渴,促进新陈代谢,有调节体温、输送养分等功能。白开水是(填“纯净物”或“混合物”)。(2)、碳酸饮料中含有碳酸和柠檬酸等酸性物质,过量摄入会影响某元素的吸收,儿童缺少该元素可能导致佝偻病,该元素为。(3)、酸奶经过发酵,使奶中糖、蛋白质水解成为小的分子(如乳酸等)益于消化,乳酸的化学式为C3H6O3 , 依据化学式计算出相对分子质量为90,计算式为。24. 不使用一次性餐具也是一种健康的饮食习惯。(1)、竹木筷子、塑料水杯、不锈钢勺子所使用的材料中,属于有机合成高分子材料的是。(2)、普遍使用的陶瓷餐盘的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是 , CaSiO3中硅元素和氧元素的质量比为。25. 厨房清洁。
(1)、“管道通”可使堵塞的管道畅通无阻,其有效成分之一为氢氧化钠。在使用时禁止与皮肤接触,其原因是。(2)、利用厨房中的可以溶解水壶中的水垢。26. 人们的生产生活离不开能源。(1)、天然气属于化石燃料,化石燃料还包括煤和。(2)、写出CH4完全燃烧的化学方程式 , 该反应(填“放热”或“吸热”)。27. 水是一种重要的资源。(1)、自来水厂净水过程中用到活性炭,其主要作用是。(2)、生活中常用来区分硬水和软水。(3)、电解水实验揭示了水的组成,发生反应的化学方程式为。已知同温同压下,气体的体积比等于气体的分子个数比。该实验中,能够说明水的化学式为“H2O”的实验现象是。28. 自热米饭是一种快餐食品。(1)、菜肴包的包装材料是铝箔。金属铝可以压制成铝箔,说明其具有良好的。(2)、食品包装中填充N2以防腐,其原因是。(3)、饭盒底部有用塑料膜密封的生石灰,使用时需将膜撕掉,倒入水,这时会发生反应放出热量,该反应的化学方程式为。 29. 阅读下面科普短文。
29. 阅读下面科普短文。敦煌石窟被誉为20世纪最有价值的文化发现,也是一座丰富多彩的颜料标本博物馆。经过大量的研究证明,敦煌壁画、彩塑的颜料大都是无机矿物颜料,而且大都为天然矿物颜料。如红色颜料中的朱砂、土红,蓝色颜料中的青金石、石青,绿色颜料中的石绿、氯铜矿,白色颜料中的高岭土、方解石和石膏,黑色颜料中的铁黑。还有一部分无机颜料是人工制造的,如用炼丹术(铅氧化)制成的红色颜料铅丹、人工合成的群青等。有极少量的植物性的有机颜料,如红色颜料胭脂,黄色颜料藤黄等。天然矿物颜料,在通常条件下都比较稳定。如黑暗潮湿洞窟壁画中的土红和露天常年曝晒壁画中的土红,都看不出它们之间的区别。朱砂有不同程度的变暗,色彩及明亮度不如原来艳丽,但色相未变。唯独人造无机颜料铅丹发生严重变色,在潮湿、光辐射(特别是紫外线)作用下,铅丹经过转化最终成为棕黑色的二氧化铅(PbO2)。历代应用的大量艳丽的颜料反映了我国古代对矿物、植物的综合运用,颜料化学及其冶炼技术的高度发展。对颜料的科学分析获得了颜料的化学、物理性能,了解了一些颜料褪色、变色、产生病害及胶质老化等问题。为预防颜料变色、保护文物提供了科学依据,对文物的研究和保护至关重要。
依据文章内容,回答下列问题。
(1)、土红、朱砂、铅丹的主要化学成分分别是①Fe2O3 ②HgS ③Pb3O4 , 其中属于氧化物的是(填数字序号)。(2)、敦煌壁画、彩塑的无机颜料的来源有。(3)、模拟敦煌莫高窟壁画的材料和结构,制作土红、朱砂、铅丹三种颜料的壁画试样,置于湿度90%,同一光照强度210天。下列吸光度-波长图像中,表示铅丹在光照前、后数据的是(填字母序号)。小资料:吸光度-波长图像表示颜料对光的吸收程度。
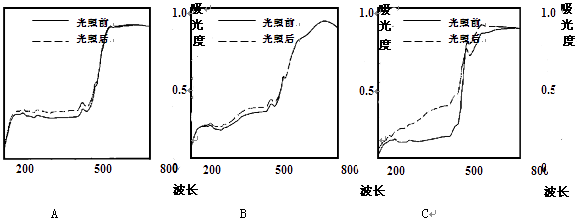 (4)、敦煌壁画、彩塑颜料中棕黑色的二氧化铅是由转化生成的。(5)、请你提一条保护壁画、彩塑颜料的建议:。30. 二氧化钛(TiO2)是许多反应的催化剂。工业上用钛铁矿【主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2(不与H2SO4反应且不溶于水)】作原料,制取二氧化钛及绿矾(FeSO4·7H2O),其生产流程如下:
(4)、敦煌壁画、彩塑颜料中棕黑色的二氧化铅是由转化生成的。(5)、请你提一条保护壁画、彩塑颜料的建议:。30. 二氧化钛(TiO2)是许多反应的催化剂。工业上用钛铁矿【主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2(不与H2SO4反应且不溶于水)】作原料,制取二氧化钛及绿矾(FeSO4·7H2O),其生产流程如下: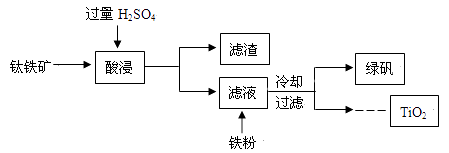 (1)、加入H2SO4后,发生的反应有 和。(2)、加入铁粉,发生置换反应的化学方程式为。(3)、以TiO2为原料还可以制取金属Ti。请将其中的一步反应的化学方程式补充完整:TiO2+2Cl2+C TiCl4 +。31. 回收利用废金属可减少资源浪费和环境污染。某工厂利用含铜废料(主要含Cu、Zn,其他杂质不溶于水、不参加反应)制取铜并得到硫酸锌溶液,主要流程如下。
(1)、加入H2SO4后,发生的反应有 和。(2)、加入铁粉,发生置换反应的化学方程式为。(3)、以TiO2为原料还可以制取金属Ti。请将其中的一步反应的化学方程式补充完整:TiO2+2Cl2+C TiCl4 +。31. 回收利用废金属可减少资源浪费和环境污染。某工厂利用含铜废料(主要含Cu、Zn,其他杂质不溶于水、不参加反应)制取铜并得到硫酸锌溶液,主要流程如下。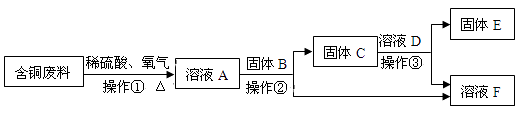
已知:2Cu + 2H2SO4 + O2 = 2CuSO4 + 2H2O
(1)、溶液A中的溶质是(写出所有可能)。(2)、下列说法中,正确的是。A.操作②③均包含过滤
b.为达到实验目的,应加入过量的固体B和适量的溶液D
c.ZnSO4的溶解度曲线比较平缓。若想获得ZnSO4晶体,应将溶液F蒸发结晶
32. 下列字母A~F所表示的物质均为初中化学常见的物质,它们由氢、碳、氧、氯、钠、钙、铁中的1~3种元素组成。(1)、固体氧化物A可用于制备改良酸性土壤的碱,A的俗称是。(2)、固体单质B完全燃烧和不完全燃烧生成两种完全不同的气体,其完全燃烧反应的化学方程式为。(3)、红色粉末C与气体D在高温条件下反应得到黑色粉末,化学方程式为。(4)、如图所示(夹持仪器略去,K1、K2均关闭),打开K1 , 液体全部流下,立即关闭K1 , 观察到产生大量气泡,且烧杯中F的溶液变浑浊。充分反应后,打开K1和K2 , 使液体全部流入锥形瓶,瓶中的溶液变浑浊。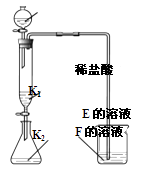
①用化学方程式表示烧杯中溶液变浑浊的原因。
②反应后锥形瓶里的溶液中含有的溶质是(写出所有可能)。
33. 某同学在实验室做如下实验。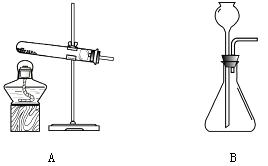 (1)、在装置A中,用高锰酸钾制取氧气的化学方程式为。(2)、在装置B中,用过氧化氢溶液和二氧化锰制取氧气的化学方程式为;用大理石和稀盐酸制取二氧化碳的化学方程式为。34. 用图所示装置测定空气中氧气的体积分数,实验时先在实际容积为250mL的集气瓶中装进50mL水,按图连好仪器。
(1)、在装置A中,用高锰酸钾制取氧气的化学方程式为。(2)、在装置B中,用过氧化氢溶液和二氧化锰制取氧气的化学方程式为;用大理石和稀盐酸制取二氧化碳的化学方程式为。34. 用图所示装置测定空气中氧气的体积分数,实验时先在实际容积为250mL的集气瓶中装进50mL水,按图连好仪器。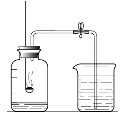 (1)、检查装置气密性。方法是将导气管放入水中,双手捂住集气瓶, 观察到烧杯中有气泡冒出;松开手后,导气管内有液柱,证明气密性良好。松开手后,导气管内有液柱的原因是。(2)、写出白磷燃烧反应的化学方程式。(3)、若实验成功,最终集气瓶中水的体积约为mL。35. 根据下列图示的实验基本操作,回答下列问题:
(1)、检查装置气密性。方法是将导气管放入水中,双手捂住集气瓶, 观察到烧杯中有气泡冒出;松开手后,导气管内有液柱,证明气密性良好。松开手后,导气管内有液柱的原因是。(2)、写出白磷燃烧反应的化学方程式。(3)、若实验成功,最终集气瓶中水的体积约为mL。35. 根据下列图示的实验基本操作,回答下列问题: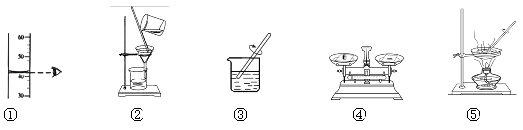 (1)、若要完成“粗盐中难溶性杂质的去除”的实验,需要进行的操作步骤依次是(填数字序号),操作③中玻璃棒的作用是。(2)、若要配制200 Kg溶质的质量分数为7%的KNO3溶液作无土栽培的营养液,需KNO3的质量为Kg,主要进行的操作步骤依次是(填数字序号)。36. 化学兴趣小组利用如下装置验证CO2能与NaOH反应。(装置气密性良好)
(1)、若要完成“粗盐中难溶性杂质的去除”的实验,需要进行的操作步骤依次是(填数字序号),操作③中玻璃棒的作用是。(2)、若要配制200 Kg溶质的质量分数为7%的KNO3溶液作无土栽培的营养液,需KNO3的质量为Kg,主要进行的操作步骤依次是(填数字序号)。36. 化学兴趣小组利用如下装置验证CO2能与NaOH反应。(装置气密性良好)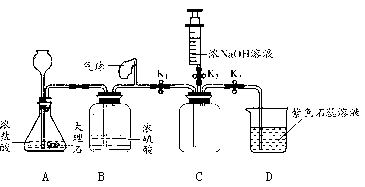 (1)、关闭K2 , 打开K1、K3 , 当D中出现的现象时,可确定C中充满CO2。(2)、C中充满CO2后,关闭K1 , 打开K2 , 将注射器中5mL浓NaOH溶液推入C中,观察到D中液体流入C中,说明CO2与NaOH发生反应。C中反应的化学方程式是。此过程中,C中压强的变化过程是。(3)、小组同学发现此实验有不足,请你指出一处,写出改进方案。
(1)、关闭K2 , 打开K1、K3 , 当D中出现的现象时,可确定C中充满CO2。(2)、C中充满CO2后,关闭K1 , 打开K2 , 将注射器中5mL浓NaOH溶液推入C中,观察到D中液体流入C中,说明CO2与NaOH发生反应。C中反应的化学方程式是。此过程中,C中压强的变化过程是。(3)、小组同学发现此实验有不足,请你指出一处,写出改进方案。三、探究题
-
37. 暖贴的发热材料主要由铁粉、活性炭、食盐、水等物质构成。

暖贴内部发热材料的截面图
【提出问题】
发热材料中各主要物质起到了什么作用?
【猜想与假设】
Ⅰ. 铁粉生锈,发生氧化反应,放出热量。
Ⅱ. 活性炭能加快铁粉氧化的速率。
III. 食盐能加快铁粉氧化的速率。
【进行实验】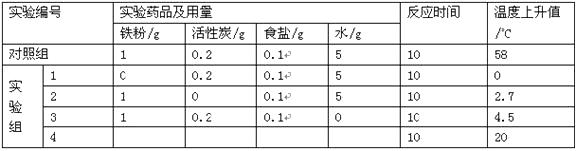
【解释与结论】(1)、铁生锈的条件是。(2)、已知铁粉在一定条件下生锈,发生氧化反应的产物可能是Fe(OH) 3 , 该反应的化学方程式为。(3)、分析(填实验编号)数据,可证明猜想与假设Ⅱ正确。(4)、分析实验组4与对照组数据,可证明猜想与假设III正确。请填写表中空缺数据。(5)、某同学认为没有必要进行实验组1,你是否同意他的观点并说明理由。(6)、某同学质疑此实验中忽略了发热材料中的水。你认为分析(填实验编号)的数据,可证明水的作用。四、计算题
-
38. 取某食用碱样品12g(主要成分为Na2CO3 , 其他为NaCl),向样品中加入98.6g某浓度的稀盐酸恰好完全反应,得到氯化钠溶液的质量为106.2g。请计算:(1)、生成二氧化碳的质量是g。(2)、最终得到的氯化钠溶液中,溶质的质量(写出计算过程及结果)。
-