2016年上海市杨浦区高考化学一模试卷
试卷更新日期:2016-08-18 类型:高考模拟
一、选择题
-
1. 物质在下列应用中,利用了其还原性的是( )A、纯碱去油污 B、铝冶炼金属 C、硝酸制炸药 D、漂粉精漂白织物2. 有关化学用语的表述正确的是( )A、轨道表示式表示N2中的共用电子对:
 B、
B、 只能是氢分子的比例模型
C、
只能是氢分子的比例模型
C、 只能是氮分子的球棍模型
D、CH4分子的比例模型:
只能是氮分子的球棍模型
D、CH4分子的比例模型:  3. 下列关于砹(85At)及其化合物的说法中,正确的是( )A、稳定性:HAt>HCl B、氧化性:At2>I2 C、At2为分子晶体 D、NaAt的水溶液呈碱性4. 化学式为N2H6SO4的某晶体,其晶体类型与硫酸铵相同,则N2H6SO4晶体中不存在( )A、离子键 B、共价键 C、分子间作用力 D、阳离子5. 仅用蒸馏水,不能鉴别的一组物质是( )A、汽油、甘油和四氯化碳 B、葡萄糖、蔗糖和纯碱 C、溴蒸气和二氧化氮 D、碘和高锰酸钾6. 下列反应的产物中,只存在+3价铁元素或氮元素的是( )A、过量的铁丝在氯气燃烧 B、过量的铁粉与溴水反应 C、烧碱溶液吸收NO2 D、硝酸铜受热分解7. 下列各组数据比较,前者比后者小的是( )A、氯水与氨水中微粒种类 B、乙烷与苯分子中碳碳键键长 C、氯化铯与氯化钠的熔点 D、Al2O3与AlCl3的熔点8. 右图是用点滴板探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水后,立即用培养皿罩住整个点滴板.下列对实验现象的解释正确的是( )
3. 下列关于砹(85At)及其化合物的说法中,正确的是( )A、稳定性:HAt>HCl B、氧化性:At2>I2 C、At2为分子晶体 D、NaAt的水溶液呈碱性4. 化学式为N2H6SO4的某晶体,其晶体类型与硫酸铵相同,则N2H6SO4晶体中不存在( )A、离子键 B、共价键 C、分子间作用力 D、阳离子5. 仅用蒸馏水,不能鉴别的一组物质是( )A、汽油、甘油和四氯化碳 B、葡萄糖、蔗糖和纯碱 C、溴蒸气和二氧化氮 D、碘和高锰酸钾6. 下列反应的产物中,只存在+3价铁元素或氮元素的是( )A、过量的铁丝在氯气燃烧 B、过量的铁粉与溴水反应 C、烧碱溶液吸收NO2 D、硝酸铜受热分解7. 下列各组数据比较,前者比后者小的是( )A、氯水与氨水中微粒种类 B、乙烷与苯分子中碳碳键键长 C、氯化铯与氯化钠的熔点 D、Al2O3与AlCl3的熔点8. 右图是用点滴板探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水后,立即用培养皿罩住整个点滴板.下列对实验现象的解释正确的是( )
选项
实验现象
解释
A
红色石蕊试纸变蓝
NH3极易溶于水
B
浓硫酸附近无白烟
NH3与浓硫酸不发生反应
C
氯化铝溶液变浑浊
NH3与AlCl3溶液反应:Al3++3OH﹣→Al(OH)3↓
D
浓盐酸附近有白烟
NH3与挥发出的HCl反应:NH3+HCl→NH4Cl
A、A B、B C、C D、D9. 有机物M的结构如图所示.关于M的描述正确的是( ) A、分子式为C8H6O6 B、能发生中和、取代、消去、氧化、加成反应 C、1molM与溴水发生反应的产物可能有3种 D、1molM与足量氢氧化钠溶液反应,消耗4molNaOH10. 用如图装置研究电化学原理,下列分析中错误的是( )
A、分子式为C8H6O6 B、能发生中和、取代、消去、氧化、加成反应 C、1molM与溴水发生反应的产物可能有3种 D、1molM与足量氢氧化钠溶液反应,消耗4molNaOH10. 用如图装置研究电化学原理,下列分析中错误的是( )
选项
连接
电极材料
分析
a
b
A
K1 K2
石墨
铁
模拟铁的吸氧腐蚀
B
K1 K2
锌
铁
模拟钢铁防护中牺牲阳极的阴极保护法
C
K1 K3
石墨
铁
模拟电解饱和食盐水
D
K1 K3
铁
石墨
模拟钢铁防护中外加电流的阴极保护法
A、A B、B C、C D、D11. 向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起( )A、溶液的pH增大 B、CH3COOH的电离程度增大 C、溶液的导电能力减小 D、溶液的c(OH﹣)减小12. 工业上常用如下的方法从海水中提溴:浓缩海水 粗产品溴 溴蒸气 物质X 产品溴,下列说法错误的是( )A、步骤①的主要反应为:Cl2+2Br﹣→Br2+2Cl﹣ B、物质X为HBrO C、步骤②③的目的是富集溴元素 D、步骤②利用了溴易挥发的性质13. 由右表提供数据及相关物质结构知识,反应:SiCl4(g)+2H2(g)→Si(s)+4HCl(g),生成1mol晶体硅的热效应是( )化学键
Si﹣Cl
H﹣H
Si﹣Si
H﹣Cl
键能(kJ/mol)
360
436
176
431
A、吸收236KJ B、放出236kJ C、放出116kJ D、吸收116kJ14. 利用图所示装置进行下列实验,能得出相应实验结论的是( )选项
①
②
③
实验结论

A
浓硫酸
Cu
KMnO4溶液褪色
SO2有漂白性
B
浓盐酸
MnO2
FeBr2溶液变为黄色
氧化性:Cl2>Br2
C
稀硫酸
碳酸钠
CaCl2溶液无明显变化
CO2不与CaCl2溶液反应
D
浓硫酸
蔗糖
溴水褪色
浓硫酸具有脱水性、吸水性
A、A B、B C、C D、D15. 现有某温度下的KCl饱和溶液m1g,溶质的质量分数为ω1%.对其采取某种措施后析出mgKCl晶体,所得母液的质量为m2g,溶质的质量分数为ω2%,则下列关系正确的是( )A、原条件下KCl的溶解度小于ω1g B、m1•ω1%﹣m=m2•ω2% C、ω1一定大于ω2 D、m1﹣m2≤m16. 80℃,0.1mol/L NaHB溶液中c(H+)>c(OH﹣),可能正确的关系是( )A、c(Na+)+c(H+)=c(HB﹣)+2c(B2﹣) B、溶液的pH=1 C、c(H+)∙c(OH﹣)=10﹣14 D、c(Na+)=c(H2B)+c(HB﹣)17. 某溶液中含有下列离子中的五种:Ba2+、Fe2+、Al3+、Fe3+、Mg2+、HCO3﹣、CO32﹣、Cl﹣、NO3﹣、SO42﹣ , 浓度均为0.1mol/L.向其中加入足量的盐酸,有气体生成且反应后溶液中阴离子的种类没有变化.以下分析错误的是( )A、原溶液中不含HCO3﹣和CO32﹣ B、向加盐酸后的溶液中再加KSCN溶液,显红色 C、能确定原溶液中的五种离子 D、原溶液中有三种阳离子和两种阴离子18. 向饱和食盐水中滴加一定量浓盐酸,对出现现象的预测可能正确的是( )A、白色沉淀 B、液体分层 C、无明显现象 D、黄绿色气体19. 短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外).Z与W、W与Q的原子序数之差均为3,五种元素原子的最外层电子数之和为21,下列说法正确的是( )A、Z、W、Q三种元素的单质属于三种不同的晶体类型 B、Q氢化物的熔点高于Z氢化物的熔点 C、一定条件下,Q单质可把Y从其氢化物中置换出来 D、最高价氧化物对应水化物的酸性顺序:Q>Y>W>X20. 对有关NaClO和NaCl混合溶液的叙述正确的是( )A、该溶液中,H+、NH 、SO 、Br﹣可以大量共存 B、该溶液中,K+、OH﹣、S2﹣、NO3﹣不能大量共存 C、向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO﹣+2H+→Cl﹣+2Fe3++H2O D、向该溶液中加入浓盐酸,每产生1molCl2 , 转移电子约为6.02×1023个21. 自然界存在反应:14CuSO4+5FeS2+12H2O→7Cu2S+5FeSO4+12H2SO4 . 在该反应中( )A、产物中的SO 有一部分是氧化产物 B、5molFeS2发生反应,有10mol电子转移 C、发生氧化反应和发生还原反应的FeS2之比为7:3 D、14mol CuSO4能氧化5molFeS222. 有两份组成及质量都相等的Na2O2和Na2CO3的混合物,向第一份中加入足量的稀硫酸,放出的气体共4.48L.将此气体通入第二份混合物,充分反应后,气体体积变为4.032L(均为标准状况下体积).则原混合物中Na2O2和Na2CO3的物质的量之比为( )A、2:9 B、3:2 C、2:1 D、8:1二、综合题
-
23. H、C、N、O、Al、S是常见的六种元素.
完成下列填空:
(1)、碳元素有12C、13C和14C等同位素.在14C原子中,核外存在对自旋相反的电子.(2)、碳在形成化合物时,其所成化学键以共价键为主,原因是 .(3)、任选上述元素可组成多种四原子的共价化合物,请写出其中含非极性键的一种化合物的电子式 .(4)、上述元素可组成盐NH4Al(SO4)2 . 向10mL1mol/L NH4Al(SO4)2溶液中滴加1mol/L的NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下.
①NH4Al(SO4)2溶液中所有离子的浓度由大到小的顺序是 , 请解释阳离子浓度差异的原因 .
②写出N点反应的离子方程式 .
③若向10mL1mol/L NH4Al(SO4)2溶液中加入20mL1.2mol/LBa(OH)2溶液,充分反应后,产生沉淀 mol.
24. 氯气用途广泛,但在使用时,一般会产生氯化氢.工业上可用O2将HCl转化为Cl2 , 以提高效益,减少污染.反应为:O2+4HCl 2Cl2+2H2O
完成下列填空:
(1)、该反应化学平衡常数K的表达式为;实验测得P0压强下,HCl平衡转化率α(HCl)随反应温度T的变化如图1所示,则正反应是反应(填“吸热”或者“放热”).(2)、上述实验中若压缩体积使压强由P0增大至P1 , 在图中画出P1压强下HCl平衡转化率α(HCl)随反应温度T变化的曲线,并简要说明理由:(3)、该反应在P0、320℃条件下进行,达平衡状态A时,测得容器内n(Cl2)=7.2×10﹣3mol,则此时容器中的n(HCl)=mol.(4)、对该反应达到平衡后,以下分析正确的是(选填编号).a.增加n(HCl),对正反应的反应速率影响更大
b.体积不变加入稀有气体,对正反应的反应速率影响更大
c.压强不变加入稀有气体,对逆反应的反应速率影响更大
d.如果平衡常数K值增大,对逆反应的速率影响更大
(5)、氯元素能形成多种离子.在水溶液中1molCl﹣、1mol ClOx﹣(x=1,2,3,4)能量的相对大小如图2所示,写出B→A+C反应的热化学方程式(用离子符号表示);若有1.5molB发生反应,转移电子 mol.25. 实验小组为探究SO2的漂白性和还原性,设计了以下实验.完成下列填空:(1)、实验室用亚硫酸钠粉末跟硫酸制取二氧化硫,有下列三种硫酸溶液,应选用(选填编号),其理由是 .a.98%浓硫酸 b.70%硫酸 c.10%稀硫酸
(2)、І.漂白性用如图所示装置(气密性良好)进行实验,观察到如下现象:

ⅰ中红色褪去、
ⅱ中无变化.
①足量碱石灰的作用是 .
②从实验中可知使品红的水溶液褪色的微粒可能是 .
(3)、实验小组进一步实验如下:取等量相同浓度的品红水溶液于两支试管中,再分别加入少量Na2SO3固体和NaHSO3固体,两支试管中的品红都褪色,于是得出结论:使品红褪色的微粒肯定是HSO3﹣或SO32﹣ . 你认为这一结论是否正确 , 理由是 .(4)、ІІ.还原性将SO2通入FeCl3溶液中,使其充分反应.
①SO2与FeCl3反应的离子方程式是 , 如何检验该反应所得含氧酸根离子 .
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色.
已知:红棕色为FeSO3(墨绿色难溶物)与FeCl3溶液形成的混合色;Fe3+可氧化SO32﹣ . 则②中红棕色变为浅绿色的原因是
26. 异丙苯( )氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:
)氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下: 氧化:
 +O→
+O→  (异丙苯过氧氢)
(异丙苯过氧氢)分解:

 (丙嗣)
(丙嗣)
已知:
物质
丙酮
苯酚
异丙苯
密度(g/mL)
0.7898
1.0722
0.8640
沸点/℃
56.5
182
153
完成下列填空:
(1)、X物质是;Y物质是 .(2)、浓硫酸的作用是 , 其优点是用量少,可能的缺点是(写一条).(3)、Z物质最适宜选择(选填编号).a.NaOH b.Na2CO3 c.NaHCO3 d.CaCO3
(4)、步骤⑥分馏,工业上在分馏塔中进行,如图 ,产品T是 , 请说明理由 . 废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
,产品T是 , 请说明理由 . 废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定: ①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶.
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀.加入少许淀粉溶液.
③用0.0250mol/LNa2S2O3标准溶液滴定至终点.用去Na2S2O3溶液22.48mL.
(5)、已知:BrO3﹣+5Br﹣+6H+→3Br2+3H2O;写出苯酚与浓溴水反应的化学方程式;第1加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是 .(6)、已知:I2+2Na2S2O3→2NaI+Na2S4O6;滴定终点的现象是;该废水中苯酚的浓度是 mol/L(保留4位小数).27. 由基本有机化工原料A(C2H2)制备有机物D和聚异戊二烯的合成路线如图所示: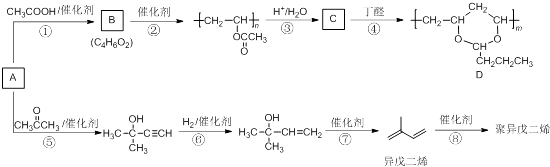
完成下列填空:
(1)、上述转化步骤中与反应①的反应类型相同的是(填编号).(2)、m与n的关系为 .(3)、异戊二烯分子中最多有个原子共平面.(4)、在异戊二烯的同分异构体中,与A具有相同官能团且分子中有支链的有机物的名称是 .(5)、参照流程图中异戊二烯的合成路线,若把步骤⑤中的反应物丙酮改为乙醛,则经过反应⑤、⑥、⑦后得到的有机物是 .28. 以有机物A和苯酚为原料合成一种医药中间体E的路线如下:
完成下列填空:
(1)、已知A的分子式为C2H2O3 , 可发生银镜反应,且具有酸性.写出A发生银镜反应的化学方程式 .(2)、有机物B 中①、②、③3个﹣OH的酸性由强到弱的顺序为;写出B与过量Na2CO3溶液反应的化学方程式 . (3)、副产物D是由2分子B生成的含有3个六元环的化合物,D的结构简式是 .(4)、已知苯酚钠和苯酚相比,不易被氧化.现由有机物B制备
中①、②、③3个﹣OH的酸性由强到弱的顺序为;写出B与过量Na2CO3溶液反应的化学方程式 . (3)、副产物D是由2分子B生成的含有3个六元环的化合物,D的结构简式是 .(4)、已知苯酚钠和苯酚相比,不易被氧化.现由有机物B制备 ,写出对应各步反应中依次所需的试剂和反应条件 . (5)、写出符合下列条件的E的所有同分异构体的结构简式(不考虑立体异构).
,写出对应各步反应中依次所需的试剂和反应条件 . (5)、写出符合下列条件的E的所有同分异构体的结构简式(不考虑立体异构).①苯环上只有2个位置未被取代,且这两个位置上的氢原子化学环境相同;
②与FeCl3溶液不发生显色反应;
③能发生银镜反应.
29. 氯化亚铜(CuCl)广泛用于有机合成、气体吸收、冶金、医药化工等行业.(1)、工业上氯化亚铜可由下列反应制备:2CuSO4+Na2SO3+2NaCl+Na2CO3→2CuCl↓+3Na2SO4+CO2↑.制备过程中需要20%的CuSO4溶液,配制100g 该CuSO4溶液需要胆矾 g,需要水 g.
(2)、实验室可用如下方法制备少量CuCl:取10mL 0.2mol/L CuCl2溶液,加入0.128g铜屑和36.5%的浓盐酸(密度为1.2g/mL)3mL,在密闭容器中加热,充分反应后,得到无色溶液A;将溶液A全部倾入水中,可得到白色的氯化亚铜沉淀.已知溶液A中只含氢离子和两种阴离子(不考虑水的电离),其中,n(H+)=0.036mol、n(Cl﹣)=0.032mol.请通过分析和计算,确定溶液A中另一阴离子的化学式和物质的量.(3)、由CO2、O2、CO、N2组成的混合气体1.008L,测得其密度为1.429g/L,将该气体依次通过足量的30%KOH溶液、氯化亚铜氨溶液(可完全吸收O2和CO)(假定每一步反应都能进行完全),使上述液体分别增加0.44g、0.44g(体积和密度均在标准状况下测定).该混合气体的摩尔质量是 g/mol;混合气体中n(CO2):n(CO和N2)= .
(4)、列式计算:①混合气体中CO的质量是多少?
②最后剩余气体的体积是多少?