四川省成都市师大一中2016-2017学年中考化学模拟试卷
试卷更新日期:2017-11-10 类型:中考模拟
一、选择题
-
1. 下列有关说法正确的是( )A、化学反应中原子不可再分 B、煤和石油属于可再生能源 C、催化剂只能加快化学反应的速率 D、铁、碘、钙是人体必需的微量元素2. 有关实验操作正确的是( )A、加热蒸发皿时垫上石棉网 B、将氢氧化钠固体放入烧杯中称量 C、在量筒中溶解氯化钠固体 D、将pH 试纸侵入待测液中测定pH3. 下列过程中涉及化学变化的是( )A、用聚乙烯塑料制得食品袋 B、用纯碱制得烧碱 C、将液态空气分离制得氧气 D、将石油分离制得汽油4. 根据生活经验和所学知识判断,下列课外实验不能成功的是( )A、用pH试纸检验酸牛奶是否变质 B、用肥皂水鉴别硬水和软水 C、用食醋除去暖水瓶中的水垢 D、用紫甘蓝和酒精溶液制酸碱指示剂5. 地壳中含有丰富的氧、硅、铝、铁元素,其有关信息如图所示,下列说法正确的是( )
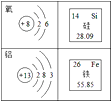 A、氧原子核内质子数为6 B、硅元素位于元素周期表中第三周期 C、铝离子(Al3+)核外有三个电子层 D、铁原子的质量为55.85g6. A,B,C三种物质的溶解度曲线如图5所示。下列分析正确的是( )
A、氧原子核内质子数为6 B、硅元素位于元素周期表中第三周期 C、铝离子(Al3+)核外有三个电子层 D、铁原子的质量为55.85g6. A,B,C三种物质的溶解度曲线如图5所示。下列分析正确的是( )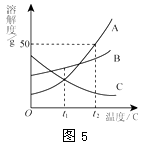 A、t1℃时,A,C两种物质的饱和溶液中溶质的质量相等 B、t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3 C、将t2℃时,A,B,C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A D、将C的饱和溶液变为不饱和溶液,可采用升温的方法7. 通过下列实验操作和现象能得出相应结论的是 ( )
A、t1℃时,A,C两种物质的饱和溶液中溶质的质量相等 B、t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3 C、将t2℃时,A,B,C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A D、将C的饱和溶液变为不饱和溶液,可采用升温的方法7. 通过下列实验操作和现象能得出相应结论的是 ( )实验操作 现象 结论 A 向收集满 CO2的软塑料瓶中加入约1/3 体积滴有石蕊试液的水,旋紧瓶盖,振荡 塑料瓶变瘪, 溶液变红 CO2能与石蕊反应 B 往久置于空气中的氢氧化钠溶液滴加稀硫酸 有气泡 氢氧化钠溶液已变质 C 在某无色溶液中滴加氯化钡溶液 有白色沉淀 无色溶液中一定含有
SO42-离子D 把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸 镁条与盐酸
产生气体更快镁的金厲活动性比锌强 A、A B、B C、C D、D8. 下列说法正确的是 ( )A、铁钉很快生锈 B、能用来检测空气中氧气的含量
B、能用来检测空气中氧气的含量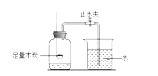 C、白磷燃烧.
C、白磷燃烧.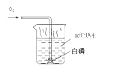 D、乙厂只排出硫酸钠
D、乙厂只排出硫酸钠 9. 将10g碳酸钙固体高温煅烧足够时间,冷却后投入足量稀盐酸中完全反应。有关结论错误的是( )A、共生成11.1克氯化钙 B、煅烧越充分则消耗的盐酸量越少 C、共生成4.4克二氧化碳 D、燃烧后固体中氧元素的质量分数减小10. 常温下,下列各组物质中,X既能与Y反应又能与Z反应的是( )
9. 将10g碳酸钙固体高温煅烧足够时间,冷却后投入足量稀盐酸中完全反应。有关结论错误的是( )A、共生成11.1克氯化钙 B、煅烧越充分则消耗的盐酸量越少 C、共生成4.4克二氧化碳 D、燃烧后固体中氧元素的质量分数减小10. 常温下,下列各组物质中,X既能与Y反应又能与Z反应的是( )X Y Z ① CO2 Ca(OH) 2溶液 H2O ② H2 O2 CuO ③ Ba(NO3) 2溶液 稀硫酸 Na2CO3溶液 ④ Fe2O3 CO 稀盐酸 A、①② B、①③ C、①③④ D、①②③④11. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )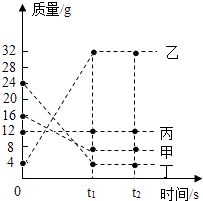 A、该反应为化合反应 B、丙可能为该反应的催化剂 C、该反应中,乙、丁的质量变化之比为7:5 D、该反应中,甲、乙的质量变化之比为1:412. 如图所示,加热烧瓶中的水使之沸腾.水蒸气从铜管喷出,把火柴靠近管口P处,火柴被加热,迅速移开火柴,火柴开始燃烧.下列说法正确的是( )
A、该反应为化合反应 B、丙可能为该反应的催化剂 C、该反应中,乙、丁的质量变化之比为7:5 D、该反应中,甲、乙的质量变化之比为1:412. 如图所示,加热烧瓶中的水使之沸腾.水蒸气从铜管喷出,把火柴靠近管口P处,火柴被加热,迅速移开火柴,火柴开始燃烧.下列说法正确的是( )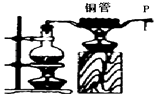 A、水沸腾,水分子质量和体积增大 B、P处水蒸气的作用是提高火柴的着火点,使其燃烧 C、火柴移离水蒸气,与氧气充分接触,从而燃烧 D、水变为水蒸气质量不变符合质量守恒定律13. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。对该实验的分析正确的是( )
A、水沸腾,水分子质量和体积增大 B、P处水蒸气的作用是提高火柴的着火点,使其燃烧 C、火柴移离水蒸气,与氧气充分接触,从而燃烧 D、水变为水蒸气质量不变符合质量守恒定律13. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。对该实验的分析正确的是( )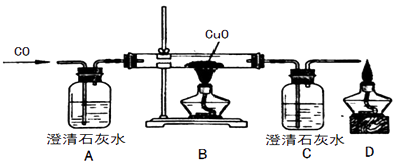 A、实验结束时应先熄灭D处酒精灯 B、C中增加的质量与B中固体减少的质量相等 C、反应开始后通入2.8g一氧化碳可生成6.4g铜 D、省略A装置仍可证明一氧化碳不能和石灰水反应,因为为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳,未见装置C变浑浊
A、实验结束时应先熄灭D处酒精灯 B、C中增加的质量与B中固体减少的质量相等 C、反应开始后通入2.8g一氧化碳可生成6.4g铜 D、省略A装置仍可证明一氧化碳不能和石灰水反应,因为为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳,未见装置C变浑浊二、填空题
-
14. 空气是一种宝贵的资源。(1)、洁净的空气属于 (填“混合物”或“纯净物”)(2)、据报道,今年1~4月南京空气中PM2.5与去年同期相比下降22.3%,下列行为不会增加空气中PM2.5的是 。A、燃煤火力发电 B、治理工地扬尘 C、露天焚烧垃圾 D、使用氢能源汽车(3)、氢气具有广泛用途,它是制造硝酸和氮肥的重要原料。写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价。
氧化物、酸、碱、盐。
15. 某方便面的营养成分表如下(其中碳水化合物主要指淀粉等): (1)、表中“钠”是指 _(填序号).A、离子 B、分子 C、元素 D、单质(2)、方便面中含的营养素分别为、、、 .(3)、方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是_.(4)、中国居民膳食指南建议每天食用食盐不超过6克.假设小明某天吃了100克该方便面,相当于吃了食盐克(保留小数点后一位).
(1)、表中“钠”是指 _(填序号).A、离子 B、分子 C、元素 D、单质(2)、方便面中含的营养素分别为、、、 .(3)、方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是_.(4)、中国居民膳食指南建议每天食用食盐不超过6克.假设小明某天吃了100克该方便面,相当于吃了食盐克(保留小数点后一位).三、实验探究题
-
16. 浩瀚的大海里蕴藏着丰富的资源,开发海水资源前景广阔,探究学习小组以含有Ca2+ , Mg2+ , Cl﹣离子的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2 , 流程如图1:
请回答下列问题: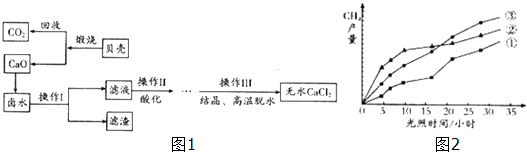 (1)、操作Ⅰ中用到的玻璃仪器有烧杯、玻璃棒、(2)、以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式 .(3)、操作Ⅱ酸化时应选择的酸是_(填写化学式).(4)、上述反应中未涉及的基本反应类型是(填写字母标号)
(1)、操作Ⅰ中用到的玻璃仪器有烧杯、玻璃棒、(2)、以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式 .(3)、操作Ⅱ酸化时应选择的酸是_(填写化学式).(4)、上述反应中未涉及的基本反应类型是(填写字母标号)a.复分解反应 b.置换反应 c.化合反应 d.分解反应
(5)、回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成CH4和O2 , 该反应的化学方程式为 , 紫外线照射时,在不同催化剂(①、②、③)的作用下,CH4产量随光照时间的变化如图2所示,在第10小时时CH4产量最高是 (填写“①”、“②”、或“③”).(6)、已知T℃时四种化合物在水中和液氨中的溶解度如下表: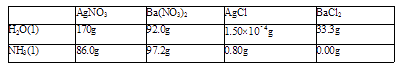
上述四种物质能在液氨中发生复分解反应的化学方程式为 .
17. 探究学习小组在实验室中用图1所示装置制取CO2并探究CO2与过氧化钠(Na2O2)的反应.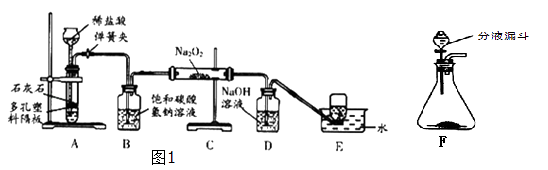
查阅资料得知:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2 , H2O发生反应:Na2O2+2CO2═2Na2CO3+O2 , 2Na2O2+H2O═4NaOH+O2↑
请回答下列问题:(1)、装置A中发生反应的化学方程式为 , 利用装置A制取CO2的优点是 .(2)、装置B的作用是吸收CO2中混有的HCl,发生反应化学方程式为(3)、装置D的作用是 .(4)、装置E中收集到的气体是(填化学式),该气体还可以用下列图2装置中的进行收集(填写字母序号). (5)、为探究反应后装置C硬质玻璃管中固体的成分,该小组同学进行了如图3实验:
(5)、为探究反应后装置C硬质玻璃管中固体的成分,该小组同学进行了如图3实验: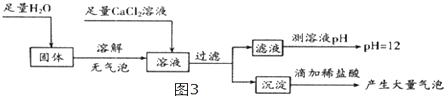
根据固体加水溶解无气泡,得_结论,加入足量氯化钙目的为 , 根据判断,反应后装置C硬质玻璃管中固体为 .
(6)、①在实验室制取二氧化碳的研究中,探究学习小组又进行了如下实验:药品编号
甲
乙
丙
丁
大理石
m g,块状
m g,块状
m g,粉末状
m g,粉末状
盐酸(过量)
w g,稀盐酸
w g,浓盐酸
w g,稀盐酸
w g,浓盐酸
I.若要研究盐酸浓度大小对反应的影响,可选择实验甲与对照(选填实验编号)。
II..除盐酸的浓度外,上述实验研究的另一个影响反应的因素是。
III.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高
②下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳地产生。请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因。
目的
原料
发生装置
气体较平稳产生的
最主要的一个原因
制取二氧化碳
块状大理石稀盐酸
A
制取氧气
粉末状二氧化碳3%的过氧化氢溶液
F
四、计算题
-
18. 某化学兴趣小组的同学在实验室配制溶质质量分数为7.3%的稀盐酸,并用其测定某氢氧化钠溶液溶质的质量分数.下图表示用上述配制的稀盐酸与20g某氢氧化钠溶液发生反应过程中,使用数字传感仪测得溶液温度变化的曲线.
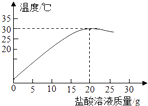 (1)、当加入25g盐酸溶液时,所得溶液中的溶质有:。(2)、试列式计算:某氢氧化钠溶液的溶质质量分数 .
(1)、当加入25g盐酸溶液时,所得溶液中的溶质有:。(2)、试列式计算:某氢氧化钠溶液的溶质质量分数 .