江苏省苏州常熟市2016-2017学年九年级下学期化学4月调研测试(一模)考试试卷
试卷更新日期:2017-11-08 类型:中考模拟
一、选择题
-
1. 下列说法都能体现物质物理性质的是( )A、镁粉用作照明弹;铜丝用作导线 B、二氧化碳用作碳酸饮料;金刚石刻划玻璃 C、氢气用作清洁燃料;稀盐酸除铁锈 D、活性炭除去冰箱内的异味;干冰进行人工降雨
-
2. 以下各类物质中一定含有氢元素的是( )
①酸 ②碱 ③盐 ④氧化物
A、①② B、①②③ C、①②④ D、①②③④ -
3. 下列物质间的转化,在一定条件下均能一步实现的是
①C→CO→CO2 ②Cu→CuO→CuSO4
③CaCO3→CaO→Ca(OH)2 ④Na2CO3→NaCl→NaNO3( )
A、①②④ B、①②③ C、①③④ D、①②③④ -
4. 将一定质量的氯酸钾与二氧化锰混合加热,变量y随加热时间的变化趋势如图,则变量y可表示的是( )
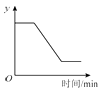 A、生成 的质量 B、固体中氧元素的质量 C、固体中 的质量分数 D、固体中钾元素的质量分数
A、生成 的质量 B、固体中氧元素的质量 C、固体中 的质量分数 D、固体中钾元素的质量分数 -
5. 每年的6月5号是“世界环境日”。 校园开展的下列活动与保护环境的主题不相符的是( )A、栽花护绿, 与植物交朋友 B、布袋购物,减少“白色污染” C、焚烧垃圾,净化校园环境 D、不燃放烟花爆竹,低碳欢庆佳节
-
6. 下列变化中属于化学变化的是( )A、冰川融化 B、钢铁生锈 C、汽油挥发 D、海水晒盐
-
7. 下列各物质的名称、俗名、化学式表示同一物质的是( )A、乙醇 酒精 C2H4O2 B、碳酸铵 碳铵 ( NH4)2CO3 C、氧化钙 熟石灰 CaO D、碳酸氢钠 小苏打 NaHCO3
-
8. 水与人们的生产生活息息相关,下列有关水的说法正确的是( )A、明矾净水的作用是消毒杀菌 B、可用肥皂水区分硬水和软水 C、水的电解实验说明水是由氢气和氧气组成的 D、氯化钠溶于水后生成大量自由移动的氯化钠离子使水溶液能够导电
-
9. 下列实验操作正确的是( )A、
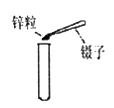 向试管中加锌粒
B、
向试管中加锌粒
B、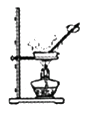 蒸发
C、
蒸发
C、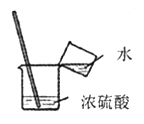 稀释
D、
稀释
D、 氧气验满
氧气验满
-
10. 下列物质中氮元素的化合价最高的是( )A、N2 B、NO C、NO2 D、N2O
-
11. 下列属于复合材料的是( )A、陶瓷 B、不锈钢 C、塑料 D、玻璃钢
-
12. 下列叙述中,错误的是( )A、食物的腐败、金属的生锈都是氧化反应 B、工业上用分离液态空气的方法制取氧气是分解反应 C、动植物的呼吸作用也是地球上产生二氧化碳的原因之一 D、干燥空气中各组分气体体积分数约为:氮气78%,氧气21%,其他气体和杂质1%
-
13. 下列说法不妥当的是( )A、洗洁精能洗碗,是因为洗洁精可溶解油污 B、磷可用于制作烟幕弹,是因为磷燃烧能产生大量白烟 C、氮气可用于食品包装袋内防腐,是因为氮气化学性质不活泼 D、可用灼烧的方法区分羊毛和棉线,是因为羊毛灼烧后有烧焦羽毛气味
-
14. 下列有关燃烧叙述正确的是( )A、家用电器着火直接用水浇灭 B、用水来灭火的原理是降低可燃物的着火点 C、只要满足燃烧的三个条件,物质在水中也可以燃烧 D、用嘴吹灭蜡烛的火焰,是因为使蜡烛火焰隔绝了氧气
-
15. 下列气体中,既能用浓硫酸干燥,也可以用氢氧化钠干燥的是( )A、CO2 B、CO C、SO2 D、NH3
-
16. 向CuCl2溶液中加入一定量铁粉,充分反应后过滤。向滤渣中加入足量稀盐酸,滤渣部分溶解,有无色气体产生。根据上述实验作出的下列推断不正确的是( )
A、滤液中不含Cu 2+ B、金属活动性:Fe>Cu C、滤渣含有铁和铜 D、滤液质量比原溶液质量大 -
17. 甲、乙两物质发生反应的微观示意图如下,则说法正确的是( )
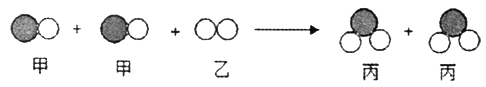 A、该反应属于化合反应 B、该反应前后分子个数保持不变 C、甲和丙中同种元素的化合价均相等 D、甲和乙的相对分子质量之和等于丙的相对分子质量
A、该反应属于化合反应 B、该反应前后分子个数保持不变 C、甲和丙中同种元素的化合价均相等 D、甲和乙的相对分子质量之和等于丙的相对分子质量 -
18. 马铃薯富含淀粉、蛋白质、维生素C、磷、钙等。下列说法错误的是( )A、钙元素可以预防佝偻病 B、蛋白质、淀粉属于有机高分子 C、维生素C可以预防坏血病 D、可用加碘食盐检验马铃薯中的淀粉
-
19. 抗癌新药西达本胺的化学式为C22H19FN4O2 , 下列关于西达本胺的说法中正确的是( )A、西达本胺有48个原子 B、西达本胺是一种有机化合物 C、西达本胺中氧元素的质量分数最小 D、西达本胺中碳元素和氢元素的质量比为22:19
-
20. 下列各组离子在指定溶液中能大量共存的是( )A、在氢氧化钠溶液中:H+、Cl- B、在稀盐酸中:K+、CO32- C、在硝酸铜溶液中:Na+、SO42- D、在碳酸氢铵溶液中:Na+、OH-
-
21. 下列说法正确的是( )A、熟石灰可以改良酸性土壤 B、生铁可以完全溶解在足量的稀盐酸中 C、铵态氮肥和草木灰一起使用会使肥效更高 D、打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,瓶口都有白雾
-
22. 鉴别下列各组物质方案不正确的是( )A、食盐水与稀盐酸:pH试纸 B、氢氧化钙固体与硝酸铵固体:水 C、二氧化碳和二氧化硫:高锰酸钾溶液 D、碳酸钠溶液和氢氧化钠溶液:酚酞试液
-
23. 除去下列物质中的少量杂质,所选试剂及操作都比较合理的是( )
序号
物质
杂质
试剂
操作
A
FeCl2溶液
CuCl2
过量铁粉
结晶
B
CO2
CO
生石灰
洗气
C
NaNO3溶液
Na2CO3
适量CaCl2溶液
过滤
D
铜粉
铁粉
过量盐酸
过滤
A、A B、B C、C D、D -
24. 下图为甲、乙两物质的溶解度皮曲线。下列说法正确的是( )
 A、t2℃时,甲物质的溶液中溶质质量分数为33.3% B、t2℃时,100g甲物质饱和溶液中含溶质50g C、将t2℃甲物质的饱和溶液降温至t1℃,会析出晶体 D、将t1℃乙物质的不饱和溶液升高温度至t2℃ ,该溶液变为饱和溶液
A、t2℃时,甲物质的溶液中溶质质量分数为33.3% B、t2℃时,100g甲物质饱和溶液中含溶质50g C、将t2℃甲物质的饱和溶液降温至t1℃,会析出晶体 D、将t1℃乙物质的不饱和溶液升高温度至t2℃ ,该溶液变为饱和溶液
二、信息分析题
-
25. 我们的生活离不开化学。现有①食醋②小苏打③生石灰④天然气⑤硝酸钾,选择适当物质的序号填空:(1)、常用于烘培糕点的是;(2)、属于化石燃料的是;(3)、能去除水壶里水垢的是;(4)、可作为某些食品干燥剂的是。
-
26. 写出下列反应的化学方程式,并回答问题。(1)、光合作用制取氧气 , 该反应将光能转化为能。(2)、工业上用赤铁矿在高温下炼铁, 该反应中还原剂是。(3)、硫酸铵与熟石灰研磨 , 反应生成的气体可用湿润的检验。(4)、用氨水中和工业废水中含有的稀硫酸 , 该反应属于反应(填基本反应类型)。
-
27. 下图表示某些物质间转化关系。其中A,D是由相同元素组成的固体,且A为紫黑色,C为黑色粉末,B、E为常见气体;X与F是由相同元素组成的无色液体,且X具有消毒杀菌作用;Y是一种红色金属。请回答下列问题:
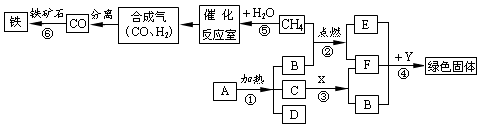 (1)、A的化学式是;(2)、C物质在反应③中的作用;(3)、写出反应②、④、⑥的化学方程式:
(1)、A的化学式是;(2)、C物质在反应③中的作用;(3)、写出反应②、④、⑥的化学方程式:②;④;⑥;
(4)、若将合成气中两气体按分子数之比为1:1进行化合(原子利用率为100%),可合成多种有机化工产品,写出其中一种可能产品的化学式。 -
28. 下列为实验室常用的实验装置,回答问题:
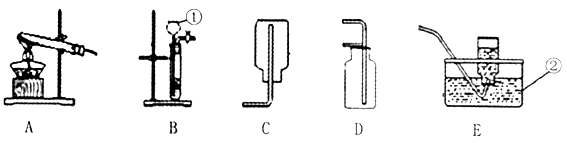 (1)、写出带有标号仪器的名称:①;②。(2)、用锌和稀硫酸制取氢气,应选用的发生装置是(填序号,下同) ,收集装置是。(3)、实验室常用稀盐酸和石灰石反应制CO2 , 该反应的化学方程式;
(1)、写出带有标号仪器的名称:①;②。(2)、用锌和稀硫酸制取氢气,应选用的发生装置是(填序号,下同) ,收集装置是。(3)、实验室常用稀盐酸和石灰石反应制CO2 , 该反应的化学方程式;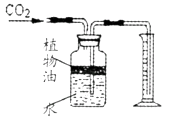 (4)、上图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是 , 植物油上方原有的空气对实验结果(填“有”或“无”)明显影响。
(4)、上图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是 , 植物油上方原有的空气对实验结果(填“有”或“无”)明显影响。
三、探究题
-
29. 小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如题图:
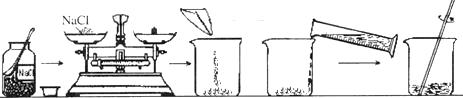 (1)、小华同学应称取氯化钠的质量是(2)、指出图中的一处错误:(3)、在用托盘天平称取食盐的过程中,发现指针已偏向分度盘左侧,他接下来的操作是(4)、在用量筒量取水的过程巾,当液面接近刻度线时,他的操作如题图所示,其中规范的是(填序号)。
(1)、小华同学应称取氯化钠的质量是(2)、指出图中的一处错误:(3)、在用托盘天平称取食盐的过程中,发现指针已偏向分度盘左侧,他接下来的操作是(4)、在用量筒量取水的过程巾,当液面接近刻度线时,他的操作如题图所示,其中规范的是(填序号)。 (5)、如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有 (填序号)。A、称量前天平没有调平 B、称量纸上残留少量食盐 C、向烧杯中加水时,有少量水溅出烧杯外
(5)、如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有 (填序号)。A、称量前天平没有调平 B、称量纸上残留少量食盐 C、向烧杯中加水时,有少量水溅出烧杯外 -
30. 某校化学兴趣小组参观制碱厂后,获得以下信息井对相关问题进行研究。
【查阅资料】
①无水硫酸铜是白色固体,吸水变蓝。
②生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质。
③生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是NH4Cl=NH3↑+HCl↑。
⑤部分生产流程如下图所示:
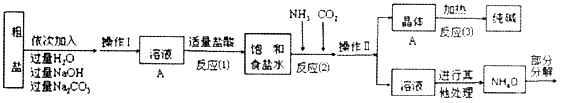
【问题讨论】
(1)、①溶液A中的溶质有NaCl和、。②操作Ⅱ的名称为。
③写出加入NaOH溶液所发生反应的化学方程式。
④流程中Na2CO3溶液的作用是除去粗盐中的。
(2)、上述生产流程中可循环使用的是 (填序号)。A、NH3 B、NaOH C、HCl D、CO2(3)、【组成探究】①晶体A受热分解的化学方程式为 。
②设计实验检验纯碱样品中是否混有晶体A,请完成下表(从下列装置中选择):
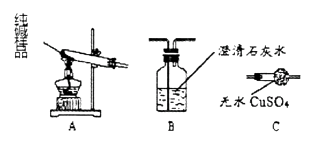
选择的装置
实验现象
实验结论
样品不含晶体A
(4)、【组成探究二】取纯碱样品加水溶解,向该溶液中加入过量稀HNO3 , 再滴加AgNO3溶液,有白色沉淀。产生沉淀的方程式为 , 由此确定纯碱样品含有杂质NaCl。
(5)、【组成探究三】同学们为了测定该纯碱样品的纯度,设计了如下实验:

①氯化钡溶液过量的目的是。
②判断滤渣是否洗干净,可向最后的洗出液中滴加 , 然后观察现象判断。
A.氯化钡溶液 B.稀硫酸 C.稀盐酸 D.碳酸钾溶液
③根据实验数据,计算样品中碳酸钠的质量分数为。(精确到0. 1 % )
四、简答题
-
31. 酸与碱发生中和反应,其实质是酸溶液中大量自由移动的H+和碱溶液中大量自由移动的OH-结合生成水分子的过程。请根据以下稀盐酸与稀氢氧化钠溶液反应的实验,回答问题。(1)、【实验一】用酚酞试液
向一试管中倒入约2mL稀氢氧化钠溶液,滴加3滴酚酞试液,振荡,再逐滴滴入稀盐酸,边滴边振荡,直至溶液刚好变为色为止,说明它们之间发生了中和反应。
(2)、【实验二】用温度计向一烧杯中加入一定量的稀氢氧化钠济液,再逐滴匀速加入稀盐酸,并用数字化仪器对反应过程中溶液的温度实时测定,得到的曲线如图-1。
①约0 - 50s温度上升是因为中和反应放热,50s后溶液温度下降的原因是。
②不能用氢氧化钠固体与稀盐酸反应测定中和反应放热的原因是。
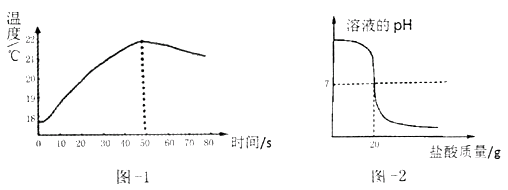 (3)、【实验三】用pH计
(3)、【实验三】用pH计向一锥形瓶中加入20g质量分数为4. 00%的稀氢氧化钠溶液,再逐滴匀速加入一定质量分数的稀盐酸,并用数字化仪器对反应过程中溶液的pH测定,得到的曲线如图 - 2。列式计算:
①所取稀盐酸的质量分数为多少?(精确到0.01%,下同)
②当恰好完全反应时所得溶液的溶质质量分数为多少?
