江苏省江阴市长泾片2016-2017学年九年级下学期化学第一次模拟(期中)考试化学试卷
试卷更新日期:2017-11-08 类型:中考模拟
一、选择题
-
1. 制备氮化镁(MgF2)时有如下反应:X + 6HF = H2SiF6 + 2H2O,则X的化学式为( )A、SiF4 B、SiH4 C、SiHF3 D、SiO22. 下列实验现象描述正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰 B、硝酸铵溶于水时溶液温度升高 C、浓盐酸打开瓶盖,瓶口有白雾出现 D、氯化铵加熟石灰研磨有氨气产生3. 下列各组物质投入水中.搅拌后能得到无色、澄清溶液的是( )A、KNO3、HCl、CuCl2 B、Ba(OH)2、BaCl2、、Na2SO4 C、Na2CO3、NaCl、Ca(OH)2 D、NaOH、KCl、H2SO44. 某工厂排放的废水中含有AgNO3和Cu(NO3)2 , 为防止水体污染,现往废水中加入一定量的铁粉,充分反应后,过滤,往滤液中滴几滴稀盐酸,有白色沉淀生成,则下列说法正确的是( )A、滤渣中一定含有铁、银、铜 B、滤渣中一定含有银,可能含有铜 C、滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜 D、滤液中一定含有硝酸亚铁、硝酸银、硝酸铜。5. “低碳”生活是一种环保的生活理念,下列不符合“低碳”理念的是( )A、开发利用新能源 B、草稿纸使用时要两面都用 C、使用一次性木筷 D、选择自行车作为出行工具6. 下列变化属于化学变化的是( )A、蔗糖溶解 B、滴水成冰 C、粮食酿酒 D、花香四溢7. 下列物质中,属于纯净物的是( )A、粗盐 B、空气 C、铁矿石 D、液氧8. 下列实验操作正确的是( )A、读出液体体积
 B、稀释浓硫酸
B、稀释浓硫酸  C、点燃酒精灯
C、点燃酒精灯  D、检查装置气密性
D、检查装置气密性  9. 元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是
9. 元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是 ( )A、属于非金属元素 B、原子序数为50 C、相对原子质量是118.7g D、原子核内中子数为5010. 根据你的经验,下列家庭小实验能成功的是( )A、用加热的方法修补电木等热固性塑料 B、用食盐水除去水瓶中的水垢 C、用实验室里的柠檬酸和小苏打等自制汽水并饮用 D、用小卵石、石英砂、活性炭等制作家庭简易净水器11. 豆浆被称为“植物奶”,其中的异黄酮(C15H10O2)具有防癌功能,下列说法正确的是( )A、异黄酮是氧化物 B、异黄酮中碳元素质量分数最大 C、异黄酮中C、H、O三种元素的质量比为15:10:2 D、异黄酮由15个碳原子,10个氢原子和2个氧原子构成12. 下图为甲乙两物质的溶解度曲线,下列说法正确的是( )
( )A、属于非金属元素 B、原子序数为50 C、相对原子质量是118.7g D、原子核内中子数为5010. 根据你的经验,下列家庭小实验能成功的是( )A、用加热的方法修补电木等热固性塑料 B、用食盐水除去水瓶中的水垢 C、用实验室里的柠檬酸和小苏打等自制汽水并饮用 D、用小卵石、石英砂、活性炭等制作家庭简易净水器11. 豆浆被称为“植物奶”,其中的异黄酮(C15H10O2)具有防癌功能,下列说法正确的是( )A、异黄酮是氧化物 B、异黄酮中碳元素质量分数最大 C、异黄酮中C、H、O三种元素的质量比为15:10:2 D、异黄酮由15个碳原子,10个氢原子和2个氧原子构成12. 下图为甲乙两物质的溶解度曲线,下列说法正确的是( ) A、甲的溶解度大于乙的溶解度 B、t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15% C、要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法 D、t2℃时,将50g甲物质放入100g水中,得到溶液的质量为150g13. 下列对部分化学知识的归纳完全正确的一组是( )
A、甲的溶解度大于乙的溶解度 B、t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15% C、要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法 D、t2℃时,将50g甲物质放入100g水中,得到溶液的质量为150g13. 下列对部分化学知识的归纳完全正确的一组是( )A.化学与生活
B.化学与环境
①生活中常用加热煮沸的方法软化硬水②用燃烧的方法区分羊毛和涤纶
③利用洗洁精的乳化作用去除油污
①焚烧植物秸秆不会造成空气污染
②PM2.5是造成雾霾天气的原因之一
③含磷洗涤剂的使用会导致水污染
C.化学与安全
D.化学与健康
①炒菜油锅着火可以用锅盖盖灭
②在室内放一盆水,可防止煤气中毒
③夜间发现液化气泄漏开灯寻找泄漏源
①人体缺铁会引起贫血
②用甲醛的水溶液浸泡海产品保鲜
③食用蔬菜和水果来补充维生素
A、A B、B C、C D、D14. 下列实验方案中,不可行的是( )A、除去粗盐中的泥沙,采用溶解、过滤、蒸发的步骤 B、用MnO2来区分水和过氧化氢溶液 C、用稀盐酸除去铁粉中混有的少量铜粉 D、用Ca(OH)2溶液检验露置在空气中的NaOH溶液是否变质15. 下列4个坐标图分别表示4个实验过程中的某些变化,其中正确的是( )A、向含有稀硫酸的硫酸铜溶液中加氢氧化钠溶液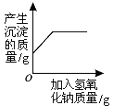 B、向一定量的稀盐酸中加入铁粉
B、向一定量的稀盐酸中加入铁粉  C、稀释pH =2的稀硫酸
C、稀释pH =2的稀硫酸  D、氢氧化钠溶液中滴加盐酸
D、氢氧化钠溶液中滴加盐酸 
二、信息分析题
-
16. 化学就在我们身边,请用所学的化学知识填空。(1)、从H、O、C、Cl、Ca五种元素中,选择适当的元素组成符合下列要求的物质,并用化学式填空(每空只填一种物质)。
①相对分子质量最小的氧化物是;②农业上用来降低土壤酸性的是;
③可用于金属表面除锈的是;④厨房用的酸性调味品是。
(2)、如图为普通电池(锌锰电池)示意图。
①碳棒可用作干电池的电极,说明石墨具有性。
②氯化锌中阴离子的符号是。
③将回收的废旧电池进行分离可以得到二氧化锰,二氧化锰中锰元素的化合价是。实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰起作用。
17. 铝在空气中能与氧气反应生成一层致密的氧化铝(Al2O3 )薄膜,该反应的化学方程式为 , 反应的基本类型是。将打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为。三、探究题
-
18. 请结合下列实验常用装置,回答有关问题。
 (1)、写出图中标有字母的仪器的名称:a。(2)、若用A装置制氧气,其反应的化学方程式为 , 在制取氧气时试管中的棉花没有发生燃烧,根据燃烧的条件分析,其主要原因是。(3)、若要制取二氧化碳,应选用的发生装置是(填“A”或“B”)。其化学方程式为 。若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放(填写试剂名称)。(4)、实验室常使用仪器E来收集气体,如现在要收集氢气,则气体从端进入(填“b”或“c”),有同学认为只要经过一定的改进措施,氧气也能从该端进入收集,则他的改进措施是。(5)、实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置,当反应进行过程中,关闭该装置中的止水夹后,可以观察到的现象是。19. 漂白粉的主要成分为次氯酸钙 [Ca(ClO)2] 和氯化钙,即可用作漂白剂,又可用作消毒剂。漂白粉中有效成分是 [Ca(ClO)2] ,漂白的原理是:Ca(ClO)2在空气中发生反应。Ca(ClO)2+ CO2+ H2O=CaCO3↓+ 2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色。(1)、HClO在常温下分解,反应为2HClO=2HCl+ O2↑。某瓶HClO溶液放置一段时间后,溶液的pH (填“增大”或“减小”或“不变”)。(2)、在漂白粉中滴加盐酸,能加快漂白的速率。写出漂白粉中加入盐酸反应的化学方程式。(3)、有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验。
(1)、写出图中标有字母的仪器的名称:a。(2)、若用A装置制氧气,其反应的化学方程式为 , 在制取氧气时试管中的棉花没有发生燃烧,根据燃烧的条件分析,其主要原因是。(3)、若要制取二氧化碳,应选用的发生装置是(填“A”或“B”)。其化学方程式为 。若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放(填写试剂名称)。(4)、实验室常使用仪器E来收集气体,如现在要收集氢气,则气体从端进入(填“b”或“c”),有同学认为只要经过一定的改进措施,氧气也能从该端进入收集,则他的改进措施是。(5)、实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置,当反应进行过程中,关闭该装置中的止水夹后,可以观察到的现象是。19. 漂白粉的主要成分为次氯酸钙 [Ca(ClO)2] 和氯化钙,即可用作漂白剂,又可用作消毒剂。漂白粉中有效成分是 [Ca(ClO)2] ,漂白的原理是:Ca(ClO)2在空气中发生反应。Ca(ClO)2+ CO2+ H2O=CaCO3↓+ 2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色。(1)、HClO在常温下分解,反应为2HClO=2HCl+ O2↑。某瓶HClO溶液放置一段时间后,溶液的pH (填“增大”或“减小”或“不变”)。(2)、在漂白粉中滴加盐酸,能加快漂白的速率。写出漂白粉中加入盐酸反应的化学方程式。(3)、有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验。【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
(4)、【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞。实验操作
实验现象
实验结论
①取少量样品于试管中,。
有气体产生,气体使石灰水变浑浊。
猜想2成立
②在上述反应后试管中加少量。
。
(5)、现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如下实验方案:
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
m= .
(6)、上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?.(不考虑过滤中的损失,计算结果保留到小数点后一位.)。20. 木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学实验小组设计回收铜的方案如下: (1)、过滤操作中必须用到的玻璃仪器有烧杯、漏斗和。(2)、反应①的化学方程式为。(3)、滤液Ⅰ中的溶质为。(4)、试剂A最好选用下列溶液(填序号)。
(1)、过滤操作中必须用到的玻璃仪器有烧杯、漏斗和。(2)、反应①的化学方程式为。(3)、滤液Ⅰ中的溶质为。(4)、试剂A最好选用下列溶液(填序号)。①H2SO4 ②CuSO4 ③MgSO4
(5)、为了完善实验方案,可对滤渣Ⅰ中的进行回收。