江苏省盐城市大丰区2016-2017学年九年级化学第二次质量检测(二模)考试试卷
试卷更新日期:2017-11-07 类型:中考模拟
一、选择题
-
1. 在我们的日常生活中涉及到许多变化,下列变化中不包含化学变化的是( )A、用石灰浆涂抹墙壁后,表面有水珠生成 B、在口中咀嚼米饭或馒头时感到有甜味 C、用干冰做制冷剂进行人工降雨 D、使用煤气作燃料烧饭做菜2. 我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是( )A、分子 B、原子 C、离子 D、中子3. 在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )A、用量筒量取水时俯视读数 B、用来配制溶液的烧杯刚用少量蒸馏水润洗过 C、用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码 D、用了含少量杂质的蔗糖配制溶液4. 下列有关物质分类或归类正确的是( )A、氧化物:生石灰和熟石灰 B、复合肥:硝酸钾和碳酸钾 C、硬水:蒸馏水和矿泉水 D、碳单质:金刚石和石墨5. 下列关于四种粒子的结构示意图的说法中正确的是( )
 A、①③是不同种元素 B、②表示的元素在化合物中通常显+1价 C、②③的化学性质相似 D、①④表示的是离子6. 下列对课本中相关实验的分析不正确的是( )A、电解水实验得到氢气和氧气能说明水是由氢、氧两种元素组成的化合物 B、氢氧化钠与硫酸铜溶液反应前后质量测定实验能说明化学变化遵循质量守恒定律 C、黄豆与芝麻混合的实验能说明分子之间有空隙 D、二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气7. 如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )
A、①③是不同种元素 B、②表示的元素在化合物中通常显+1价 C、②③的化学性质相似 D、①④表示的是离子6. 下列对课本中相关实验的分析不正确的是( )A、电解水实验得到氢气和氧气能说明水是由氢、氧两种元素组成的化合物 B、氢氧化钠与硫酸铜溶液反应前后质量测定实验能说明化学变化遵循质量守恒定律 C、黄豆与芝麻混合的实验能说明分子之间有空隙 D、二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气7. 如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( ) A、S、P在氧气中燃烧均会产生大量白烟 B、Ⅰ、Ⅱ两类反应均体现了氧气的可燃性 C、Fe在Ⅰ、Ⅱ两类反应中的产物不相同 D、Ⅰ类反应放出热量,Ⅱ类反应吸收热量8. 下列有关生产、环保、能源、资源问题的叙述错误的是( )A、PM2.5专用口罩中使用了活性炭,是利用活性炭的吸附性 B、温室效应主要是由二氧化碳等气体引起的 C、煤、石油、天然气属于混合物,是不可再生能源 D、pH<7的雨水说明空气已受到污染9. 科学实验必须按规范进行操作,下列实验操作中规范的是( )A、取少量氯化钠
A、S、P在氧气中燃烧均会产生大量白烟 B、Ⅰ、Ⅱ两类反应均体现了氧气的可燃性 C、Fe在Ⅰ、Ⅱ两类反应中的产物不相同 D、Ⅰ类反应放出热量,Ⅱ类反应吸收热量8. 下列有关生产、环保、能源、资源问题的叙述错误的是( )A、PM2.5专用口罩中使用了活性炭,是利用活性炭的吸附性 B、温室效应主要是由二氧化碳等气体引起的 C、煤、石油、天然气属于混合物,是不可再生能源 D、pH<7的雨水说明空气已受到污染9. 科学实验必须按规范进行操作,下列实验操作中规范的是( )A、取少量氯化钠 B、闻药品气味
B、闻药品气味 C、滴加液体
C、滴加液体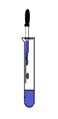 D、稀释浓硫酸
D、稀释浓硫酸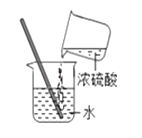 10. 盐场晒盐后所得的卤水中含有MgCl2 , KCl和MgSO4等物质,它们的溶解度曲线如图所示,下列说法正确的是( )
10. 盐场晒盐后所得的卤水中含有MgCl2 , KCl和MgSO4等物质,它们的溶解度曲线如图所示,下列说法正确的是( ) A、t1℃时,KCl和MgSO4两饱和溶液所含溶质质量一定相等 B、t2℃时,MgSO4的饱和溶液升高温度和降低温度都能析出晶体 C、t3℃时,100gMgCl2的饱和溶液中含有agMgCl2 D、将t3℃时的KCl溶液降温到t1℃,溶液的溶质质量分数变小11. 下列各组离子能在指定溶液中大量共存的一组是( )A、在稀盐酸中:Ag+、NO3﹣ B、在硫酸钠溶液中:Ba2+、Cl﹣ C、在硝酸钠溶液中:Zn2+、SO42﹣ D、在碳酸氢铵溶液中:K+、OH﹣12. 除去下列各物质中混有的少量杂质,所用试剂和操作均正确的是( )
A、t1℃时,KCl和MgSO4两饱和溶液所含溶质质量一定相等 B、t2℃时,MgSO4的饱和溶液升高温度和降低温度都能析出晶体 C、t3℃时,100gMgCl2的饱和溶液中含有agMgCl2 D、将t3℃时的KCl溶液降温到t1℃,溶液的溶质质量分数变小11. 下列各组离子能在指定溶液中大量共存的一组是( )A、在稀盐酸中:Ag+、NO3﹣ B、在硫酸钠溶液中:Ba2+、Cl﹣ C、在硝酸钠溶液中:Zn2+、SO42﹣ D、在碳酸氢铵溶液中:K+、OH﹣12. 除去下列各物质中混有的少量杂质,所用试剂和操作均正确的是( )序号
物质
杂质
所用试剂和操作方法
A
CaCO3
CaO
高温充分煅烧
B
H2
HCl
依次通过足量的NaOH溶液、浓硫酸
C
NaCl固体
细沙
加足量的水溶解、过滤
D
铁粉
Fe2O3
加入适量的稀盐酸,过滤、洗涤、干燥
A、A B、B C、C D、D13. 下列各组物质的鉴别方法中正确的是( )A、用燃着的木条鉴别O2、CO2、N2三种气体 B、用水鉴别CuSO4、NaOH、NH4NO3三种固体 C、用灼烧的方法鉴别木炭粉、CuO、Fe3O4三种黑色粉末 D、用pH试纸一次性鉴别H2SO4、C2H5OH、NaCl三种溶液14. 甲和乙可以合成清洁燃料丙,微观过程如图。下列说法错误的是( ) A、甲中碳元素的化合价为+2价 B、丙中C,H,O的质量比为12:3:8 C、丁的化学式为H2O2 D、该反应体现无机物可转化为有机物15. 烧杯中有一定质量的氧化镁和碳酸镁的混合物,向其中加入150g稀盐酸,恰好完全反应.一定温度下,得到156g不饱和溶液.下列数据中,与反应后溶液的溶质质量分数最接近的是( )A、9.1% B、6.1% C、12.2% D、16.6%
A、甲中碳元素的化合价为+2价 B、丙中C,H,O的质量比为12:3:8 C、丁的化学式为H2O2 D、该反应体现无机物可转化为有机物15. 烧杯中有一定质量的氧化镁和碳酸镁的混合物,向其中加入150g稀盐酸,恰好完全反应.一定温度下,得到156g不饱和溶液.下列数据中,与反应后溶液的溶质质量分数最接近的是( )A、9.1% B、6.1% C、12.2% D、16.6%二、信息分析题
-
16. 根据问题填空:
(1)、化学用语是学习化学的重要工具,用适当的化学符号填空①2个氩原子; ②人体内含量最高的金属元素;
③醋酸溶液中的阳离子是; ④极易与血红蛋白结合的有毒气体是。
(2)、化学——我们的生活 ,利用你所学的化学知识,完成下列相关问题:①梅花扑鼻香自来,从分子性质的角度解释,这是因为_。
②将乒乓球碎片和滤纸片置于薄铜片上,用酒精灯火焰加热铜片。能验证燃烧的条件之一是:。
③洗涤剂去除油污是因为洗涤剂具有作用。
④打开汽水瓶塞,有气泡冒出,说明气体溶解度与有关。
⑤英语中有句谚语“每天一个苹果,医生远离我”,说明苹果是一种对人体健康非常有益的水果,苹果为人体提供的对应营养素是。
⑥装汽水的塑料瓶属于(填“金属材料”或“合成材料”或“复合材料”)。
17. 根据下列装置回答问题。 (1)、请写出仪器a的名称:。(2)、用氯酸钾和二氧化锰为原料制取较纯净的氧气可选用的装置组合为(填字母,下同),此反应的基本类型为。二氧化锰在反应中的作用是。(3)、小曹老师带领学生进行上述实验时,发现“一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此,小曹老师让该同学往集气瓶装入半瓶水,再用排水法收集1/2集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃。
(1)、请写出仪器a的名称:。(2)、用氯酸钾和二氧化锰为原料制取较纯净的氧气可选用的装置组合为(填字母,下同),此反应的基本类型为。二氧化锰在反应中的作用是。(3)、小曹老师带领学生进行上述实验时,发现“一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此,小曹老师让该同学往集气瓶装入半瓶水,再用排水法收集1/2集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃。① 用下图方案收集“1/2集气瓶的氧气”,其中最合理的是 (填字母);

② 用排水法收集气体时,如何判断集气瓶中气体已收集满?答:;
③ 空气中氧气的体积分数约为21%。本实验中,集气瓶内的氧气约占总体积的%,所以用“使带火星木条复燃”来检验集气瓶中充满氧气的方法不可靠。
(4)、实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式是 , 若用F装置收集二氧化碳,气体应从端通入(填“b”或“c”)。18. 金属是重要的资源。
(1)、铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的二氧化碳?”如图所示实验中(试管内的“ ”均为铜片),只需完成实验即可达到探究目的(填字母组合)。
”均为铜片),只需完成实验即可达到探究目的(填字母组合)。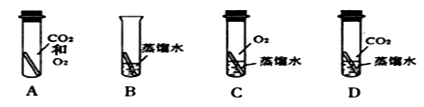 (2)、铁是世界上年产量第一的金属。工业上用一氧化碳和赤铁矿炼铁的化学方程式是 , 得到的生铁可炼成钢。(3)、铝是地壳中含量最多的金属元素。
(2)、铁是世界上年产量第一的金属。工业上用一氧化碳和赤铁矿炼铁的化学方程式是 , 得到的生铁可炼成钢。(3)、铝是地壳中含量最多的金属元素。①用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,观察到熔化的铝被一层膜兜着并不滴落,产生该现象的原因是。
②铝和氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2H2O= 2NaAlO2+3H2↑,足量的稀盐酸与氢氧化钠溶液分别和等质量的铝粉充分反应,产生氢气的质量分别为m1、m2 , 下列有关m1、m2大小关系的说法正确的是(填字母)。
A.m1>m2 B.m1<m2 C.m1=m2 D.无法比较
(4)、验证Cu、Fe、Al金属的活动性强弱,下列的实际组合实验方案不能达到实验目的是 。A、FeSO4溶液、Al、Cu B、Al2(SO4)3溶液、稀盐酸溶液、Fe、Cu C、Al2(SO4)3溶液、FeSO4溶液、Cu D、AlCl3溶液、CuCl2溶液、Fe19. 某兴趣小组同学对NaOH、Na2CO3、NaHCO3、NaCl等常见的钠的化合物进行了研究。(1)、【知识回顾】下列相关说法正确的是 。A、氢氧化钠俗名叫烧碱,可用于改良酸性土壤 B、碳酸钠俗称纯碱,属于碱 C、碳酸氢钠俗称苏打,可用于治疗胃酸过多 D、氯化钠在自然界中主要存在于海水中(2)、【提出问题】NaOH露置于空气中易变质,那么实验室中的氢氧化钠有没有变质呢?该小组同学对实验室中一瓶氢氧化钠固体样品的成分进行了探究。【查阅资料】Ⅰ.NaOH在空气中不会转化成NaHCO3。
Ⅱ.BaCl2溶液呈中性,Ba(OH)2是可溶性碱。
Ⅲ.CO2在饱和的NaHCO3溶液中几乎不溶解。
【提出猜想】猜想①:样品中只有NaOH
猜想②:样品中只有Na2CO3
猜想③:样品中既有NaOH又有Na2CO3
NaOH变质反应的化学方程式为。
(3)、【实验探究】兴趣小组同学设计如下实验进行探究。实验操作
实验现象与结论
①取少量样品,加足量水。
样品全部溶解,得无色溶液。
②.取少量实验①所得无色溶液于试管中,滴加足量稀盐酸。
有气泡产生,则猜想(填“①”、“②”或“③”)不成立。
③.取少量实验①所得无色溶液于试管中,滴加 溶液。
有白色沉淀产生,有关化学方程式为。
④.静置一段时间后,取实验3中试管中上层清液,滴加。
对应现象: ,则猜想③成立。
(4)、【定量研究】上述样品变质的程度如何呢?该兴趣小组同学设计如图装置测定样品中Na2CO3的质量分数。
步骤如下:
①按图连接好装置,并检查气密性;
②准确称取该样品1.0g,放入烧瓶内;
③打开分液漏斗活塞,滴加30.0%的稀硫酸至过量,关闭活塞;
④反应结束后,量筒内液体的读数为55.0mL。(已知:室温条件下,CO2的密度为1.6g•L﹣1)
B装置集气瓶内原有的空气对实验结果(填“有”或“没有”)影响。
(5)、B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是;
(6)、充分反应后,装置A中残留的二氧化碳对实验结果是否有明显影响?填(“有”或“没有”)
(7)、计算该样品中Na2CO3的质量分数(写出计算过程,结果保留到0.1%)。