初中化学人教版一轮复习考点16质量守恒定律及其应用 化学方程式
试卷更新日期:2021-04-05 类型:一轮复习
一、单选题
-
1. 下图是制取饮用水消毒剂二氧化氯的微观过程图,下列说法错误的是( )
(其中
 表示氯原子,
表示氯原子,  表示钠原子,
表示钠原子,  表示氧原子)
表示氧原子) A、二氧化氯的化学式为ClO2 B、二氧化氯分子中氯、氧原子个数比为1:2 C、反应物和生成物中共有两种氧化物 D、化学反应前后原子的种类不变2. 下列实验中,固体质量变化与下图相符合的是( )
A、二氧化氯的化学式为ClO2 B、二氧化氯分子中氯、氧原子个数比为1:2 C、反应物和生成物中共有两种氧化物 D、化学反应前后原子的种类不变2. 下列实验中,固体质量变化与下图相符合的是( ) A、硫在盛有氧气的集气瓶中燃烧 B、铁丝在盛有氧气的集气瓶中燃烧 C、一定量的镁条在氧气中充分燃烧 D、向盛有氢氧化钠溶液的试管中逐滴加入硫酸铜溶液3. 铜锈的主要成分是碱式碳酸铜。碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3 2CuO+X+CO2↑。下列说法错误的是( )A、X是相对分子质量最小的氧化物 B、反应前后各元素的质量均保持不变 C、反应前后固体物质中铜元素的质量分数不变 D、加热Cu2(OH)2CO3的试管口应稍向下倾斜4. 在反应2A+B=2C中,48gA与一定质量的B恰好完全反应,生成80gC。则A与B的相对分子质量之比为( )A、2:1 B、3:4 C、1:2 D、4:35. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )。
A、硫在盛有氧气的集气瓶中燃烧 B、铁丝在盛有氧气的集气瓶中燃烧 C、一定量的镁条在氧气中充分燃烧 D、向盛有氢氧化钠溶液的试管中逐滴加入硫酸铜溶液3. 铜锈的主要成分是碱式碳酸铜。碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3 2CuO+X+CO2↑。下列说法错误的是( )A、X是相对分子质量最小的氧化物 B、反应前后各元素的质量均保持不变 C、反应前后固体物质中铜元素的质量分数不变 D、加热Cu2(OH)2CO3的试管口应稍向下倾斜4. 在反应2A+B=2C中,48gA与一定质量的B恰好完全反应,生成80gC。则A与B的相对分子质量之比为( )A、2:1 B、3:4 C、1:2 D、4:35. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )。 A、丁一定是该反应的催化剂 B、该反应的基本类型是分解反应 C、参与反应的甲、乙质量比为14:3 D、参与反应的甲、丙质量比为7:106. 下图为治理汽车尾气反应的微观示意图,有关说法错误的是( )
A、丁一定是该反应的催化剂 B、该反应的基本类型是分解反应 C、参与反应的甲、乙质量比为14:3 D、参与反应的甲、丙质量比为7:106. 下图为治理汽车尾气反应的微观示意图,有关说法错误的是( ) A、该反应不属于置换反应 B、该反应生成的丙和丁的分子个数比为1:1 C、反应前后,分子的种类一定发生变化 D、该反应中涉及的物质有三种为氧化物7. 实验是学习化学的重要手段,通过实验可以培养我们的实践能力和创新精神。下列实验设计不能达到实验目的是( )
A、该反应不属于置换反应 B、该反应生成的丙和丁的分子个数比为1:1 C、反应前后,分子的种类一定发生变化 D、该反应中涉及的物质有三种为氧化物7. 实验是学习化学的重要手段,通过实验可以培养我们的实践能力和创新精神。下列实验设计不能达到实验目的是( )选项
A
B
C
D
实验设计




实验目的
探究CO2与水反应
验证质量守恒定律
探究分子的运动
比较合金和纯金属的硬度
A、A B、B C、C D、D8. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中正确的是( ) A、该反应中,甲、乙的质量变化之比为7:2 B、丙可能为该反应的催化剂 C、该反应为分解反应 D、反应后密闭容器内的物质是纯净物9. 下列化学方程式书写正确的是( )A、 B、 C、 D、10. 化学方程式 2Mg+O2 2MgO 可读作( )A、镁加氧气等于氧化镁 B、2 个镁加 1 个氧气等于 2 个氧化镁 C、镁和氧气在点燃条件下生成氧化镁 D、镁元素加氧元素点燃生成氧化镁11. 2020 年 5 月 5 日,配置有氢氧发动机的长征五号B 火箭,搭载我国新一代载人试验飞船顺利升空,飞船成功返回。从变化观念和平衡思想认识反应:2H2+O2 2H2O。下列说法正确的是( )A、氢气和氧气混合生成水 B、氢气和氧气反应吸收热量 C、2g 氢气和 1g 氧气反应生成 3g 水 D、反应前后元素种类不变、元素的存在形态改变12. 氨气(NH3)燃烧反应的化学方程式为:4NH3 + 3O2 6H2O + 2 X,则X的化学式为( )A、H2 B、O2 C、N2 D、NO2
A、该反应中,甲、乙的质量变化之比为7:2 B、丙可能为该反应的催化剂 C、该反应为分解反应 D、反应后密闭容器内的物质是纯净物9. 下列化学方程式书写正确的是( )A、 B、 C、 D、10. 化学方程式 2Mg+O2 2MgO 可读作( )A、镁加氧气等于氧化镁 B、2 个镁加 1 个氧气等于 2 个氧化镁 C、镁和氧气在点燃条件下生成氧化镁 D、镁元素加氧元素点燃生成氧化镁11. 2020 年 5 月 5 日,配置有氢氧发动机的长征五号B 火箭,搭载我国新一代载人试验飞船顺利升空,飞船成功返回。从变化观念和平衡思想认识反应:2H2+O2 2H2O。下列说法正确的是( )A、氢气和氧气混合生成水 B、氢气和氧气反应吸收热量 C、2g 氢气和 1g 氧气反应生成 3g 水 D、反应前后元素种类不变、元素的存在形态改变12. 氨气(NH3)燃烧反应的化学方程式为:4NH3 + 3O2 6H2O + 2 X,则X的化学式为( )A、H2 B、O2 C、N2 D、NO2二、填空题
-
13. 从科学家认识物质的视角认识二氧化碳。

①组成角度:二氧化碳(CO2)是由种元素组成的。
②分类角度:CO2属于(选填“单质”或“化合物”)。
③性质角度:如图,b处木条首先熄灭,说明CO2的密度比空气(选填“大”或“小”)。
④应用角度:用CO2生成甲醇,反应的微观示意图为:

参加反应的两种分子个数比为。
⑤制取角度:实验室用含0.2molCaCO3的大理石和足量稀盐酸反应,可生成CO2mol。(根据化学方程式列式计算)
14. 写出下列反应的化学方程式:①碳在氧气中充分燃烧。
②铁丝在氧气中燃烧。
③加热铜粉。
④双氧水和二氧化锰的混合物。
⑤实验室制取二氧化碳的反应原理。
⑥向澄清的石灰水中通入二氧化碳气体的反应
三、实验探究题
-
15. 以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
(提出问题)化学反应前后各物质的质量总和是否相等?
(1)、(猜想与假设)猜想1:不相等; 猜想2:。(2)、(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。甲组
乙组
实验方案


实验现象
有气泡产生,天平指针向右偏转
铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转
结论
猜想1正确
猜想2正确,反应的化学方程式:
(3)、(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在中进行。(4)、(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是。
四、综合题
-
16. “84消毒液”是一种以次氯酸钠(NaClO) 为主的高效消毒剂,呈无色或淡黄色液体,且具有刺激性气味,有效氯含量为5.5~6.5%,被广泛用于宾馆、医院和家庭等场所的消毒。84消毒液漂白作用较强,对织物有漂白作用。洁厕灵的主要成分是HCl,与“84消毒液”反应会生成有毒的氯气(Cl2)。NaClO不稳定,如图是对其稳定性的研究结果。依据文章内容,回答下列问题:
 (1)、次氯酸钠(NaClO) 中氯元素的化合价是。(2)、25℃时,某“84消毒液”pH为10,将其滴入紫色石蕊溶液中,石蕊溶液变。(3)、次氯酸钠自身没有消毒作用,有消毒作用的是次氯酸钠与空气中二氧化碳反应得到的次氯酸,反应方程式为: , 则X的化学式为。(4)、勿用50℃以上热水稀释的原因是。(5)、下列有关“84消毒液”的说法中,正确的是(填序号)。
(1)、次氯酸钠(NaClO) 中氯元素的化合价是。(2)、25℃时,某“84消毒液”pH为10,将其滴入紫色石蕊溶液中,石蕊溶液变。(3)、次氯酸钠自身没有消毒作用,有消毒作用的是次氯酸钠与空气中二氧化碳反应得到的次氯酸,反应方程式为: , 则X的化学式为。(4)、勿用50℃以上热水稀释的原因是。(5)、下列有关“84消毒液”的说法中,正确的是(填序号)。A “84消毒液”应避免接触皮肤,因消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用
B 现有12%的次氯酸钠溶液20g,可加800g水稀释成0.3%的次氯酸钠溶液
C “84消毒液”漂白作用较强,对彩色衣物要慎用
D “84消毒液”不要与其他洗涤剂或消毒剂混合使用是因为避免产生有毒的氯气
17. 请沿用科学家认识事物的方式认识“空气”。(1)、从分类角度:空气属于(填“混合物”或“纯净物”)。(2)、从微观角度:用“○”表示氮原子,用“”表示氧原子。①用“
 ”可表示的微粒是(填名称)。
”可表示的微粒是(填名称)。②同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,下图中可表示空气微观模型的是(填字母标号)。
 (3)、从变化角度:已知:常压下,氮气沸点―196℃,氧气沸点--183℃。将燃着的木条置于盛满液态空气(模拟分离液态空气条件)的烧杯口,观察到的现象是。该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是(4)、从应用角度:利用空气制取氮肥的流程下图所示。
(3)、从变化角度:已知:常压下,氮气沸点―196℃,氧气沸点--183℃。将燃着的木条置于盛满液态空气(模拟分离液态空气条件)的烧杯口,观察到的现象是。该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是(4)、从应用角度:利用空气制取氮肥的流程下图所示。
①Ⅰ中参加反应的单质甲为
②Ⅱ中反应的化学方程式为
③物质所含元素化合价发生变化的反应称为氧化还原反应,反应Ⅱ(填“属于”或“不属于”)氧化还原反应。
(5)、从环保角度,下列保护空气措施不合理的有_____(填序号)。A、工厂通过加高烟囱直接排放废气 B、推广使用乙醇汽油代替普通汽油 C、提倡步行、骑自行车等“低碳”出行方式五、计算题
-
18. 为探究CuO和C反应的最佳质量比(忽略副反应),化学兴趣小组取CuO和C的混合物17.2g,按不同的质量比进行实验,实验结果如图所示,横坐标表示混合物中CuO所占的质量分数,纵坐标表示生成物中Cu的质量。
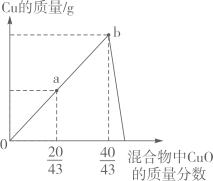 (1)、分析可知,CuO和C的最佳质量比对应图中的点。(2)、计算a点时,产生CO2的质量(写出详细计算过程)。
(1)、分析可知,CuO和C的最佳质量比对应图中的点。(2)、计算a点时,产生CO2的质量(写出详细计算过程)。
-