初中化学人教版一轮复习考点13物质的构成与组成
试卷更新日期:2021-04-05 类型:一轮复习
一、单选题
-
1. 奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源,这里的“钙”指( )A、钙离子 B、钙原子 C、钙元素 D、钙单质2. 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是最小的粒子,不可再分 D、氯化钠是由钠离子和氯离子构成的3. 关于下列符号或图示的说法正确的是( )
①N2②Mg2+③
 ④
④ 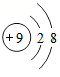 ⑤
⑤ 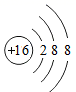 ⑥
⑥ 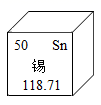 A、①表示两个氮原子 B、②和④均表示阳离子 C、③和⑤所表示的微粒化学性质相似 D、由⑥可知锡的相对原子质量为118.714. 下列物质中,由分子构成的是( )A、水 B、汞 C、氯化钠 D、金刚石5. 我国的5G通信芯片主要由氮化镓材料制成。下图是镓元素在元素周期表中的相关信息,下列说法错误的是( )
A、①表示两个氮原子 B、②和④均表示阳离子 C、③和⑤所表示的微粒化学性质相似 D、由⑥可知锡的相对原子质量为118.714. 下列物质中,由分子构成的是( )A、水 B、汞 C、氯化钠 D、金刚石5. 我国的5G通信芯片主要由氮化镓材料制成。下图是镓元素在元素周期表中的相关信息,下列说法错误的是( ) A、镓属于金属元素 B、镓原子的质子数是31 C、镓原子质量是69.72g D、镓原子核外有31个电子6. 宏观辨识与微观探析是化学核心素养之一。下列对宏观事实的微观推理错误的是( )A、6000L氧气经加压可装入40L的钢瓶中,是因为氧分子变小 B、氢气与氧气属于不同物质,是因为它们由不同分子构成 C、墙内开花墙外可闻到花香,是因为分子在不断地运动 D、碱有相似的化学性质,是因为碱溶液中都含有OH-7. 下列微粒中不能直接构成物质的是( )A、分子 B、原子 C、中子 D、离子8. 如图所示,在小烧杯A中盛有滴入酚酞溶液的蒸馏水,然后向小烧杯B中倒入浓氨水,立即用大烧杯罩住烧杯A和B,过一段时间后发现烧杯A中溶液由无色变为红色。下列有关说法错误的是( )
A、镓属于金属元素 B、镓原子的质子数是31 C、镓原子质量是69.72g D、镓原子核外有31个电子6. 宏观辨识与微观探析是化学核心素养之一。下列对宏观事实的微观推理错误的是( )A、6000L氧气经加压可装入40L的钢瓶中,是因为氧分子变小 B、氢气与氧气属于不同物质,是因为它们由不同分子构成 C、墙内开花墙外可闻到花香,是因为分子在不断地运动 D、碱有相似的化学性质,是因为碱溶液中都含有OH-7. 下列微粒中不能直接构成物质的是( )A、分子 B、原子 C、中子 D、离子8. 如图所示,在小烧杯A中盛有滴入酚酞溶液的蒸馏水,然后向小烧杯B中倒入浓氨水,立即用大烧杯罩住烧杯A和B,过一段时间后发现烧杯A中溶液由无色变为红色。下列有关说法错误的是( )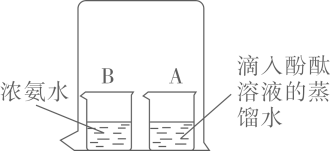 A、实验说明浓氨水易挥发 B、实验说明分子不断运动 C、烧杯A中溶液变红,说明显碱性 D、烧杯B中溶液的pH逐渐变大9. 下列宏观事实的微观解释错误的是( )A、墙内开花墙外香——分子是不断运动的 B、6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小 C、硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子 D、一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同10. 如图是某原子的结构示意图和对应元素在元素周期表中的信息。下列说法错误的是( )
A、实验说明浓氨水易挥发 B、实验说明分子不断运动 C、烧杯A中溶液变红,说明显碱性 D、烧杯B中溶液的pH逐渐变大9. 下列宏观事实的微观解释错误的是( )A、墙内开花墙外香——分子是不断运动的 B、6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小 C、硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子 D、一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同10. 如图是某原子的结构示意图和对应元素在元素周期表中的信息。下列说法错误的是( )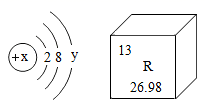 A、x为13 B、该原子易失去电子 C、该元素为非金属元素 D、该元素位于元素周期表的第三周期11. 如图为某粒子结构示意图,下列说法错误的是( )
A、x为13 B、该原子易失去电子 C、该元素为非金属元素 D、该元素位于元素周期表的第三周期11. 如图为某粒子结构示意图,下列说法错误的是( ) A、该粒子属于非金属元素 B、该粒子核外电子数为17 C、该粒子具有3个电子层 D、在化学反应中,该元素原子易得电子形成Cl-12. 制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )A、22 B、48 C、70 D、2613. 下列因果关系错误的是( )A、因为分子构成不同,所以水和过氧化氢的化学性质不同 B、因为质子数不同,所以碳原子和氮原子所属的元素种类不同 C、因为碳原子排列方式不同,所以金刚石和石墨的性质完全不同 D、因为电子层数及最外层电子数不同,所以钠原子
A、该粒子属于非金属元素 B、该粒子核外电子数为17 C、该粒子具有3个电子层 D、在化学反应中,该元素原子易得电子形成Cl-12. 制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )A、22 B、48 C、70 D、2613. 下列因果关系错误的是( )A、因为分子构成不同,所以水和过氧化氢的化学性质不同 B、因为质子数不同,所以碳原子和氮原子所属的元素种类不同 C、因为碳原子排列方式不同,所以金刚石和石墨的性质完全不同 D、因为电子层数及最外层电子数不同,所以钠原子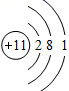 和钠离子
和钠离子  的化学性质不同
的化学性质不同
二、填空题
-
14. 元素周期表是学习和研究化学的重要工具,下图为元素周期表的一部分,根据下表回答问题:
 (1)、8号元素属于(填“金属元素”或“非金属元素”)。(2)、11号元素与17号元素组成化合物的化学式为:。(3)、某粒子结构示意图为
(1)、8号元素属于(填“金属元素”或“非金属元素”)。(2)、11号元素与17号元素组成化合物的化学式为:。(3)、某粒子结构示意图为 ,该粒子所表示的符号是:。 (4)、煤、石油、天然气等化石燃料中主要含有上表中的元素(填元素符号)。15. 化学用语是学习化学的重要工具,是国际通用的化学语言,请用相关化学用语填空。(1)、氮元素; 两个氧原子。(2)、3Fe2+表示。(3)、氮肥能促进农作物茎、叶生长,但铵态氮肥与碱性物质混合使用会降低肥效,原因是生成一种有刺激性气味的气体,该气体是(写化学式)。(4)、写出下列化学方程式
,该粒子所表示的符号是:。 (4)、煤、石油、天然气等化石燃料中主要含有上表中的元素(填元素符号)。15. 化学用语是学习化学的重要工具,是国际通用的化学语言,请用相关化学用语填空。(1)、氮元素; 两个氧原子。(2)、3Fe2+表示。(3)、氮肥能促进农作物茎、叶生长,但铵态氮肥与碱性物质混合使用会降低肥效,原因是生成一种有刺激性气味的气体,该气体是(写化学式)。(4)、写出下列化学方程式①水通电分解;
②天然气燃烧。
三、实验探究题
-
16. 小倩同学了解到:外国人把中国称为“China”,在英文中与瓷器是同一个单词。“青花瓷”又是在中国瓷器中最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。
她查阅元素周期表发现钴(读音: )元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
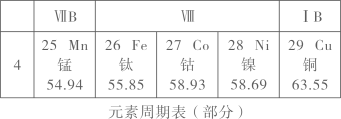
(提出问题)小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
(寻求帮助)
(1)、(咨询老师)得知:因为铁与钴两种元素原子的结构具有相同点(见右图),使得二者的化学性质相似。因此把这两种元素放在一起。请你帮助小倩完成下列问题: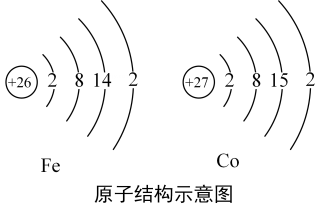
①钴元素在元素周期表中的原子序数为 , 一个钴原子比一个铁原子多一个(填序号)。
a.中子
b.电子
c.质子
d.电子层
②铁原子与钴原子具有相同的(填序号,下同)。元素的化学性质主要与原子的有关,因此二者的化学性质相似。
a.核电荷数
b.核外电子数
c.电子层数
d.最外层电子数
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为;钴在氧气中燃烧生成Co3O4 , 化学方程式为。
(2)、(查阅资料)钴元素有着广泛的用途:钴及其化合物在材料生产、化工生产、医疗中都有着广泛的应用。钴在电池制造中需求量增长很快,钴酸锂(已知:化学式为LiCoO2 , 锂元素化合价为+1)常用作手机电池的正极材料,其中钻元素的化合价为。(3)、(深入探讨)(产生问题)既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
(设计并实验验)
根据所学知识,同学们已知下列反应可以进行,并进行实验:
观察记录实验现象:氧化亚铁为黑色固体;实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。(查阅资料得知:原因是溶液中的Fe(OH)2遇空气中的氧气生成Fe(OH)3)
同学们欲探究钴元素化合物的性质,设计并进行了如下实验:
请你依据实验现象,完成下列问题:
I.实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式。另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解溶液呈绿色。说明反应后钴离子在溶液中呈现的颜色与加入酸的有关。
Ⅱ.实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的有关。通过实验探究,同学们得出结论:铁和钴两种元素的化合物化学性质相似。
四、综合题
-
17. 元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分,元素周期表的横行叫做周期,纵行叫做族,分为主族、副族、VⅢ族和0族,主族用字母A表示,共有七个主族,依次用IA、ⅡA……表示,同一主族元素化学性质相似。根据下表回答问题:
族

周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
VIA
VIIA
0
一
1H氢
2 He氦
二
3Li锂
4 Be铍
5B硼
6C碳
7N氮
8O氧
9F氟
10Ne氖
三
11Na钠
12Mg镁
13Al铝
14Si硅
15P磷
16S硫
17Cl氯
18Ar氩
(1)、观察元素周期表,可发现同一周期接近尾部的是(填“金属”或“非金属”)元素,在化学反应中容易(填“得到”或“失去”)电子。(2)、根据元素周期表可以查到第三周期、第ⅡA族的元素是 , 它的原子序数为。(3)、氯离子(Cl-)的质子数是17,则氯离子的核外电子总数为。(4)、在元素周期表中,He元素不排在ⅡA族而排在0族的依据是。18. 如图是氯元素在元素周期表中的信息以及四种粒子的结构示意图。请根据图回答下列问题: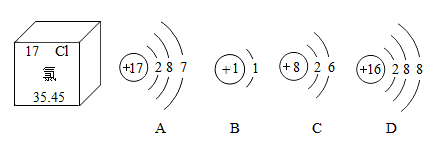 (1)、氯元素的相对原子质量是。(2)、A-D中具有相对稳定结构的粒子是(填字母序号)。(3)、为了缓解二氧化碳过多引起的温室效应加剧,我国科学研究人员成功研制出一种纳米纤维催化剂,将二氧化碳转化为液体燃料甲醇(CH3OH),其反应的微观示意图如下,请写出该反应的化学方程式。
(1)、氯元素的相对原子质量是。(2)、A-D中具有相对稳定结构的粒子是(填字母序号)。(3)、为了缓解二氧化碳过多引起的温室效应加剧,我国科学研究人员成功研制出一种纳米纤维催化剂,将二氧化碳转化为液体燃料甲醇(CH3OH),其反应的微观示意图如下,请写出该反应的化学方程式。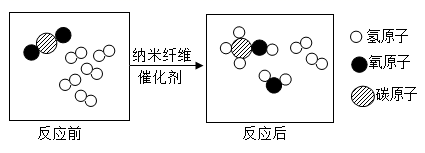
-