2021年初中科学中考一轮复习-酸和碱
试卷更新日期:2021-03-31 类型:一轮复习
一、单选题
-
1. 规范实验操作是获得实验成功的重要保证,如图实验操作正确的是( )A、滴加氯化钙溶液
 B、测溶液的pH值
B、测溶液的pH值  C、稀释浓硫酸
C、稀释浓硫酸  D、称量氢氧化钠
D、称量氢氧化钠  2. 下列关于Ca(OH)2的说法,错误的是( )A、微溶于水,水溶液呈碱性,能使无色酚酞变红 B、能与酸反应,可用于降低土壤的酸性 C、可与CuSO4溶液按一定比例混合配制波尔多液,该反应属于复分解反应 D、其澄清溶液可用来检验CO2 , 与CO2反应后溶液质量增加3. 蚂蚁等昆虫叮咬人时,会向人体注入一种物质R,使皮肤红肿。实验测定物质R呈酸性,由此推断,要消除红肿,可涂抹下列物质中的( )A、食醋 B、肥皂水 C、浓氢氧化钠 D、稀盐酸4. 下列物质的性质与用途的对应关系正确的是( )
2. 下列关于Ca(OH)2的说法,错误的是( )A、微溶于水,水溶液呈碱性,能使无色酚酞变红 B、能与酸反应,可用于降低土壤的酸性 C、可与CuSO4溶液按一定比例混合配制波尔多液,该反应属于复分解反应 D、其澄清溶液可用来检验CO2 , 与CO2反应后溶液质量增加3. 蚂蚁等昆虫叮咬人时,会向人体注入一种物质R,使皮肤红肿。实验测定物质R呈酸性,由此推断,要消除红肿,可涂抹下列物质中的( )A、食醋 B、肥皂水 C、浓氢氧化钠 D、稀盐酸4. 下列物质的性质与用途的对应关系正确的是( )选项
性质
用途
A
浓硫酸具有脱水性
干燥氧气
B
氢氧化钠呈碱性
改良酸性土壤
C
稀盐酸能与某些金属氧化物反应
除铁锈
D
氢氧化钠能与某些非金属氧化物反应
吸收一氧化碳
A、A B、B C、C D、D5. 以下是生活中常见水果的 pH 值,其中酸性最强的是( ) A、西瓜 B、青柠檬 C、葡萄 D、白梨6. 实验室中一瓶浓盐酸敞口放置一定时间,下列四幅图,能正确反映其变化关系的是( )A、
A、西瓜 B、青柠檬 C、葡萄 D、白梨6. 实验室中一瓶浓盐酸敞口放置一定时间,下列四幅图,能正确反映其变化关系的是( )A、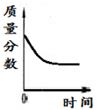 B、
B、 C、
C、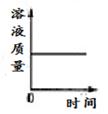 D、
D、 7. 向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸溶液。下列能正确反映其对应变化关系的是( )A、
7. 向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸溶液。下列能正确反映其对应变化关系的是( )A、 B、
B、 C、
C、 D、
D、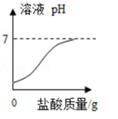 8. 小科在研究碱的化学性质时,设计了如图所示的五组实验,下列叙述正确的是( )
8. 小科在研究碱的化学性质时,设计了如图所示的五组实验,下列叙述正确的是( ) A、甲组实验能观察到无色变成红色,可推出氢氧化铜也能使指示剂变色 B、乙组实验无明显现象,说明两者不能发生反应 C、丙组和戊组实验能观察到相同现象 D、丁组实验产生蓝色絮状沉淀,说明凡是碱都能和含铜离子的溶液发生反应9. 下列物质敞口放置在空气中,质量会增加但不发生化学变化的是( )A、氢氧化钠固体 B、浓硫酸 C、熟石灰 D、浓盐酸10. 小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A、甲组实验能观察到无色变成红色,可推出氢氧化铜也能使指示剂变色 B、乙组实验无明显现象,说明两者不能发生反应 C、丙组和戊组实验能观察到相同现象 D、丁组实验产生蓝色絮状沉淀,说明凡是碱都能和含铜离子的溶液发生反应9. 下列物质敞口放置在空气中,质量会增加但不发生化学变化的是( )A、氢氧化钠固体 B、浓硫酸 C、熟石灰 D、浓盐酸10. 小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )

 A、①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞 B、③中反应的实质是H+和OH-结合生成水 C、⑤中稀释浓硫酸时,倒入的乙物质是水 D、⑥中酚酞试液用完后,滴管及时清洗11. 小科按图示操作进行酸的性质实验,下列有关分析正确的是( )
A、①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞 B、③中反应的实质是H+和OH-结合生成水 C、⑤中稀释浓硫酸时,倒入的乙物质是水 D、⑥中酚酞试液用完后,滴管及时清洗11. 小科按图示操作进行酸的性质实验,下列有关分析正确的是( ) A、若X是稀硫酸,则a可能是紫色石蕊试液 B、若X是稀硫酸,则d一定是CuO固体 C、若X是稀盐酸,则c一定是单质 D、若b是Fe2O3 , 则黄色溶液一定是氯化铁12. 生铁和足量的稀盐酸充分反应后会留有残渣,残渣的主要成分是( )A、氯化亚铁 B、碳 C、氯化铁 D、铁
A、若X是稀硫酸,则a可能是紫色石蕊试液 B、若X是稀硫酸,则d一定是CuO固体 C、若X是稀盐酸,则c一定是单质 D、若b是Fe2O3 , 则黄色溶液一定是氯化铁12. 生铁和足量的稀盐酸充分反应后会留有残渣,残渣的主要成分是( )A、氯化亚铁 B、碳 C、氯化铁 D、铁二、填空题
-
13. 为探究一瓶久置的氢氧化钠固体样品是否全部变质,小科将少量样品配制成溶液,取少 量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2 溶液呈中性)
 (1)、由甲图实验现象可以得出溶液呈性。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、图乙中,滴加足量的 BaCl2 溶液的目的是。14. 稀盐酸是实验室中的一种重要试剂,用途广泛。(1)、在稀盐酸的下列用途中,不能用稀硫酸代替的是。(选填序号)
(1)、由甲图实验现象可以得出溶液呈性。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、图乙中,滴加足量的 BaCl2 溶液的目的是。14. 稀盐酸是实验室中的一种重要试剂,用途广泛。(1)、在稀盐酸的下列用途中,不能用稀硫酸代替的是。(选填序号)①金属表面除锈;②除去氯化钠中少量的氢氧化钠;③实验室制取二氧化碳。
(2)、向盛有稀盐酸的烧杯中加入适量的某种物质与之反应,反应前后烧杯内溶液中主要离子种类及个数比例变化如图所示,则加入的固体可能是下列中的(选填序号)。
①铁 ②碳酸钠 ③氧化铁 ④氢氧化镁
15. 将稀盐酸逐滴加入盛氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入氢氧化钠溶液的质量变化如图所示。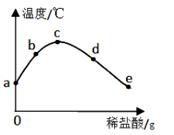 (1)、该反应的实质是。(2)、从a到c的过程中,溶液的pH值。(填“升高”“降低”或“不变”)(3)、图中各点中溶质种类完全相同的两点是。(填字母)16. “玩卡片”是一种小游戏。某兴趣小组给卡片上标上物质的化学式,要求甲、乙同学各出一张,先后两张卡中的物质必须会发生反应,直到最后所剩卡片最少为胜利者。
(1)、该反应的实质是。(2)、从a到c的过程中,溶液的pH值。(填“升高”“降低”或“不变”)(3)、图中各点中溶质种类完全相同的两点是。(填字母)16. “玩卡片”是一种小游戏。某兴趣小组给卡片上标上物质的化学式,要求甲、乙同学各出一张,先后两张卡中的物质必须会发生反应,直到最后所剩卡片最少为胜利者。 (1)、六张卡片中属于碱的是。(填化学式)(2)、若乙同学先出卡片“CuO”,甲同学可选的卡片有张。(3)、若甲同学先出卡片 2,可以让两人卡片出完。此出法中,乙同学最后出的卡片是。
(1)、六张卡片中属于碱的是。(填化学式)(2)、若乙同学先出卡片“CuO”,甲同学可选的卡片有张。(3)、若甲同学先出卡片 2,可以让两人卡片出完。此出法中,乙同学最后出的卡片是。(填卡片序号)
17. 从下列物质中,选择正确答案的序号填在相应的空格里:①氢氧化钠固体 ②碳酸钙 ③食醋 ④熟石灰
(1)、农业上用于改良酸性土壤的是。(2)、能用来干燥氧气的物质是。18. 室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度随加入盐酸质量而变化的曲线如图所示。 (1)、表明稀盐酸和氢氧化钠恰好完全反应的是(选填“A”、“B”、“C”)点。(2)、在C点溶液中加入碳酸钙,现象为。
(1)、表明稀盐酸和氢氧化钠恰好完全反应的是(选填“A”、“B”、“C”)点。(2)、在C点溶液中加入碳酸钙,现象为。三、实验探究题
-
19. 工业上用电解饱和食盐水的方法制备烧碱,小乐对用此方法生产的、外包装破损的烧碱样品进行了如下探究。
【提出问题】烧碱样品中含有哪些杂质?
【建立猜想】猜想1:可能含有碳酸钠,判断依据是氢氧化钠能和二氧化碳反应生成碳酸钠。
猜想2:可能含有氯化钠,判断依据是在化工生产中,原料可能。
【实验探究】
实验操作
实验现象
实验结论
取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液
烧碱样品中含有碳酸钠和氯化钠
【反思评价】除去烧碱样品中含有的少量碳酸钠,可选用的药品是。
A.CuCl2溶液 B.Ba(NO3)2溶液 C.Ba(OH)2 溶液 D.KOH溶液
20. 小敏研究影响锌与盐酸反应快慢的因素。
序号
盐酸溶液浓度
2分钟内产生氢气的体积
1
5%
10mL
2
15%
28mL
(1)、 图甲中A、B仪器可以组装一套测量气体体积的装置,利用该装置时A中的管接c。(2)、他选用2克完全相同的锌片分别和同体积5%、15%的稀盐酸进行实验。获得表格数据。由此推断实验是通过来体现反应快慢的。(3)、小敏分析数据得到如下结论:锌与盐酸反应快慢与盐酸浓度有关,盐酸浓度越大反应越快。其他同学认为结论不可靠,他们的依据是:。(4)、实验中小敏发现锌与稀盐酸反应时,一开始产生氢气速度并没有随盐酸浓度的减少而减慢,查阅资料得知化学反应中往往伴随着能量变化。由此作出猜想:锌与盐酸反应快慢还与有关。21. 做酸碱实验时,小敏将稀盐酸逐滴加到氢氧化钡溶液中(如图),发现一直无明显现象,突然想起忘记加无色酚酞试液,为探究反应的进程,过程如下:(已知BaCl2溶液呈中性)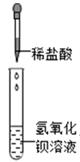
【建立猜想】①氢氧化钡过量 ②盐酸过量 ③ 两者恰好完全反应
【实验设计】
步骤一:取少量反应后的溶液于试管中,滴入几滴无色酚酞试液,溶液不变色,得出猜想①错误。
步骤二:继续探究
实验方案
实验操作
实验现象
实验结论
Ⅰ
重新取样,滴加少量AgNO3溶液
白色沉淀
猜想②正确
Ⅱ
重新取样,滴加足量Na2CO3溶液
________
猜想②正确
白色沉淀
猜想③正确
(1)、你是否认同方案Ⅰ的结论,并说明理由;(2)、表格空白处的实验现象是:;(3)、【表达交流】为确定猜想②是否正确,还可以选择的试剂有。A.紫色石蕊试液
B.二氧化碳
C.镁条
四、解答题
-
22. 向一含有盐酸的氯化铁溶液边振荡边逐滴滴加氢氧化钠溶液,且至过量,某同学了如图,要表明反应过程中,溶液总质量与滴入氢氧化钠溶液质量的关系。

请看图分析:
(1)、b点对应的溶液中,溶质化学式为;(2)、图中部分线段有误,请在答题卡的图中,重新画出溶液溶质总质量与滴入氢氧化钠的溶液质量变化关系曲线(要求标出abc折线点)23. 某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。
实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:
(1)、先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;(2)、过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。请描述小气球形状的变化情况,并对此作出合理的解释。