2021年初中科学中考一轮复习-水和溶液
试卷更新日期:2021-03-31 类型:一轮复习
一、单选题
-
1. mg硝酸钾的不饱和溶液,恒温蒸发水分,直到有少量晶体析出.在此变化过程中,溶液溶质质量分数(a%)与时间(t)的变化关系可用图( )A、
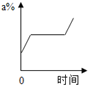 B、
B、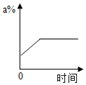 C、
C、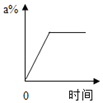 D、
D、 2. 在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度,下列说法正确的是( )A、溶剂质量不变 B、溶质质量增加 C、溶解度变小 D、溶液中溶质质量分数不变3. 相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( )A、Na2O B、NaOH C、CuSO4·5H2O D、H2SO44. 温州苍南有“世界矾都”之称,迄今有600多年的炼矾历史。制取的明矾可用于净水,也可用于制备发酵粉、油漆等,其制作流程为:煅烧明矾石→加水溶解→蒸发浓缩→析出结晶物→……如图是明矾制作过程中的结晶环节,能作为判断结晶池中液体为饱和溶液的依据是( )
2. 在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度,下列说法正确的是( )A、溶剂质量不变 B、溶质质量增加 C、溶解度变小 D、溶液中溶质质量分数不变3. 相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( )A、Na2O B、NaOH C、CuSO4·5H2O D、H2SO44. 温州苍南有“世界矾都”之称,迄今有600多年的炼矾历史。制取的明矾可用于净水,也可用于制备发酵粉、油漆等,其制作流程为:煅烧明矾石→加水溶解→蒸发浓缩→析出结晶物→……如图是明矾制作过程中的结晶环节,能作为判断结晶池中液体为饱和溶液的依据是( ) A、溶液澄清透明 B、溶液均一稳定 C、溶液浓度较大 D、池底晶体析出5. 20℃时,有质量分数为5%的食盐溶液A和质量分数为26.47%的食盐溶液B,下列有关A、B两种食盐溶液的判断正确的是( )A、向m g溶液B中加入x g食盐,振荡后,溶液的质量不变,则食盐在20℃时的溶解度为36 B、等质量的A,B中,溶剂质量:B>A C、m g溶液B中的溶质质量为 g D、向m g溶液A中加入x g食盐,振荡后,溶液的质量大于m g6. 如图甲、乙是电解水的实验及电解时水分子分解的微观示意图。有关叙述正确的是( )
A、溶液澄清透明 B、溶液均一稳定 C、溶液浓度较大 D、池底晶体析出5. 20℃时,有质量分数为5%的食盐溶液A和质量分数为26.47%的食盐溶液B,下列有关A、B两种食盐溶液的判断正确的是( )A、向m g溶液B中加入x g食盐,振荡后,溶液的质量不变,则食盐在20℃时的溶解度为36 B、等质量的A,B中,溶剂质量:B>A C、m g溶液B中的溶质质量为 g D、向m g溶液A中加入x g食盐,振荡后,溶液的质量大于m g6. 如图甲、乙是电解水的实验及电解时水分子分解的微观示意图。有关叙述正确的是( ) A、a试管中产生的气体是氧气 B、a、b试管中产生气体的质量比为2∶1 C、水电解的过程中,氢原子数和氧原子数都没发生变化 D、电解水的变化只是分子间的空隙发生了变化7. 某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是( )
A、a试管中产生的气体是氧气 B、a、b试管中产生气体的质量比为2∶1 C、水电解的过程中,氢原子数和氧原子数都没发生变化 D、电解水的变化只是分子间的空隙发生了变化7. 某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是( ) A、②中溶液是饱和溶液 B、③中溶液一定是不饱和溶液 C、②③中溶液的溶质质量分数不相同 D、③中溶液的溶质质量大于②中溶液的溶质质量8. 宁波是具有丰富水资源的美丽城市,下列措施不符合建设生态宁波理念的是( )
A、②中溶液是饱和溶液 B、③中溶液一定是不饱和溶液 C、②③中溶液的溶质质量分数不相同 D、③中溶液的溶质质量大于②中溶液的溶质质量8. 宁波是具有丰富水资源的美丽城市,下列措施不符合建设生态宁波理念的是( )①积极推进建设农村生活污水处理系统
②在水源保护区大规模建设宾馆、山庄
③允许向各江河中排放泥浆水
④严禁停靠在姚江、奉化江的运煤、运油船舶将清洗船舱的水直接排入海中
⑤完全禁止海洋捕捞和湖、河养殖
A、①②③ B、②③④ C、②③⑤ D、③④⑤9. 小兰通过预习知道,电解水时生成氢气与氧气的体积比为2∶1,但实验所得数据是氢气与氧气体积比略大于2∶1。针对这一发现,你认为下列做法中不可取的是( )A、反复多次实验查找原因 B、实验所得数据和理论值差不多,可以认为实验已成功 C、大胆提出假设:氧气比氢气易溶于水 D、查找实验装置是否漏气10. 如图为电解水过程的微观示意图,下列说法不正确的是( ) A、氧分子是由氧原子构成的,氢分子是由氢原子构成的 B、这个微观示意图说明了水分子是由氧原子和氢原子构成的 C、这个微观示意图可以解释为什么获得的氢气体积是氧气体积的两倍 D、该实验证明了水中含有氢气和氧气11. 电解水实验如图。下列说法正确的是( )
A、氧分子是由氧原子构成的,氢分子是由氢原子构成的 B、这个微观示意图说明了水分子是由氧原子和氢原子构成的 C、这个微观示意图可以解释为什么获得的氢气体积是氧气体积的两倍 D、该实验证明了水中含有氢气和氧气11. 电解水实验如图。下列说法正确的是( )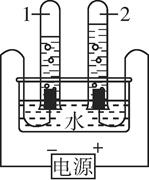 A、试管2中得到氢气 B、水电解得到氢气和氧气,所以水和氢气、氧气的性质完全相同 C、该实验说明水是由氢气和氧气组成的 D、可用带火星的木条检验生成的氧气12. 中学生所穿的校服都是用化纤面料做成的,如果不小心沾上了油漆,在不弄坏衣服的前提下把衣服洗干净,请你根据表中的知识选用一种溶剂来进行洗涤( )
A、试管2中得到氢气 B、水电解得到氢气和氧气,所以水和氢气、氧气的性质完全相同 C、该实验说明水是由氢气和氧气组成的 D、可用带火星的木条检验生成的氧气12. 中学生所穿的校服都是用化纤面料做成的,如果不小心沾上了油漆,在不弄坏衣服的前提下把衣服洗干净,请你根据表中的知识选用一种溶剂来进行洗涤( )溶剂
对油漆
对化纤
甲
能溶解
能溶解
乙
能溶解
不能溶解
丙
不能溶解
能溶解
丁
不能溶解
不能溶解
A、甲 B、乙 C、丙 D、丁二、填空题
-
13. 在温度不变的条件下,将100gA物质溶液蒸发掉10g水,有4g品体析出,再蒸发掉10g水,又有5g晶体析出。A物质在该温度时的溶解度为g,若再恒温蒸发10g水,则又有g晶体析出。14. 碘是一种紫黑色晶体,可以溶解在汽油中,形成紫红色溶液。
 (1)、碘的汽油溶液中,溶质是 , 溶剂是。(2)、甲、乙、丙三个同学分别画出如图所示的示意图来表示溶液中碘分子的分布(汽油分子没有画出)。根据你在实验中观察到的现象,(选填“甲”“乙”或“丙”)的示意图符合事实,你的依据是。15. 某兴趣小组为了研究硝酸钾(KNO3)的溶解和结晶,做了下列实验(室温下),其过程如下:
(1)、碘的汽油溶液中,溶质是 , 溶剂是。(2)、甲、乙、丙三个同学分别画出如图所示的示意图来表示溶液中碘分子的分布(汽油分子没有画出)。根据你在实验中观察到的现象,(选填“甲”“乙”或“丙”)的示意图符合事实,你的依据是。15. 某兴趣小组为了研究硝酸钾(KNO3)的溶解和结晶,做了下列实验(室温下),其过程如下: (1)、①中溶质的质量分数为。(2)、实验过程中一定属于饱和溶液的是(填序号)。16. 根据电解水的实验,回答下列问题:
(1)、①中溶质的质量分数为。(2)、实验过程中一定属于饱和溶液的是(填序号)。16. 根据电解水的实验,回答下列问题: (1)、从宏观上观察:如图所示,试管a和b中产生气体的体积比约为 , b中产生的气体是。(2)、在实验室中用自来水制取净化程度较高的水的方法是。(3)、水是生命之源,我国水资源总量虽位居世界第六位,但人均水量很少。请你写出一条节约用水的方法:。17. 制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制50g质量分数为10%的氢氧化钠溶液。(1)、若用氢氧化钠固体配制,需称量氢氧化钠的质量为g。(2)、用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要。(3)、下列操作正确的是____(填字母)。A、称量氢氧化钠固体时,左盘放砝码 B、在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体 C、将准确称量的氢氧化钠固体放入装有水的量筒中溶解 D、将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签(4)、若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为g;配制时应选用mL(选填“10”或“50”)的量筒量取水。
(1)、从宏观上观察:如图所示,试管a和b中产生气体的体积比约为 , b中产生的气体是。(2)、在实验室中用自来水制取净化程度较高的水的方法是。(3)、水是生命之源,我国水资源总量虽位居世界第六位,但人均水量很少。请你写出一条节约用水的方法:。17. 制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制50g质量分数为10%的氢氧化钠溶液。(1)、若用氢氧化钠固体配制,需称量氢氧化钠的质量为g。(2)、用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要。(3)、下列操作正确的是____(填字母)。A、称量氢氧化钠固体时,左盘放砝码 B、在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体 C、将准确称量的氢氧化钠固体放入装有水的量筒中溶解 D、将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签(4)、若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为g;配制时应选用mL(选填“10”或“50”)的量筒量取水。三、实验探究题
-
18. 如图甲所示为小乐配制100克溶质的质量分数为12%的氯化钠溶液的部分操作(其中托盘天平的砝码盒中质量最小的砝码为10克),回答问题:
 (1)、图甲所示的部分操作,先后顺序是(填写序号)。(2)、在图甲①所示的操作中,应先调节天平平衡,然后在左、右托盘各放一张质量相等的称量纸,接下来的操作是。(3)、在图甲③所示的操作中,小乐在用量筒量取水的过程中,若采取了图乙方式读取水的体积,则此操作将导致所配制的氯化钠溶液的溶质质量分数(选填“>”或“<”)12%。19. 小乐用电解水的实验探究水的组成,回答问题:
(1)、图甲所示的部分操作,先后顺序是(填写序号)。(2)、在图甲①所示的操作中,应先调节天平平衡,然后在左、右托盘各放一张质量相等的称量纸,接下来的操作是。(3)、在图甲③所示的操作中,小乐在用量筒量取水的过程中,若采取了图乙方式读取水的体积,则此操作将导致所配制的氯化钠溶液的溶质质量分数(选填“>”或“<”)12%。19. 小乐用电解水的实验探究水的组成,回答问题: (1)、图甲是电解水的实验装置,在水电解器的玻璃管里注满水后,接通(选填“直流电”或“交流电”);等a、b玻璃管内收集到一定体积的气体后关闭电源。若要检验b玻璃管中的气体,其操作是。(2)、图乙是电解水的微观示意图,其中①②③的正确的顺序是。(3)、查阅资料得知“同温同压下,气体的体积比等于气体的分子个数比”。则该实验中能够说明“水分子中氢、氧原子个数比为2∶1”的实验现象是。20. 如表是氯化钠、氯化铵在不同温度时的溶解度。
(1)、图甲是电解水的实验装置,在水电解器的玻璃管里注满水后,接通(选填“直流电”或“交流电”);等a、b玻璃管内收集到一定体积的气体后关闭电源。若要检验b玻璃管中的气体,其操作是。(2)、图乙是电解水的微观示意图,其中①②③的正确的顺序是。(3)、查阅资料得知“同温同压下,气体的体积比等于气体的分子个数比”。则该实验中能够说明“水分子中氢、氧原子个数比为2∶1”的实验现象是。20. 如表是氯化钠、氯化铵在不同温度时的溶解度。温度(℃)
0
20
40
60
80
溶解度(g)
氯化钠
35.7
36.0
36.6
37.3
38.4
氯化铵
29.4
37.2
45.8
55.2
65.6
(1)、以上两种物质的溶解度受温度影响较大的是。(2)、40℃时,将40.6g氯化钠加到100g水中,充分搅拌使之溶解,所得溶液的质量为。(3)、20℃时,氯化钠饱和溶液的溶质质量分数为(精确到小数点后1位)。21. 某同学配制50g 6%的氯化钠溶液,整个操作过程如图所示,请回答下列问题: (1)、配制溶液的正确操作顺序为(填序号,下同),其中操作有误的是。(2)、图②中盛放氯化钠固体的仪器名称是 , 需称取氯化钠g。(3)、量水时选用的量筒量程最合适的是(填字母),读数时视线要与量筒内保持水平。
(1)、配制溶液的正确操作顺序为(填序号,下同),其中操作有误的是。(2)、图②中盛放氯化钠固体的仪器名称是 , 需称取氯化钠g。(3)、量水时选用的量筒量程最合适的是(填字母),读数时视线要与量筒内保持水平。A.10mL B.25mL
C.50mL D.100mL
(4)、经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是____(填字母)。A、氯化钠固体不纯 B、用生锈砝码称量 C、装瓶时有少量溶液洒出 D、溶解时烧杯内壁有水珠22. 仔细阅读下面的探究实验信息,回答相关问题。Ⅰ.【实验目的】探究溶解过程中,溶液温度的变化情况。
Ⅱ.【查阅资料】
①物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
②实验条件下,水的凝固点为0℃、沸点为100℃。
Ⅲ.【提出猜想】物质溶解过程中,溶液的温度或升高,或降低,或不变。
Ⅳ.【实验探究】某探究小组的同学设计了如图所示的两种方案。在如图乙所示方案中,每次加入物质b之前均使用温度计测量热水温度,使之保持在99℃。
 (1)、Ⅴ.【实验结论】
(1)、Ⅴ.【实验结论】图甲所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度(选填“升高”“降低”或“不变”,下同)。
(2)、图乙所示实验中,若加入物质b后,热水会突然沸腾,说明溶液的温度。(3)、Ⅵ.【拓展实验】按照图丙所示进行实验。若物质c为氢氧化钠,则U形管内的左边液面将(选填“高于”“低于”或“等于”)右边液面;若U形管内的液面位置变化与之相反,则物质c为(填序号)。
①氧化钙 ②硝酸铵 ③氯化钠
(4)、Ⅶ.【反思交流】该小组的同学进一步就物质溶解过程中溶液温度变化的原因展开了讨论,分析得出:若Q吸Q放(选填“>”“<”或“=”,下同),则溶液温度升高;若Q吸与Q放的相对大小与之相反,则溶液温度降低;若Q吸Q放 , 则溶液温度不变。
(5)、在图乙所示方案中,小张同学对实验现象很感兴趣,他继续向热水中加入相同质量的物质b,又看到沸腾现象,至烧杯中出现固体物质后,再继续加入相同质量的物质b,就看不到沸腾现象。请解释不再产生沸腾现象的原因:。四、解答题
-
23. 现有硝酸钾(KNO3)和氯化钠(NaCl)两种物质的溶解度数据如下表:
温度/℃
0
10
20
30
40
50
60
70
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
37.8
KNO3
13.3
20.9
31.6
45.8
45.8
85.5
110
138
(1)、20℃时,能否制得溶质质量分数为30%的氯化钠溶液?请计算后说明。(2)、人们把海水引入盐田,风吹日晒后,食盐就会结晶析出。这种从溶液中得到体的方法叫(填“蒸发溶剂”或“冷却热饱和溶液”)。(3)、有硝酸钾和氯化钠的饱和溶液各一杯,它们的温度、溶质质量分数都相同,则由表可知这两杯溶液的温度的最小范围是。24. 如图所示的两个实验都能验证水的组成。 (1)、图甲所示实验中,观察到的现象是。(2)、图乙所示实验中,接通直流电源一段时间后,玻璃管b内产生的气体是 , 该管内产生约10mL气体时,玻璃管a内产生约mL气体。(3)、若取36g质量分数为1%的硫酸钠溶液进行电解,消耗了6g水,则电解后硫酸钠溶液中溶质的质量分数为是多少?
(1)、图甲所示实验中,观察到的现象是。(2)、图乙所示实验中,接通直流电源一段时间后,玻璃管b内产生的气体是 , 该管内产生约10mL气体时,玻璃管a内产生约mL气体。(3)、若取36g质量分数为1%的硫酸钠溶液进行电解,消耗了6g水,则电解后硫酸钠溶液中溶质的质量分数为是多少?