2021年初中科学中考一轮复习-构成物质的微粒及元素
试卷更新日期:2021-03-31 类型:一轮复习
一、单选题
-
1. 2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C18 , 这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个( )A、 原子 B、质子 C、中子 D、电子2. 如图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
 A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子中b与c的数目一定相同 D、原子中a与c的数目一定相同3. 如图是某个化学反应前后的微观模拟图,请根据图示判断参加反应的
A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子中b与c的数目一定相同 D、原子中a与c的数目一定相同3. 如图是某个化学反应前后的微观模拟图,请根据图示判断参加反应的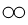 和
和 与反应后生成的
与反应后生成的 个数比是( )
个数比是( )
 A、5∶1∶2 B、1∶2∶2 C、1∶1∶1 D、2∶3∶14. 如图是一定量的 B2 和 AB 在一定条件下混合以及混合结果的模型,则( )
A、5∶1∶2 B、1∶2∶2 C、1∶1∶1 D、2∶3∶14. 如图是一定量的 B2 和 AB 在一定条件下混合以及混合结果的模型,则( ) A、反应得到的生成物有两种 B、反应前后元素化合价不变 C、该反应为化合反应 D、参加反应的两种分子个数比为 3∶25. 知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c相对应的是( )
A、反应得到的生成物有两种 B、反应前后元素化合价不变 C、该反应为化合反应 D、参加反应的两种分子个数比为 3∶25. 知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c相对应的是( ) A、原子、原子核、核外电子 B、原子核、原子、核外电子 C、原子、核外电子、原子核 D、核外电子、原子核、原子6. 我国著名科学家张青莲教授主持测定了铕等9种原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( )A、63 B、89 C、152 D、2157. 具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子,聚变发生后,氘、氚原子核转变为氦原子核。根据以上叙述,下列说法正确的是( )A、氘和氘与氢的原子序数不同 B、氘原子和氚原子是氢的不同元素 C、氘原子和氚原子是氢的两种同位素 D、氘原子和氚原子的相对原子质量相同8. “○”表示氧原子,用“●”表示氢原子,能保持水的化学性质的粒子是( )A、
A、原子、原子核、核外电子 B、原子核、原子、核外电子 C、原子、核外电子、原子核 D、核外电子、原子核、原子6. 我国著名科学家张青莲教授主持测定了铕等9种原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( )A、63 B、89 C、152 D、2157. 具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子,聚变发生后,氘、氚原子核转变为氦原子核。根据以上叙述,下列说法正确的是( )A、氘和氘与氢的原子序数不同 B、氘原子和氚原子是氢的不同元素 C、氘原子和氚原子是氢的两种同位素 D、氘原子和氚原子的相对原子质量相同8. “○”表示氧原子,用“●”表示氢原子,能保持水的化学性质的粒子是( )A、 B、
B、 C、
C、 D、
D、 9. 如下图是4位同学对分子原子和离子的描述,其中正确的是( )A、
9. 如下图是4位同学对分子原子和离子的描述,其中正确的是( )A、 B、
B、 C、
C、 D、
D、 10. 俄国科学家门捷列夫对元素周期表的编制作出巨大献,人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的核外电子数为( )A、101 B、157 C、258 D、35911. 2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个( )A、 原子 B、质子 C、中子 D、电子
10. 俄国科学家门捷列夫对元素周期表的编制作出巨大献,人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的核外电子数为( )A、101 B、157 C、258 D、35911. 2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个( )A、 原子 B、质子 C、中子 D、电子二、填空题
-
12. 将相应的序号填入下列空格:①原子;②分子;③元素。(1)、蒸馏水不宜养鱼,因为蒸馏水中几乎不含氧。(2)、市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等,这里的“钙”“锌”“碘”是指。(3)、多吃海带可预防“大脖子病”,是因为海带中含有丰富的碘。(4)、碳元素是所有质子数为6的碳的总称。13. 月球上的23He蕴藏量巨大,地球上的氦元素主要以24He形式存在。从原子的构成来看,23He、24He两种原子的数不同,化学性质基本相同,互称为原子。14. 氟利昂是一种常见的制冷剂。氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如下:
 (1)、请写出臭氧的化学式;臭氧与氧气化学性质不同的原因是。(2)、一个过氧化氯(Cl2O2)分子是由构成的;一个一氧化氯(ClO)分子是由构成的,它们的化学性质(选填“相同”或“不同”),因为。15. 用高能粒子轰击原子核是研究微观粒子的一种方法。
(1)、请写出臭氧的化学式;臭氧与氧气化学性质不同的原因是。(2)、一个过氧化氯(Cl2O2)分子是由构成的;一个一氧化氯(ClO)分子是由构成的,它们的化学性质(选填“相同”或“不同”),因为。15. 用高能粒子轰击原子核是研究微观粒子的一种方法。1934年,意大利科学家费米用中子轰击铀原子(质子数为92,元素符号为U),得到了一种质量增加的原子,他公开宣布发现了93号元素,被科学界认可,从而获得了诺贝尔物理学奖。
1938年,德国科学家哈恩在重复费米的实验后,发现费米实验中得到的是56号钡元素,并用图示模型来定义这一变化。费米知道后,立即重复哈恩的实验,结果证实自己错了,费米坦率地检讨并纠正了错误。
 (1)、费米用中子轰击铀原子,不可能增加铀原子的数,所以得不到93号元素。(2)、结合材料分析,以下观点正确的是 。A、面对前人的观点要敢于质疑 B、科学结论的得出要依据客观事实 C、对科学的认识是一个不断修正、完善的过程16. 人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金属箔。实验发现:多数α粒子穿过金属箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。(1)、卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的 ;(2)、当α粒子轰击金属箔时,图中四条运动轨迹不可能出现的是(填字母)。
(1)、费米用中子轰击铀原子,不可能增加铀原子的数,所以得不到93号元素。(2)、结合材料分析,以下观点正确的是 。A、面对前人的观点要敢于质疑 B、科学结论的得出要依据客观事实 C、对科学的认识是一个不断修正、完善的过程16. 人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金属箔。实验发现:多数α粒子穿过金属箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。(1)、卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的 ;(2)、当α粒子轰击金属箔时,图中四条运动轨迹不可能出现的是(填字母)。 17. 对原子结构模型的形成,汤姆生、卢瑟福和玻尔等科学家做出了突出贡献。请根据所学完成下列有关问题。
17. 对原子结构模型的形成,汤姆生、卢瑟福和玻尔等科学家做出了突出贡献。请根据所学完成下列有关问题。 (1)、汤姆生发现了原子中存在一种带负电荷的粒子,证明了原子是可以再分的。汤姆生发现的粒子是。(2)、1911年,卢瑟福等人进行了α粒子(α粒子是带两个单位正电荷的氦原子核)散射实验,为建立现代原子理论打下了基础。 如图a、b、c、d四条线中,不可能是α粒子在该实验中的运动轨迹的是。(3)、从原子结构模型建立的过程中,我们发现 。(可多选)A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、玻尔原子模型的建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质
(1)、汤姆生发现了原子中存在一种带负电荷的粒子,证明了原子是可以再分的。汤姆生发现的粒子是。(2)、1911年,卢瑟福等人进行了α粒子(α粒子是带两个单位正电荷的氦原子核)散射实验,为建立现代原子理论打下了基础。 如图a、b、c、d四条线中,不可能是α粒子在该实验中的运动轨迹的是。(3)、从原子结构模型建立的过程中,我们发现 。(可多选)A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、玻尔原子模型的建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质三、实验探究题
-
18. 人类对原子结构的认识永无止境。请根据所学知识回答:(1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均 (填“正确”或“错误”)。
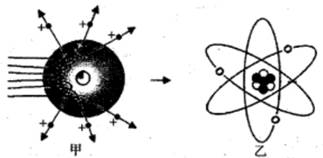 (2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。
(2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。四、解答题
-
19. H、 H、 H分别表示氢元素的三种原子,其上、下标的意义如图所示。 H、 H、 H可简写成1H、2H、3H。
 (1)、1H、2H、3H三种原子中,数目不等(选填“质子”或“中子”或“电子”);(2)、相同分子数的2H2和3H2分别与足量O2反应全部转化成H2O,生成的质量前者(选填“大于”或“等于"或“小于”)后者。20. 伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是:一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
(1)、1H、2H、3H三种原子中,数目不等(选填“质子”或“中子”或“电子”);(2)、相同分子数的2H2和3H2分别与足量O2反应全部转化成H2O,生成的质量前者(选填“大于”或“等于"或“小于”)后者。20. 伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是:一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆森通过实验发现了电子,进一步发展了原子、分子论。汤姆森主要是纠正了“道尔顿原子论”中的观点。
1911年,卢瑟福又通过实验,推测原子是由和核外电子构成,并提出了沿用至今的现代原子结构理论。
(2)、道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样,对实验现象进行解释的过程叫做。原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了来表达他们的理论成果。
-