天津市红桥区2020年中考化学二模试卷
试卷更新日期:2021-03-17 类型:中考模拟
一、单选题
-
1. 每年的6月5日是世界环境日,环境保护是我国的一项基本国策,下列做法不利于环境保护的是( )A、大力兴建火力发电厂 B、合理开采矿石 C、用布袋代替塑料袋购物 D、乘坐公交车出行2. 下列物质溶于水,充分搅拌后,能得到溶液的是( )A、植物油 B、碘 C、高锰酸钾 D、面粉3. 分类是学习和研究化学常用的方法。下列物质分类正确的是( )A、微量元素:Fe、I、Zn B、氧化物:Fe2O3、Mg(OH)2、CaCO3 C、合金:生铁、焊锡、黄金 D、合成材料:棉花、蚕丝、聚乙烯4. 规范实验操作是实验成功的基础和关键。下列实验基本操作正确的是( )A、
 B、
B、 C、
C、 D、
D、 5. 强化安全意识,提升安全素养。下列采取的安全措施错误的是( )A、进入溶洞探险先做灯火实验 B、在火灾逃生时用湿毛巾捂住口鼻 C、在面粉厂张贴严禁烟火标志 D、厨房内煤气泄漏立即打开排气扇6. 下列实验现象描述正确的是( )A、硫在氧气中燃烧:安静的燃烧,发出淡蓝色火焰,放出热量 B、木炭在空气中燃烧生成二氧化碳 C、铁丝伸入盛有氧气的集气瓶中,火星四射,生成黑色固体 D、镁条在空气中燃烧时,发出耀眼白光,生成白色固体7. 如图是元素X的一种粒子结构示意图,下列说法正确的是( )
5. 强化安全意识,提升安全素养。下列采取的安全措施错误的是( )A、进入溶洞探险先做灯火实验 B、在火灾逃生时用湿毛巾捂住口鼻 C、在面粉厂张贴严禁烟火标志 D、厨房内煤气泄漏立即打开排气扇6. 下列实验现象描述正确的是( )A、硫在氧气中燃烧:安静的燃烧,发出淡蓝色火焰,放出热量 B、木炭在空气中燃烧生成二氧化碳 C、铁丝伸入盛有氧气的集气瓶中,火星四射,生成黑色固体 D、镁条在空气中燃烧时,发出耀眼白光,生成白色固体7. 如图是元素X的一种粒子结构示意图,下列说法正确的是( ) A、X是金属元素 B、该粒子最外电子层已达到稳定结构 C、该粒子的核电荷数为18 D、该粒子可表示为X +8. 下列有关燃烧和灭火的说法中,错误的是( )A、用水来灭火,是因为降低了可燃物的着火点 B、油锅着火时可用锅盖盖灭,是因为隔绝了空气 C、山林中开辟的隔离带可以控制火势蔓延,是因为隔离了可燃物 D、木炭在氧气中燃烧比在空气中燃烧更剧烈,是因为氧气浓度不同9. 有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强弱的顺序正确的是( )A、X、Y、Z B、X、Z、Y C、Y、Z、X D、Z、Y、X10. 已知A+3B=2C+3D中,已知23gA与48gB恰好完全反应生成44gC,又知D的相对分子质量为18,则A的相对分子质量为( )A、44 B、32 C、23 D、4611. 下列有关化学基本概念说法正确的是( )
A、X是金属元素 B、该粒子最外电子层已达到稳定结构 C、该粒子的核电荷数为18 D、该粒子可表示为X +8. 下列有关燃烧和灭火的说法中,错误的是( )A、用水来灭火,是因为降低了可燃物的着火点 B、油锅着火时可用锅盖盖灭,是因为隔绝了空气 C、山林中开辟的隔离带可以控制火势蔓延,是因为隔离了可燃物 D、木炭在氧气中燃烧比在空气中燃烧更剧烈,是因为氧气浓度不同9. 有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强弱的顺序正确的是( )A、X、Y、Z B、X、Z、Y C、Y、Z、X D、Z、Y、X10. 已知A+3B=2C+3D中,已知23gA与48gB恰好完全反应生成44gC,又知D的相对分子质量为18,则A的相对分子质量为( )A、44 B、32 C、23 D、4611. 下列有关化学基本概念说法正确的是( )①分子是构成物质的一种微粒②原子也是构成物质的一种微粒③在化学反应中,分子、原子都可分④具有相同质子数的粒子一定是同种元素⑤同种元素组成的物质一定是单质⑥二氧化碳由碳原子和氧分子构成⑦石蜡燃烧的过程中既有物理变化又有化学变化⑧由同种分子构成的物质一定是纯净物
A、①②③④ B、①②⑤⑦ C、①②④⑧ D、①②⑦⑧12. 甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应下列符合对应反应关系的选项是( )
选项
A
B
C
D
物质
甲
C
HCl
Ca(OH)2
Fe
乙
CO
Ca(OH)2
Na2CO3
HCl
丙
CuO
NaOH
H2SO4
CuSO4
丁
O2
CO2
Ba(NO3)2
NaOH
A、A B、B C、C D、D13. 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),该反应过程的微观示意图如下。下列说法正确的是( )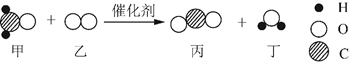 A、物质甲为甲醛,其分子由碳原子和水分子构成 B、物质乙中氧元素的化合价为-2价 C、该反应前后原子种类和数目均发生改变 D、该反应消耗物质甲和生成物质丁的质量比为5﹕314. 将10g氧化铜粉末加入到100g一定质量分数的稀硫酸中,微热到氧化铜全部溶解,再向溶液中加入ag铁粉,使溶液中的溶质完全反应后,过滤,将滤渣在低温下烘干,得到干燥固体质量仍然为ag,下列分析错误的是( )A、稀硫酸中溶质质量分数为14% B、滤渣中一定只含有铜 C、加入铁粉后有红色固体产生,还有少量气泡产生 D、a的取值范围:a>8
A、物质甲为甲醛,其分子由碳原子和水分子构成 B、物质乙中氧元素的化合价为-2价 C、该反应前后原子种类和数目均发生改变 D、该反应消耗物质甲和生成物质丁的质量比为5﹕314. 将10g氧化铜粉末加入到100g一定质量分数的稀硫酸中,微热到氧化铜全部溶解,再向溶液中加入ag铁粉,使溶液中的溶质完全反应后,过滤,将滤渣在低温下烘干,得到干燥固体质量仍然为ag,下列分析错误的是( )A、稀硫酸中溶质质量分数为14% B、滤渣中一定只含有铜 C、加入铁粉后有红色固体产生,还有少量气泡产生 D、a的取值范围:a>8二、多选题
-
15. 下列有关物质鉴别方案正确的一组是( )A、敞口放置的NaOH溶液,可通过加入酚酞溶液,鉴别其是否变质 B、MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别 C、Na2CO3溶液、KNO3溶液、盐酸、NaCl溶液,不加任何试剂即可鉴别 D、CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂即可鉴别
三、填空题
-
16. 有下列物质:①氮气②甲烷③干冰④食盐⑤碳酸氢钠⑥聚乙烯。请按要求将相应物质的序号填写在题中的空白处。(1)、常用于防腐、调味用的盐是。(2)、能进行人工降雨的物质是。(3)、可以制成食品包装袋的物质是。(4)、用于烤制糕点的发酵粉的是。(5)、焊接金属时常用作保护气的物质是。(6)、最简单的有机化合物是。17. 根据下列图示,回答问题。
 (1)、氟元素的相对原子质量为;D中的x是。(2)、①和②是不同种元素,它们的最本质的区别是。(3)、A,B,C,D结构示意图中,属于同种元素的粒子是(填序号)(4)、A粒子的化学性质与B,C,D中(填序号)粒子的化学性质相似。18. 化学与生产、生活息息相关,请运用化学知识回答下列问题:(1)、下列物质属于合成材料的是(填字母)
(1)、氟元素的相对原子质量为;D中的x是。(2)、①和②是不同种元素,它们的最本质的区别是。(3)、A,B,C,D结构示意图中,属于同种元素的粒子是(填序号)(4)、A粒子的化学性质与B,C,D中(填序号)粒子的化学性质相似。18. 化学与生产、生活息息相关,请运用化学知识回答下列问题:(1)、下列物质属于合成材料的是(填字母)A 聚乙烯B 棉花C 合成橡胶D 桑蚕丝
(2)、有些村庄需打深井取用地下水,可用区分地下水是软水还是硬水,生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是。(3)、提倡少用煤、、天然气三大化石燃料,有利于改善空气质量。(4)、新冠肺炎疫情期间,84消毒液是常见的消毒剂。①84消毒液和洁厕灵混合使用时会发生化学反应2 HCl+NaClO= NaCl+H2O+X,X气体有毒,因此二者不能混合使用。那么X的化学式为。
②教室喷洒过消毒液后,室内充满消毒液气味,说明分子具有的特性为。
(5)、熟石灰在生产生活中用途广泛,既可以与(填化学式)按一定比例符合制备波尔多液,又可以用来改良(填“酸性”、“中性”或“碱性”)土壤。(6)、铁是年产量最高的金属材料。某钢铁厂每天需消耗3500t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是t。19. 写出下列反应的化学方程式:(1)、铝与氧气反应。(2)、氯酸钾制取氧气。(3)、小苏打治疗胃酸过多。20. 甲、乙、丙三种固体(均不含结晶水)的溶解度曲线如图所示。 (1)、20℃时,三种物质的溶解度由大到小依次为。(2)、30℃时,甲和乙的饱和溶液各100g两种溶液中溶剂质量的大小关系:为甲乙填(<、>、=)。(3)、甲中含有少量的乙,提纯甲的方法是。(4)、甲、乙、丙中的某一种固体进行如下所示的实验。
(1)、20℃时,三种物质的溶解度由大到小依次为。(2)、30℃时,甲和乙的饱和溶液各100g两种溶液中溶剂质量的大小关系:为甲乙填(<、>、=)。(3)、甲中含有少量的乙,提纯甲的方法是。(4)、甲、乙、丙中的某一种固体进行如下所示的实验。
①溶液a的溶质质量分数是。(精确到0.1%)
②取用的固体是;温度t的范围是。
21. 甲、乙、丙、丁4种常见物质,由H、C、O、Na、Ca五种元素中的2~3种组成。(1)、甲是一种实验室常用的液体燃料(C2H5OH),它是一种(填“可再生”或“不可再生”)能源。请写出该液体燃料完全燃烧的化学方程式。(2)、①若乙是甲完全燃烧的产物之一,且乙为液体。丙是常见的干燥剂中的主要成分,二者反应放热,则丙的化学式为。②若乙是甲完全燃烧的另外一种产物,且乙为气体。丙和丁属于同类物质,乙和丙、乙和丁能相互转化,从丙和丁的固体混合物中提取丙的实验过程如图。

则操作a是先 , 后 , 乙转化成丁的化学方程式是。
四、实验题
-
22. 实验室常利用以下装置完成气体制备及性质实验,请回答:
 (1)、指出编号仪器的名称:① , ②。(2)、以上A装置有一处明显的不正确,请加以改正 , 利用改正后的装置继续完成后面的实验。(3)、欲使用高锰酸钾制取氧气,应选择的A装置,反应方程式为;为防止高锰酸钾粉末进入导管,应采取的措施是。(4)、工业上常需分离CO、CO2的混合气体,某同学采用装置F也能达到分离该混合气体的目的,操作步骤如下:
(1)、指出编号仪器的名称:① , ②。(2)、以上A装置有一处明显的不正确,请加以改正 , 利用改正后的装置继续完成后面的实验。(3)、欲使用高锰酸钾制取氧气,应选择的A装置,反应方程式为;为防止高锰酸钾粉末进入导管,应采取的措施是。(4)、工业上常需分离CO、CO2的混合气体,某同学采用装置F也能达到分离该混合气体的目的,操作步骤如下:①关闭活塞b,打开活塞a,通入混合气体,可从导管c处收集到气体。
②然后,关闭活塞a,打开活塞b,又可收集到另一种气体,写出F中发生反应的化学方程式。
23. 溶液在日常生产生活及科学研究中具有广泛的用途,如图是配置溶质质量分数为10%的NaCl溶液的实验操作示意图: (1)、用图1中序号表示配制溶液的正确操作顺序;(2)、图③中玻璃棒的作用是 .(3)、称量NaCl时,天平平衡后的状态如图1中⑤所示,游码标尺示数如图2,则称取的NaCl质量为 g.(4)、NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的溶质质量分数(填“大于”、“小于”或“等于”)10%.(5)、医疗上常用0.9%的氯化钠溶液作为生理盐水.现要配制该生理盐水1000g,需要质量分数为12%的氯化钠溶液(密度约为1.09g/cm3) mL.(计算结果精确到0.1.
(1)、用图1中序号表示配制溶液的正确操作顺序;(2)、图③中玻璃棒的作用是 .(3)、称量NaCl时,天平平衡后的状态如图1中⑤所示,游码标尺示数如图2,则称取的NaCl质量为 g.(4)、NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的溶质质量分数(填“大于”、“小于”或“等于”)10%.(5)、医疗上常用0.9%的氯化钠溶液作为生理盐水.现要配制该生理盐水1000g,需要质量分数为12%的氯化钠溶液(密度约为1.09g/cm3) mL.(计算结果精确到0.1.五、流程题
-
24. 木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学实验小组设计回收铜的方案如下:
 (1)、过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和。(2)、反应①的化学方程式为。(3)、滤液I中的溶质名称为。(4)、试剂A可以选用下列溶液(填序号)。
(1)、过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和。(2)、反应①的化学方程式为。(3)、滤液I中的溶质名称为。(4)、试剂A可以选用下列溶液(填序号)。①H2SO4
②CuSO4
③MgSO4
(5)、为了完善实验方案,可对滤渣Ⅰ中的进行回收。六、计算题
-
25. 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca10(PO4)6(OH)2)形式存在,其相对分子质量为1004,牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。如图是某品牌纯牛奶包装上的部分文字说明,请认真阅读后回答下列问题:
 (1)、牛奶中富含的营养素为(填一种即可)。(2)、Ca10(PO4)6(OH)2由种元素组成。(3)、一盒牛奶含钙至少多少g?(精确到0.01)(4)、若人体每天至少需要0.6g钙,而这些钙有90%来自牛奶,则一个人每天要喝多少盒牛奶?26. 某氯化钠样品中含有少量的氯化钙,样品中钠元素和钙元素的质量比为23:20。取一定量的该样品,向其中加入适量的碳酸钠溶液(密度为1.1g/cm3)恰好完全反应,过滤,得到10g沉淀和112.8g滤液。请计算:(1)、原样品中氯化钙的质量(2)、所加入碳酸钠溶液的溶质质量分数。(3)、所加入碳酸钠溶液的体积。(计算结果精确到0.1)
(1)、牛奶中富含的营养素为(填一种即可)。(2)、Ca10(PO4)6(OH)2由种元素组成。(3)、一盒牛奶含钙至少多少g?(精确到0.01)(4)、若人体每天至少需要0.6g钙,而这些钙有90%来自牛奶,则一个人每天要喝多少盒牛奶?26. 某氯化钠样品中含有少量的氯化钙,样品中钠元素和钙元素的质量比为23:20。取一定量的该样品,向其中加入适量的碳酸钠溶液(密度为1.1g/cm3)恰好完全反应,过滤,得到10g沉淀和112.8g滤液。请计算:(1)、原样品中氯化钙的质量(2)、所加入碳酸钠溶液的溶质质量分数。(3)、所加入碳酸钠溶液的体积。(计算结果精确到0.1)
-
-