四川省南充市西充县义兴片区2019-2020学年九年级下学期化学第一次月考试卷
试卷更新日期:2021-03-15 类型:月考试卷
一、单选题
-
1. 关于钢的说法错误的是( )A、钢是纯净物 B、钢是铁的合金 C、钢的含碳量低于生铁 D、钢的性能优于生铁2. 20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
物质
甲
乙
丙
丁
未溶解固体的质量/g
4.2
2
0
9.2
下列说法正确的是( )
A、所得四杯溶液都是饱和溶液 B、丁溶液的溶质质量分数最大 C、20℃时四种物质溶解度的关系为:丙>乙>甲>丁 D、四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液3. 芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的.下面是生产单质硅过程中的一个重要反应:SiO2+2C Si+2CO↑,该反应的基本类型是()A、化合反应 B、分解反应 C、置换反应 D、复分解反应4. “金银铜铁锡”俗称五金,在这五种金属中,有一种金属与其他四种金属的盐溶液都能发生反应,这种金属是( )A、金 B、铜 C、铁 D、锡5. 如图所示,是甲、乙、丙三种固体物质的溶解度曲线.下列说法正确的是( )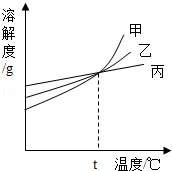 A、t℃时,甲、乙、丙三种物质的饱和溶液的质量分数相等 B、在两份相同质量的水中分别加入甲与丙,达到饱和时溶解甲的质量大于丙 C、相同温度时,甲、乙、丙三种饱和溶液,其质量分数关系为:甲>乙>丙 D、甲中混有少量丙时,可采用高温制成热的饱和溶液,再蒸发结晶提纯甲6. 下图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
A、t℃时,甲、乙、丙三种物质的饱和溶液的质量分数相等 B、在两份相同质量的水中分别加入甲与丙,达到饱和时溶解甲的质量大于丙 C、相同温度时,甲、乙、丙三种饱和溶液,其质量分数关系为:甲>乙>丙 D、甲中混有少量丙时,可采用高温制成热的饱和溶液,再蒸发结晶提纯甲6. 下图是A、B、C三种物质的溶解度曲线,下列分析错误的是( ) A、50℃时A,B,C三种物质的溶解度由大到小的顺序是A>B>C B、50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂的质量比为1:2 C、将C的饱和溶液变为不饱和溶液,采用降温的方法 D、将50℃时A,B,C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C7. 光亮的铁钉在下列几种情况下,最不容易生锈的是( )
A、50℃时A,B,C三种物质的溶解度由大到小的顺序是A>B>C B、50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂的质量比为1:2 C、将C的饱和溶液变为不饱和溶液,采用降温的方法 D、将50℃时A,B,C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C7. 光亮的铁钉在下列几种情况下,最不容易生锈的是( )
A、 B、
B、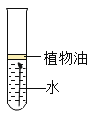 C、
C、 D、
D、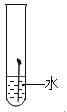 8. 硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,错误的是( )
8. 硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,错误的是( )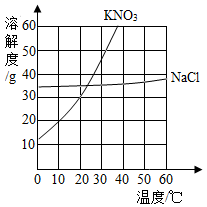 A、两种溶液中溶质的质量分数相等 B、通常情况下,采取降温的方法能将两种溶液都变成饱和溶液 C、若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10 D、若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小9. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A、两种溶液中溶质的质量分数相等 B、通常情况下,采取降温的方法能将两种溶液都变成饱和溶液 C、若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10 D、若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小9. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A、X、Y、Z B、Z、Y、X C、Y、X、Z D、X、Z、Y10. 往AgNO3和Cu( NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是( )A、滤渣中一定有Fe粉 B、滤渣中一定有Cu粉 C、滤渣中一定有Fe2+ D、滤渣中一定有Ag+、Cu2+二、填空题
-
11. 地壳中含量最高的金属元素是;人体中含量最多的金属元素是;熔点最低的金属是;目前世界上年产量最高的金属是。12. 金属在生成生活中应用广泛。(1)、最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管。下列管材中,属于金属材料的是(填字母序号,下同);
 (2)、铁生锈的条件是为了防止钢铁锈蚀,人们常用的方法(任写一种)来达到目的;(3)、金属的回收和利用是保护金属资源的一种有效途径,废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为;(4)、应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应
(2)、铁生锈的条件是为了防止钢铁锈蚀,人们常用的方法(任写一种)来达到目的;(3)、金属的回收和利用是保护金属资源的一种有效途径,废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为;(4)、应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应A Fe 和 CuSO4 溶液
B Mg 和 MnSO4 溶液
C Mn 和 FeSO4 溶液
①写出 Fe 和 CuSO4 溶液反应的化学方程式。
②Mn、Fe、Mg 、Cu 四种金属的活动性由强到弱的顺序。
13. 如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题: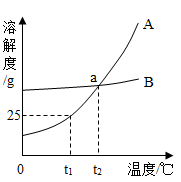 (1)、t1℃时,A物质的溶解度为g;(2)、a点的含义是;(3)、溶解度受温度影响小的物质是;(4)、从A、B的混合物中分离A物质,一般采用的方法.14. 下图是A、B的溶解度曲线。t2℃时分别将100gA、B的饱和溶液降温至t1℃,析出晶体质量AB(填“>”、“<”或“=”);把t2℃时150gA的饱和溶液稀释为20%,需加水g。
(1)、t1℃时,A物质的溶解度为g;(2)、a点的含义是;(3)、溶解度受温度影响小的物质是;(4)、从A、B的混合物中分离A物质,一般采用的方法.14. 下图是A、B的溶解度曲线。t2℃时分别将100gA、B的饱和溶液降温至t1℃,析出晶体质量AB(填“>”、“<”或“=”);把t2℃时150gA的饱和溶液稀释为20%,需加水g。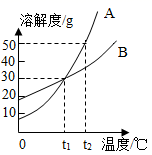 15. 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
15. 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题: (1)、t1℃时,A,B两种物质的溶解度是AB(填“>”、“<”或“=”,下同)。(2)、将t3℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是AB。
(1)、t1℃时,A,B两种物质的溶解度是AB(填“>”、“<”或“=”,下同)。(2)、将t3℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是AB。三、科学探究题
-
16. 某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液。实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与。
(提出问题)废液中含有什么物质?
(交流表达)
(1)、小明通过观察,认为废液中一定含有硫酸铜。他观察到的现象是 。(2)、小红通过分析,认为废液中一定含有硫酸亚铁,她的依据是:。(3)、(作出猜想)小华认为废液中还可能含有稀硫酸。(实验验证)小华取少量废液于试管中,加入少量锌粒产生现象, 则证明废液中确实含有硫酸。通过分析与实验,同学们得出废液中含有硫酸亚铁、硫酸铜和硫酸。
(4)、(拓展应用)①若将废液中的溶质全部转化为硫酸亚铁,应加入过量的。写出该反应过程中的化学方程式;;
②反应完全后过滤,滤渣中物质为 , 滤液中溶质为硫酸亚铁。
四、计算题
-
17. 小华利用一瓶稀盐酸和相关的仪器,测定黄铜合金(Cu-Zn合金)样品的组成(不考虑黄铜中的其他杂质)。将30 mL稀盐酸分三次加入到10 g黄铜样品的粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次
第二次
第三次
连续加入稀盐酸的体积/mL
10
10
10
生成氢气的质量/g
0.08
0.08
0.04
(1)、从上表数据分析,小华用10g合金粉末总共收集到氢气g(2)、求该合金中铜的质量分数。
-