广东省东莞市光明中学2019-2020学年高三下学期化学第一次月考试卷
试卷更新日期:2021-03-10 类型:月考试卷
一、单选题
-
1. 中国传统文化中蕴藏丰富的化学知识,下列有关说法正确的是( )
A
宋·敖陶孙“人生请治田,种球多酿酒”
酿酒的主要原料是油脂
B
明·徐祯卿“草桑作蚕丝,罗琦任侬着”
区分蚕丝和棉纤维可用灼烧的方法
C
宋·苏轼“蜜蜂采花作黄蜡,取蜡为花亦其物”
蜂蜜中含果糖、葡萄糖、蔗糖和麦芽糖,它们都属于单糖
D
《纲目》“桐油吐人,得酒即解”
桐油的主要成分为高级脂肪酸甘油酯,高级脂肪酸甘油酯属于高分子化合物
A、A B、B C、C D、D2. 阿伏加德罗常数的值用NA表示。下列说法中正确的是( )A、33.6L丙烯(标准状况)与足量HCl发生加成反应,生成1-氯丙烷个数为1.5NA B、一定条件下,Ca与O2反应生成7.2gCaO2 , 转移电子的个数为0.4NA C、2mol冰醋酸与4mol乙醇一定条件下充分反应,生成乙酸乙酯个数为2NA D、1L 1mol/L的葡萄糖溶液中,溶质所含羟基的个数为5NA3. 有机物M的结构简式为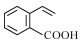 ,下列说法正确的是( ) A、有机物M既能使酸性KMnO4溶液褪色又能使溴水褪色,且反应类型相同 B、与有机物M具有相同的官能团,且不包括M的同分异构体有3种 C、1mol有机物M与足量氢气反应,消耗氢气4mol D、有机物M能发生取代、加成、氧化、水解等反应4. 四种主族元素a、b、c、d分布在三个短周期中,其原子序数依次增大,b、d的简单离子具有相同的电子层结构,b的气态氢化物溶于水可以使酚酞变红,d的简单离子半径是同周期主族元素中最小的,四种元素原子的最外层电子数之和为15。下列叙述正确的是( )A、b元素最高价氧化物对应的水化物为强酸 B、最简单气态氢化物的热稳定性:b>c C、c为第二周期第VIIA族元素 D、原子半径:d>c>b>a5. 用下列实验装置进行的相应实验,能达到实验目的的是( )
,下列说法正确的是( ) A、有机物M既能使酸性KMnO4溶液褪色又能使溴水褪色,且反应类型相同 B、与有机物M具有相同的官能团,且不包括M的同分异构体有3种 C、1mol有机物M与足量氢气反应,消耗氢气4mol D、有机物M能发生取代、加成、氧化、水解等反应4. 四种主族元素a、b、c、d分布在三个短周期中,其原子序数依次增大,b、d的简单离子具有相同的电子层结构,b的气态氢化物溶于水可以使酚酞变红,d的简单离子半径是同周期主族元素中最小的,四种元素原子的最外层电子数之和为15。下列叙述正确的是( )A、b元素最高价氧化物对应的水化物为强酸 B、最简单气态氢化物的热稳定性:b>c C、c为第二周期第VIIA族元素 D、原子半径:d>c>b>a5. 用下列实验装置进行的相应实验,能达到实验目的的是( )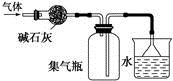
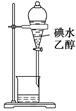
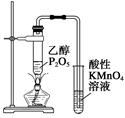
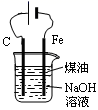
图1 图2 图3 图4
A、图1所示装置可干燥、收集氨气,并吸收多余的氨 B、图2所示装置可萃取碘水中的碘 C、图3所示装置可证明乙醇发生消去反应生成了乙烯 D、图4所示装置可制备Fe(OH)2并能较长时间观察其颜色6. 常温下,向20mL0.1mol/L NaHA(酸式盐)溶液中分别滴加0.1mol/L 盐酸或0.1mol/L NaOH溶液,溶液的pH与滴加溶液体积关系如图所示。下列推断正确的是( )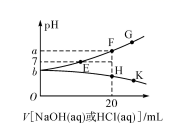 A、NaHA在水中电离程度大于水解程度 B、在对应的各点溶液中,H点水电离程度最大 C、E点对应的溶液中有c(Na+)=c(HA-)+c(A2-) D、F点对应的溶液中存在c(H+)+c(Na+)=(OH-)+c(HA-)+c(A2-)
A、NaHA在水中电离程度大于水解程度 B、在对应的各点溶液中,H点水电离程度最大 C、E点对应的溶液中有c(Na+)=c(HA-)+c(A2-) D、F点对应的溶液中存在c(H+)+c(Na+)=(OH-)+c(HA-)+c(A2-)二、综合题
-
7. 1,2-二氯乙烷是一种广泛使用的有机溶剂、黏合剂,也用作谷物和粮仓的熏蒸剂,沸点83.5℃,熔点-35℃。某研究性学习小组的同学利用如图(加热装置省略)装置制备一定量的1,2-二氯乙烷,制备原理为:C2H5OH C2H4→CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8g/mL 。
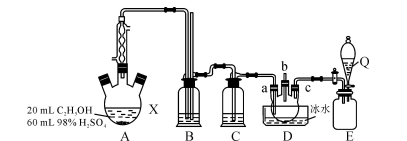 (1)、根据制备原理,可知装置A中还缺少的一种实验仪器是。使用冷凝管的目的是。(2)、实验时A中三颈烧瓶内有有刺激性气味的无机气体产生,为吸收反应中生成的无机气体,在装置B中应加入(填字母序号)。
(1)、根据制备原理,可知装置A中还缺少的一种实验仪器是。使用冷凝管的目的是。(2)、实验时A中三颈烧瓶内有有刺激性气味的无机气体产生,为吸收反应中生成的无机气体,在装置B中应加入(填字母序号)。a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)、D中a、c两个导管进入仪器中的长度不同,其优点是 , 对导管b的进一步处理方法是 , 装置E是氯气的贮气瓶,则Q中的物质是。(4)、若得到ag1,2-二氯乙烷,则乙醇的利用率为。三、工业流程题
-
8. 2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。(1)、自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈________,可以认为存在锂元素。A、紫红色 B、紫色 C、黄色(2)、工业中利用锂辉石(主要成分为LiAlSi2O6 , 还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:

已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。
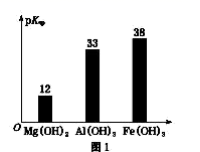
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6 , 其氧化物的形式为。
②为提高“酸化焙烧”效率,常采取的措施是。
③向“浸出液”中加入CaCO3 , 其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、Al3+完全沉淀,则pH至少为。(已知:完全沉淀后离子浓度低于1×10-5)mol/L)
④“沉锂”过程所获得的“母液”中仍含有大量的Li+ , 可将其加入到“”步骤中。
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
(3)、利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6 LixC6+Li1-xCoO2 , 其工作原理如图2。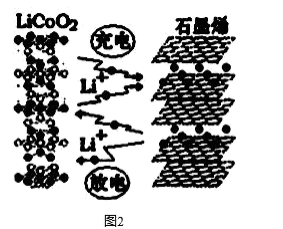
下列关于该电池的说法正确的是___________(填字母)。
A、电池反应式中过程1为放电过程 B、该电池若用隔膜可选用质子交换膜 C、石墨烯电池的优点是提高电池的储锂容量进而提高能量密度 D、充电时,LiCoO2 极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2 E、对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收四、综合题
-
9. 燃煤废气中的氮氧化物(NOx)、CO2、SO2等气体,常用下列方法处理,以实现节能减排、废物利用等。已知:25℃ 时,Kb(NH3·H2O)=1.8×10-5; H2SO3:Ka1=1.5×10-2 , Ka2=1.0×10-7。(1)、处理烟气中的SO2常用液吸法。室温条件下,将烟气通入浓氨水中得到(NH4)2SO3溶液,0.1mol/L(NH4)2SO3溶液的pH(填“>”“<”或“=”)7。(2)、用活性炭可以还原处理氮氧化物,有关反应为C(s)+2NO(g) ⇌ N2(g)+CO2(g)。在恒容条件下,能判断该反应一定达到平衡状态的依据是 ________(填选项编号)。A、单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g) B、混合气体的密度不再发生改变 C、反应体系的压强不再发生改变 D、混合气体的平均相对分子质量不再改变(3)、有科学家经过研究发现,用CO2和H2在210~290℃,催化剂条件下可转化生成甲醇蒸气和水蒸气。
①230℃,向容器中投入0.5molCO2和1.5molH2 , 当转化率达80% 时放出热量19.6kJ能量,写出该反应的热化学方程式。
②一定条件下,往 2L恒容密闭容器中充入1.0molCO2和3.0molH2 , 在不同催化剂作用下,相同时间内 CO2的转化率随温度的变化如图1所示:

催化剂效果最佳的是催化剂(填“Ⅰ”“Ⅱ”“Ⅲ”)。b点v( 正 )v( 逆 )( 填“>”“<”或“=”) 。此反应在 a 点时已达平衡状态,a 点的转化率比 c 点高的原因。已知容器内的起始压强为100kPa,则图中c点对应温度下反应的平衡常数Kp=KPa-2 。(保留两位有效数字,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)
(4)、一定条件下,CO2和H2也可以发生反应CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ΔH<0,一定温度下,在3L容积可变的密闭容器中发生如上反应,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是。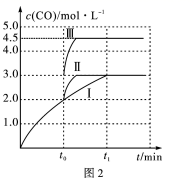 10. 第四期某些过渡元素在工业生产中有着极其重要的作用。(1)、铬是最硬的金属单质,被称为“不锈钢的添加剂”。
10. 第四期某些过渡元素在工业生产中有着极其重要的作用。(1)、铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr在周期表中的位置;其原子核外电子排布的最高能层符号.
(2)、在1 mol CrO5(其中Cr为+6价)中,含有过氧键的数目为。(3)、钒(23V)是我国的丰产元素,被称之为“工业的味精”,广泛用于催化及钢铁工业。回答下列问题:写出钒原子价电子排布图;V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为;
 (4)、Ni是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物Ni(CO)4 , 其中配原子是。(5)、钛称之为21世纪金属,具有一定的生物功能。钙钛矿(CaTiO3)晶体是工业获取钛的重要原料。CaTiO3晶胞如下图,边长为a=0.266m,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为nm,与Ti紧邻的O个数为。
(4)、Ni是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物Ni(CO)4 , 其中配原子是。(5)、钛称之为21世纪金属,具有一定的生物功能。钙钛矿(CaTiO3)晶体是工业获取钛的重要原料。CaTiO3晶胞如下图,边长为a=0.266m,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为nm,与Ti紧邻的O个数为。 (6)、在CaTiO3晶胞结构的另一种表示中,Ca处于各顶角位置,则T处于位置,O处于位置。11. 聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如下:
(6)、在CaTiO3晶胞结构的另一种表示中,Ca处于各顶角位置,则T处于位置,O处于位置。11. 聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如下: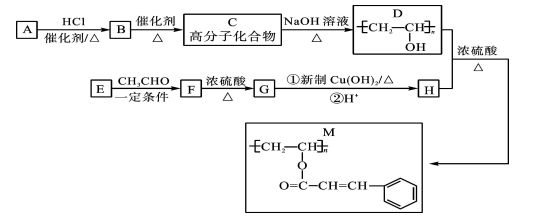
已知:R1-CHO+R2-CH2CHO
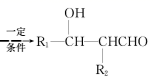
请回答:
(1)、B的化学名称为;M中含氧官能团的名称为;F→G的反应类型为。(2)、C→D的化学反应方程式为。(3)、H的顺式结构简式为。(4)、同时满足下列条件的F的同分异构体有种(不考虑立体异构):①属于芳香族化合物;②能发生水解反应和银镜反应。写出其中一种核磁共振氢谱有4种吸收峰,且峰面积之比为6∶2∶1∶1的物质的结构简式。(5)、参照上述合成路线和相关信息,以乙烯和乙醛为原料(无机试剂任选)合成有机物如图所示,设计合成路线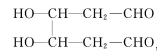
-
-