天津市宁河区芦台二中2019-2020学年高一下学期化学第一次月考试卷
试卷更新日期:2021-03-10 类型:月考试卷
一、单选题
-
1. 光导纤维的应用使人们可以在家中坐享“互联网+”带来的变革与实惠,下列物质中可以用来生产光导纤维的是( )A、钛合金 B、二氧化硅 C、晶体硅 D、氧化铝2. 下列有关氮元素的单质及其化合物的说法错误的有( )
①氮气与氧气在放电的条件下可直接生成NO2 ②铵盐都不稳定,受热分解都生成氨气 ③向Fe(NO3)2溶液中滴加稀盐酸,无明显的变化 ④实验室加热氯化铵固体,用碱石灰除氯化氢的方法制备氨气
A、1个 B、2个 C、3个 D、4个3. 如图,利用培养皿探究SO2的性质。实验时向Na2SO3固体上滴几滴浓硫酸,立即用另一表面皿扣在上面。
下表中对实验现象的描述或所做的解释错误的是( )
选项
实验现象
解释
A
BaCl2溶液变浑浊
SO2与BaCl2溶液反应产生了BaSO3沉淀
B
Na2S溶液变浑浊
SO2与Na2S溶液反应产生了S单质
C
酸性KMnO4溶液褪色
SO2具有还原性
D
品红溶液褪色
SO2具有漂白性
A、A B、B C、C D、D4. 下列实验装置不能达到实验目的的是( )A、用SO2做喷泉实验 B、验证Cu与浓硝酸反应的热量变化
B、验证Cu与浓硝酸反应的热量变化  C、验证NH3易溶于水
C、验证NH3易溶于水  D、比较Na2CO3与NaHCO3的稳定性
D、比较Na2CO3与NaHCO3的稳定性  5. 下列叙述错误的是( )A、氨易液化,液氨常用作制冷剂 B、与金属反应时,稀硝酸可能被还原为更低价态,稀硝酸氧化性强于浓硝酸 C、铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 D、稀硝酸和活泼金属反应时得不到氢气6. 化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是( )A、定性检验SO
5. 下列叙述错误的是( )A、氨易液化,液氨常用作制冷剂 B、与金属反应时,稀硝酸可能被还原为更低价态,稀硝酸氧化性强于浓硝酸 C、铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 D、稀硝酸和活泼金属反应时得不到氢气6. 化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是( )A、定性检验SO ,将BaCl2溶液用HNO3酸化
B、为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C、检验溶液中是否含有Fe2+时,用硝酸酸化
D、检验溶液中是否含有SO
,将BaCl2溶液用HNO3酸化
B、为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C、检验溶液中是否含有Fe2+时,用硝酸酸化
D、检验溶液中是否含有SO  时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
7. 某小组为研究原电池原理,设计如图装置。下列叙述错误的是( )
时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
7. 某小组为研究原电池原理,设计如图装置。下列叙述错误的是( ) A、无论a和b是否连接均可形成原电池 B、a和b不连接时,铁片上会有金属铜析出 C、a和b用导线连接时,铜片上发生的反应为Cu2++2e-= Cu D、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色8. 在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是( )A、v(A)=0.5 mol·L-1·s-1 B、v(B)=0.3 mol·L-1·s-1 C、v(C)=0.8 mol·L-1·s-1 D、v(D)=1 mol·L-1·s-19. 某反应由两步反应A B C构成,它的反应能量曲线如图,下列叙述正确的是( )
A、无论a和b是否连接均可形成原电池 B、a和b不连接时,铁片上会有金属铜析出 C、a和b用导线连接时,铜片上发生的反应为Cu2++2e-= Cu D、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色8. 在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是( )A、v(A)=0.5 mol·L-1·s-1 B、v(B)=0.3 mol·L-1·s-1 C、v(C)=0.8 mol·L-1·s-1 D、v(D)=1 mol·L-1·s-19. 某反应由两步反应A B C构成,它的反应能量曲线如图,下列叙述正确的是( ) A、两步反应均为吸热反应 B、三种化合物中C最稳定 C、A与C的能量差为E4 D、A B的反应,反应条件一定要加热10. 反应C(s)+H2O(g) CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确的是( )A、保持压强不变,充入少量氦气,反应速率会减小 B、若v(CO)=v(H2O),则反应达平衡状态 C、其他条件不变,适当增加C(s)的质量会使反应速率增大 D、其他条件不变,仅将容器的体积缩小一半,反应速率减小11. 某学生将电流表用导线与两个电极连接在一起,再将两个电极同时插入某种电解质溶液中,能观察到有电流产生的是( )A、用铜片、铅笔芯作电极插入稀硫酸中 B、用两个铜片作电极插入硝酸银溶液中 C、用锌片、铜片作电极插入番茄中 D、用铜片、铁片作电极插入酒精中12. 可再生能源是我国重要的能源资源,在满足能源需求、改善能源结构、减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术是实现节能减排的一项重要措施。下列有关分析错误的是( )
A、两步反应均为吸热反应 B、三种化合物中C最稳定 C、A与C的能量差为E4 D、A B的反应,反应条件一定要加热10. 反应C(s)+H2O(g) CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确的是( )A、保持压强不变,充入少量氦气,反应速率会减小 B、若v(CO)=v(H2O),则反应达平衡状态 C、其他条件不变,适当增加C(s)的质量会使反应速率增大 D、其他条件不变,仅将容器的体积缩小一半,反应速率减小11. 某学生将电流表用导线与两个电极连接在一起,再将两个电极同时插入某种电解质溶液中,能观察到有电流产生的是( )A、用铜片、铅笔芯作电极插入稀硫酸中 B、用两个铜片作电极插入硝酸银溶液中 C、用锌片、铜片作电极插入番茄中 D、用铜片、铁片作电极插入酒精中12. 可再生能源是我国重要的能源资源,在满足能源需求、改善能源结构、减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术是实现节能减排的一项重要措施。下列有关分析错误的是( ) A、如上图是太阳能光伏发电原理图,图中A极为正极 B、风能、太阳能、生物质能等属于可再生能源 C、推广可再生能源有利于经济可持续发展 D、光伏发电能量转化方式是太阳能直接转变为电能
A、如上图是太阳能光伏发电原理图,图中A极为正极 B、风能、太阳能、生物质能等属于可再生能源 C、推广可再生能源有利于经济可持续发展 D、光伏发电能量转化方式是太阳能直接转变为电能二、多选题
-
13. 用下列两种途径制取H2SO4(某些反应条件和产物已省略),下列有关说法错误的是( )
途径①:S H2SO4 途径②:S SO2 SO3 H2SO4
A、途径①中反应仅体现了浓硝酸的强氧化性 B、途径②中可通过控制反应条件,将S直接氧化为SO3 C、由途径①和②分别制取1molH2SO4 , 理论上均消耗1molS,均共转移6mol电子 D、途径②相较于途径①更能体现“绿色化学”的理念,因为途径②的污染相对于途径①更小三、填空题
-
14. 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如下。
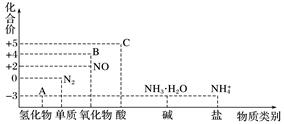
回答下列问题:
(1)、在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是。(2)、在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:。(3)、实验室中,检验溶液中含有NH4+的操作方法是。(4)、物质B为红棕色气体,写出该物质与水反应的离子方程式: , 当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为mol。(5)、写出一种人工固氮的化学反应原理。(6)、Cu与一定浓度的硝酸溶液反应生成NO时的离子反应方程式为。15. 某温度下,在2L密闭容器中充入4mol A气体和3mol B气体,发生下列反应:2A(g)+B(g) C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。(1)、求x =。(2)、求这段时间A的平均反应速率为 mol·L-1·s-1。(3)、平衡时B的浓度为 mol·L-1。(4)、A的转化率为。(5)、下列叙述能说明上述反应达到平衡状态的是_____A、单位时间内每消耗2mol A,同时生成1mol C B、单位时间内每生成1mol B,同时生成1mol C C、D的体积分数不再变化 D、混合气体的压强不再变化 E、B、C的浓度之比为1∶116. 微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn=ZnO+2Ag,其中一个电极反应为Ag2O+H2O+2e-=2Ag+2OH-。 (1)、判断正负极的材料。
(1)、判断正负极的材料。负极材料 , 正极材料。
(2)、写出另一电极的电极反应式,并判断反应类型。电极反应式
反应类型
(3)、判断电池工作时,电子的流动方向和电解质溶液中离子的流动方向。电子由到 , 溶液中的阳离子流向电池的 , 阴离子流向(4)、在电池使用的过程中,电解质溶液中KOH的物质的量怎样变化?(增大、减小、不变)(5)、当电池工作时通过电路对外提供了1 mol电子,计算消耗的负极的质量。(6)、氢氧燃料电池为绿色化学电源,在碱性NaOH溶液为电解质溶液时的负极电极反应式为。
-