吉林省长春市农安县农安三中2019-2020学年九年级下学期化学第二次月考试卷
试卷更新日期:2021-03-09 类型:月考试卷
一、单选题
-
1. 厨房里的下列变化,属于物理变化的是( )A、煤燃烧 B、刀生锈 C、菜腐烂 D、水蒸发2. “绿水青山就是金山银山”。下列物质的大量排放,不会造成环境污染的是( )A、氮气 B、二氧化氮 C、固体粉尘 D、工业废水3. 生活中常见的下列物质不能溶于水的是( )A、加碘食盐 B、花生油 C、桂花醋 D、小苏打4. 下列实验操作中,正确的是( )A、滴加液体
 B、稀释浓硫酸
B、稀释浓硫酸 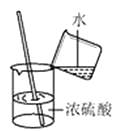 C、检查气密性
C、检查气密性  D、熄灭酒精灯
D、熄灭酒精灯 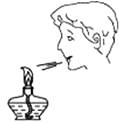 5. 人们在工作、生活中为了防止发生事故,常采取一些安全措施,下列措施安全的是( )A、油锅着火,立即用水浇火 B、家用电器着火时,应立即用水浇灭 C、煤矿的矿井注意通风并严禁烟火 D、厨房煤气泄露,立即打开油烟机6. 研发高性能“中国芯”是我国信息产业的当务之急,“中国芯”的主要材料是高纯度的单质硅,工业上用 来制取粗硅,下列说法正确的是( )A、SiO2属于金属氧化物 B、该反应为置换反应 C、硅元素在地壳中的含量比氧元素多 D、该反应体现了C的氧化性7. 下列说法中,正确的是( )A、浓盐酸、浓硫酸都易挥发 B、CH4、CO都能作燃料 C、CaO、NaOH溶液都能做干燥剂 D、CO2、CO都是有毒气体8. 下列关于物质的组成、结构、性质、用途以及变化规律的总结中,正确的是( )A、Cl、Cl-两种微粒的质子数相同,化学性质相同 B、H2O2、H2SO4、Ca(OH)2均由不同种元素组成,都属于混合物 C、NaOH、Al(OH)3都是常见的碱,都可用于治疗胃酸过多 D、FeSO4溶液和Fe2(SO4)3溶液中的阳离子不同,溶液颜色不同9. 列有关物质用途的说法中正确的是( )A、NaOH、CaO都能用作食品干燥剂 B、KNO3、NH4Cl都能用作化肥 C、N2、O2都能用作焊接金属的保护气 D、NaCl和NaNO2都能用作食品的调味品10. 下列实验方案中,能达到目的的是( )A、分离CaCO3和NaCl的混合物:加水溶解、过滤、干燥 B、.制取Mg(OH)2:将Ba(OH)2溶液和MgSO4溶液混合后过滤 C、除去H2中水蒸气和HCl气体:依次通过浓硫酸和NaOH溶液 D、检验KCl溶液中混有的K2CO3:取样,加入足量的Ca(OH)2溶液
5. 人们在工作、生活中为了防止发生事故,常采取一些安全措施,下列措施安全的是( )A、油锅着火,立即用水浇火 B、家用电器着火时,应立即用水浇灭 C、煤矿的矿井注意通风并严禁烟火 D、厨房煤气泄露,立即打开油烟机6. 研发高性能“中国芯”是我国信息产业的当务之急,“中国芯”的主要材料是高纯度的单质硅,工业上用 来制取粗硅,下列说法正确的是( )A、SiO2属于金属氧化物 B、该反应为置换反应 C、硅元素在地壳中的含量比氧元素多 D、该反应体现了C的氧化性7. 下列说法中,正确的是( )A、浓盐酸、浓硫酸都易挥发 B、CH4、CO都能作燃料 C、CaO、NaOH溶液都能做干燥剂 D、CO2、CO都是有毒气体8. 下列关于物质的组成、结构、性质、用途以及变化规律的总结中,正确的是( )A、Cl、Cl-两种微粒的质子数相同,化学性质相同 B、H2O2、H2SO4、Ca(OH)2均由不同种元素组成,都属于混合物 C、NaOH、Al(OH)3都是常见的碱,都可用于治疗胃酸过多 D、FeSO4溶液和Fe2(SO4)3溶液中的阳离子不同,溶液颜色不同9. 列有关物质用途的说法中正确的是( )A、NaOH、CaO都能用作食品干燥剂 B、KNO3、NH4Cl都能用作化肥 C、N2、O2都能用作焊接金属的保护气 D、NaCl和NaNO2都能用作食品的调味品10. 下列实验方案中,能达到目的的是( )A、分离CaCO3和NaCl的混合物:加水溶解、过滤、干燥 B、.制取Mg(OH)2:将Ba(OH)2溶液和MgSO4溶液混合后过滤 C、除去H2中水蒸气和HCl气体:依次通过浓硫酸和NaOH溶液 D、检验KCl溶液中混有的K2CO3:取样,加入足量的Ca(OH)2溶液二、填空题
-
11. 请用化学用语填空(1)、2个铝离子;(2)、空气中含量最多元素 ;(3)、碘酒中的溶剂。12. 有以下物质,①红磷;②水;③氧化镁;④氨水;⑤铁,其中属于单质的是(填序号,下同),属于氧化物的是 , 含有水分子的是。13. 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
 (1)、图一是汞元素在元素周期表中的信息,则汞元素属于(填“金属”或“非金属”)元素,该元素的原子核外电子数为;(2)、图二为元素周期表的一部分,甲、乙代表两种不同元素,以下判断正确的是(填字母序号)。
(1)、图一是汞元素在元素周期表中的信息,则汞元素属于(填“金属”或“非金属”)元素,该元素的原子核外电子数为;(2)、图二为元素周期表的一部分,甲、乙代表两种不同元素,以下判断正确的是(填字母序号)。A甲的原了序数大于乙
B甲和Cl在同一周期
C乙和He的最外层电子数相同
14. 氧气和水是重要的化学物质,应用它们的化学知识回答问题。(1)、二者在组成上的共同点是都含有;(2)、超市里的一些食品采用真空包装,其原理是除去袋内的空气,使微生物因缺少而受到抑制,达到防腐作用;(3)、在过滤、吸附和蒸馏三种净水方法中,单一操作相对净化程度最高的是;(4)、某条河的附近有一硫酸厂,欲检验该厂废水呈酸性,一般可选用下列药品中的________(填字母序号)。A、Ca(OH)2 B、Mg C、CaO D、AgNO3 E NaCO315. 请回答有关金属的问题。(1)、在Cu和Zn中,活动性较强的是;(2)、Cu与AgNO3溶液的反应中,离子变成了原子;(3)、只用少量的盐酸、一支试管和锌、铜、铝,通过加入金属的顺序不同,也能验证这三种金属的活动性的强弱,则加入的顺序为(假设每次的反应均反应完全)。16. 根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题。
温度(℃)
0
20
40
60
80
100
溶解度
(g/100g水)
KNO3
13.3
31.6
64.0
110.0
169.0
246.0
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
(1)、在80℃时,NaCl的溶解度为g;(2)、在35℃时,KNO3和NaCl两种物质中,溶解度较大的是;(3)、将80gKNO3、20gNaCl分别放入100g60℃的水中,充分搅拌,再到20℃,下列有关说法中,正确的是。A 0℃时有部分KNO3与溶液共存
B 降温到20℃时只有KNO3析出
C 降温到20℃时NaCl已经饱和
三、计算题
-
17. 要用溶质质量分数为19.6%的稀硫酸与金属锌反应制取氢气,请回答下列问题(1)、用水和浓硫酸来配制500g溶质质量分数为19.6%的稀硫酸。需溶质质量分数为98%的浓硫酸的质量为g;(2)、配制溶液时,用玻璃棒不断搅拌,玻璃棒的作用是;(3)、取配制后的溶液50g与足量的金属锌反应,生成氢气的质量为g。
四、简答题
-
18. 分析下列化学反应,回答有关问题。
①CaCO3+2HCl=CaCl2+H2O+CO2↑
②Na2CO3+2HCl=2NaCl+H2O+CO2↑
③BaCO3+2HCl=BaCl2+H2O+CO2↑
(1)、通常情况下,含有碳酸根(CO32-)的盐与稀盐酸反应都生成盐、水和;(2)、依据上述反应规律,写出碳酸钾与稀盐酸反应的化学方程式;(3)、欲鉴别碳酸钠和氯化钠两瓶白色粉末,你的实验操作是。19. 实验室中,小美做了三个实验,分别向三支试管中依次加入相应的物质。实验一:氢氧化钠溶液+过量稀盐酸+适量氧化铜
实验二:氢氧化钠溶液+几滴酚酞+过量稀盐酸
实验三:稀盐酸+过量氢氧化钠溶液+过量碳酸钠
(1)、实验一(填“能”或“否”)证明氢氧化钠与稀盐酸发生反应;(2)、实验二中发生反应的化学方程式为;(3)、实验三的实验现象是;(4)、上述三个实验中涉及酸的化学性质有:与酸碱指示剂、;(5)、实验结束后,将三个实验的所有废液倒在一起,最终只得到蓝色溶液。取少量蓝色溶液,加入足量盐酸,无明显现象。为了确定溶液中可能有的离子是否存在,下列物质可行的是___________。A、酚酞溶液 B、Na2CO3溶液 C、NaOH溶液 D、BaCl2溶液五、实验题
-
20. 以下是在实验室里制取气体时常用的部分仪器。

 (1)、在实验室里,用高锰酸钾制取并用排水法收集氧气。除选用上图中可用的部分仪器外,还必须补充的玻璃仪器是;(2)、下列制取气体的实验,可利用上图仪器中的A,B,C,F,G,K,L,M和N,组装成的制取气体的装置来完成的是。
(1)、在实验室里,用高锰酸钾制取并用排水法收集氧气。除选用上图中可用的部分仪器外,还必须补充的玻璃仪器是;(2)、下列制取气体的实验,可利用上图仪器中的A,B,C,F,G,K,L,M和N,组装成的制取气体的装置来完成的是。A 锌粒和稀硫酸制取氢气
B 加热氯酸钾和二氧化锰的混合物制取氧气
C 用块状碳化钙和水在常温下混合制取难溶于水的乙炔气体
D 加热碱石灰和氯化铵的固体混合物制取极易溶于水的氨气
六、流程题
-
21. 以黄铁矿为原料,生产硫酸的简要流程如图:
 (1)、黄铁矿中的元素一定含有;(2)、浓硫酸具有性,必须密封保存。(3)、该生成流程中,生产设备不是敞开的,以防主要污染物泄漏造成空气污染;(4)、流程中SO2转化为SO3的反应属于化合反应,其化学方程式为。
(1)、黄铁矿中的元素一定含有;(2)、浓硫酸具有性,必须密封保存。(3)、该生成流程中,生产设备不是敞开的,以防主要污染物泄漏造成空气污染;(4)、流程中SO2转化为SO3的反应属于化合反应,其化学方程式为。七、推断题
-
22. 某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
 (1)、写出生成白色固体丙的化学方程式;(2)、向无色溶液D中加入过量稀盐酸的目的是;(3)、分析上述实验可知,白色固体甲中一定没有的物质是;(4)、取溶液无色溶液A,B,C,D的一种,分别滴加到稀硫酸和NaOH溶液样品中,就能把二者鉴别开来的是无色溶液。
(1)、写出生成白色固体丙的化学方程式;(2)、向无色溶液D中加入过量稀盐酸的目的是;(3)、分析上述实验可知,白色固体甲中一定没有的物质是;(4)、取溶液无色溶液A,B,C,D的一种,分别滴加到稀硫酸和NaOH溶液样品中,就能把二者鉴别开来的是无色溶液。
-
-
-