吉林省四平市铁西区吉林师大附中2019-2020学年九年级下学期化学第一次月考试卷
试卷更新日期:2021-03-09 类型:月考试卷
一、单选题
-
1. 空气中含量最高的物质是( )A、氮气 B、稀有气体 C、氧气 D、水蒸气2. 属于活性炭物理性质的是( )A、稳定性 B、吸附性 C、还原性 D、可燃性3. 下图所示实验操作正确的是( )A、测定溶液的pH
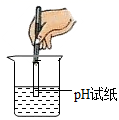 B、读出液体的体积
B、读出液体的体积  C、稀释浓硫酸
C、稀释浓硫酸  D、移走蒸发皿
D、移走蒸发皿  4. 下列说法正确的是()A、原子的质量主要集中在原子核上 B、相同的原子无法构成不同的分子 C、温度计内汞柱液面上升说明汞原子体积变大 D、原子呈电中性是因为原子中质子数与中子数相等5. 下列实验现象,描述错误的是()A、将一氧化碳通入灼热的氧化铁,红色粉末逐渐变为黑色粉末 B、碳在氧气中剧烈燃烧,发出白光,生成一种能使澄清石灰水变浑浊的气体 C、电解水时负极和正极产生气体的体积比为1:2 D、向硫酸铜溶液中滴加氢氧化钠溶液,产生蓝色沉淀6. 下列关于溶液的说法错误的是()A、用洗洁精洗去餐具上的油污,利用的是乳化原理 B、气体的溶解度与温度和压强有关 C、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污7. 一氧化碳在氧气中燃烧,火焰呈蓝色,同时放出大量的热,其反应的微观过程如下图所示,根据此图判断,下列说法正确的是 ( )
4. 下列说法正确的是()A、原子的质量主要集中在原子核上 B、相同的原子无法构成不同的分子 C、温度计内汞柱液面上升说明汞原子体积变大 D、原子呈电中性是因为原子中质子数与中子数相等5. 下列实验现象,描述错误的是()A、将一氧化碳通入灼热的氧化铁,红色粉末逐渐变为黑色粉末 B、碳在氧气中剧烈燃烧,发出白光,生成一种能使澄清石灰水变浑浊的气体 C、电解水时负极和正极产生气体的体积比为1:2 D、向硫酸铜溶液中滴加氢氧化钠溶液,产生蓝色沉淀6. 下列关于溶液的说法错误的是()A、用洗洁精洗去餐具上的油污,利用的是乳化原理 B、气体的溶解度与温度和压强有关 C、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污7. 一氧化碳在氧气中燃烧,火焰呈蓝色,同时放出大量的热,其反应的微观过程如下图所示,根据此图判断,下列说法正确的是 ( ) A、该反应是置换反应 B、化学反应前后元素的种类不变 C、化学反应前后分子的种类和数目都不变 D、发生反应前,一氧化碳和氧气的质量比是7:48. 下列实验能达到实验目的是( )
A、该反应是置换反应 B、化学反应前后元素的种类不变 C、化学反应前后分子的种类和数目都不变 D、发生反应前,一氧化碳和氧气的质量比是7:48. 下列实验能达到实验目的是( )
A、探究铁锈蚀条件 B、探究燃烧条件
B、探究燃烧条件  C、测定空气中氧气含量
C、测定空气中氧气含量  D、探究分子运动
D、探究分子运动  9. 逻辑推理是化学学习中常用的思维方法,以下推理正确的是( )A、碱都含有氢、氧元素,所以含有氢、氧元素的化合物一定是碱 B、中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 C、单质是同种元素组成的纯净物,所以同种元素组成的纯净物一定是单质 D、置换反应有单质和化合物生成,所以生成单质和化合物的反应都属于置换反应10. 某同学根据下列四个实验目的设计的方案,其中不合理的是( )A、鉴别软硬水:取样,加等量的肥皂水 B、鉴别硫酸铵和氯化钠:取样,加熟石灰混合研磨 C、除去氢氧化钠溶液中少量碳酸钠:加过量的氢氧化钙溶液后过滤 D、除去氯化铜溶液中的少量盐酸:加过量的氧化铜粉末,过滤
9. 逻辑推理是化学学习中常用的思维方法,以下推理正确的是( )A、碱都含有氢、氧元素,所以含有氢、氧元素的化合物一定是碱 B、中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 C、单质是同种元素组成的纯净物,所以同种元素组成的纯净物一定是单质 D、置换反应有单质和化合物生成,所以生成单质和化合物的反应都属于置换反应10. 某同学根据下列四个实验目的设计的方案,其中不合理的是( )A、鉴别软硬水:取样,加等量的肥皂水 B、鉴别硫酸铵和氯化钠:取样,加熟石灰混合研磨 C、除去氢氧化钠溶液中少量碳酸钠:加过量的氢氧化钙溶液后过滤 D、除去氯化铜溶液中的少量盐酸:加过量的氧化铜粉末,过滤二、填空题
-
11. 用符合要求的物质的序号填空。
①氯化钠 ②小苏打 ③干冰 ④武德合金
(1)、可用于治疗胃酸过多的是。(2)、可用于制保险丝的是。(3)、可用于配制生理盐水的是。(4)、可用于人工降雨的是。12. 下图中ABCD是四种粒子的结构示意图,请回答下列问题。 (1)、以上粒子的结构示意图中,属于同种元素的粒子是(填字母)。(2)、以上四种粒子中,能得到电子的是(填字母代号)。(3)、D中x。13. “见著知微,见微知著”是化学思维方法,从宏观知微观。(1)、50mL水与50mL乙醇混合后,溶液总体积小于100mL,微观解释为。(2)、气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是(填符号)。(3)、一氧化碳和二氧化碳化学性质不同的原因:。14. 水是生命之源,人类的日常生活和工农业生产都离不开水。(1)、向某水样中加入肥皂水,搅拌,若观察到的现象,则水样为软水。(2)、如果工业废水中含有酸性物质,应该用性物质处理后再排放。(3)、市售“自热米饭”的自热原理是:让饭盒夹层中的水与生石灰接触,反应并放出大量的热。该反应的化学方程式是。15. 人类文明进步与金属材料的发展关系十分密切,金属在生活和生产中有着非常广泛的应用。请回答下列问题。(1)、生铁和钢都是铁的合金,二者性能不同的原因是。(2)、厨房中的下列物品所使用的主要材料是金属材料的是
(1)、以上粒子的结构示意图中,属于同种元素的粒子是(填字母)。(2)、以上四种粒子中,能得到电子的是(填字母代号)。(3)、D中x。13. “见著知微,见微知著”是化学思维方法,从宏观知微观。(1)、50mL水与50mL乙醇混合后,溶液总体积小于100mL,微观解释为。(2)、气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是(填符号)。(3)、一氧化碳和二氧化碳化学性质不同的原因:。14. 水是生命之源,人类的日常生活和工农业生产都离不开水。(1)、向某水样中加入肥皂水,搅拌,若观察到的现象,则水样为软水。(2)、如果工业废水中含有酸性物质,应该用性物质处理后再排放。(3)、市售“自热米饭”的自热原理是:让饭盒夹层中的水与生石灰接触,反应并放出大量的热。该反应的化学方程式是。15. 人类文明进步与金属材料的发展关系十分密切,金属在生活和生产中有着非常广泛的应用。请回答下列问题。(1)、生铁和钢都是铁的合金,二者性能不同的原因是。(2)、厨房中的下列物品所使用的主要材料是金属材料的是A.保鲜膜 B.不锈钢炊具 C.橡胶手套 D.铜制水龙头
(3)、还原铁粉常用做食品除湿剂(干燥剂),又称“双吸剂”。它能够吸收空气中的。(4)、铝制品抗腐蚀性强的原因。16. 根据如图甲、乙、丙三种固体的溶解度曲线回答下列问题: (1)、M点表示的含义是。(2)、50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为。(3)、将丙的不饱和溶液转化成饱和溶液的方法(答一种即可)。(4)、20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数(填“变大”、“变小”或“不变”)。17. 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心。氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜。为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题。
(1)、M点表示的含义是。(2)、50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为。(3)、将丙的不饱和溶液转化成饱和溶液的方法(答一种即可)。(4)、20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数(填“变大”、“变小”或“不变”)。17. 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心。氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜。为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题。 (1)、小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶盖。依据反应③说明NaOH必须密封保存,否则在空气中要变质。如果该溶液变质,则发生反应的化学方程式为。(2)、要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是____________。A、稀盐酸 B、酚酞溶液 C、CaCl2 D、Ca(OH)2(3)、依据反应②,氢氧化钾能与下列物质反应的是。
(1)、小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶盖。依据反应③说明NaOH必须密封保存,否则在空气中要变质。如果该溶液变质,则发生反应的化学方程式为。(2)、要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是____________。A、稀盐酸 B、酚酞溶液 C、CaCl2 D、Ca(OH)2(3)、依据反应②,氢氧化钾能与下列物质反应的是。A 硫酸 B 氯化钡 C 硫酸铜 D 碳酸钠
(4)、为了吸收二氧化碳,氢氧化钠溶液比氢氧化钙溶液好,理由是。(5)、硫酸铵[(NH4)2SO4]、磷酸二氢钙[Ca(H2PO4)2]、亚硝酸钠(NaNO2)、硝酸钾(KNO3)等属于盐,其中又属于复合肥的是。三、实验题
-
18. 化学是一门以实验为基础的学科,请结合下列图示实验装置,回答问题。
 (1)、图中①仪器的名称是:。(2)、用氯酸钾和二氧化锰固体制取较纯的氧气时,可选用的发生装置和收集装置是(填字母序号),反应的化学方程式是。(3)、用E装置收集二氧化碳,其验满的方法是。(4)、小阳欲制取并测定生成氢气的体积,请从上图A~G中选择最佳的装置进行组合,整套装置的导管口连接顺序是b→(填接口序号)。
(1)、图中①仪器的名称是:。(2)、用氯酸钾和二氧化锰固体制取较纯的氧气时,可选用的发生装置和收集装置是(填字母序号),反应的化学方程式是。(3)、用E装置收集二氧化碳,其验满的方法是。(4)、小阳欲制取并测定生成氢气的体积,请从上图A~G中选择最佳的装置进行组合,整套装置的导管口连接顺序是b→(填接口序号)。四、计算题
-
19. 请回答并完成下列计算。(1)、实验室要配制50g溶质质量分数为8%的氢氧化钠溶液,需称取g氢氧化钠固体。(2)、向上述配制好的溶液中加入50g稀硫酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。
-