初中化学鲁教版九年级下学期 第九单元测试卷
试卷更新日期:2021-03-06 类型:单元试卷
一、单选题
-
1. 金属资源是不可再生的,保护金属资源是我们刻不容缓的职责。下列有关叙述错误的是( )。A、大力开采矿物,以保障金属材料的供应 B、提高废旧金属的回收利用率 C、在金属制品表面刷漆、涂油,防止金属腐蚀 D、用特种塑料代替金属制造机器的零部件2. 下列关于金属的说法正确的是( )A、焊锡是纯净的锡 B、铝制品属 于不可回收垃圾 C、铁在潮湿空气中容易生锈 D、纯铜的硬度大于青铜3. 下列方法中不能防止铁锅被腐蚀的是( )。A、表层镀锌 B、食盐水浸泡 C、制成合金 D、表层涂油4. 利用铝合金代替铝制钥匙,主要是利用铝合金的( )。A、密度小 B、熔点低 C、不易腐蚀 D、硬度大5. 正确的实验设计和规范操作是科学实验的基本要求。下列实验正确且能达到实验目的的是( )A、探究空气中氧气的含量
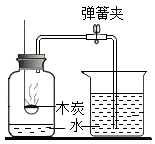 B、探究燃烧的条件
B、探究燃烧的条件 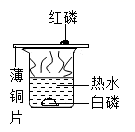 C、验证质量守恒定律
C、验证质量守恒定律 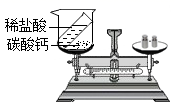 D、比较黄铜和铜的硬度
D、比较黄铜和铜的硬度 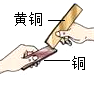 6. 下列图像能正确表示对应变化关系的是( )A、实验室电解水
6. 下列图像能正确表示对应变化关系的是( )A、实验室电解水 B、加热KClO3和MnO2的混合物制取氧气
B、加热KClO3和MnO2的混合物制取氧气  C、将等质量的镁片、铁片加入足量的等浓度的稀硫酸中
C、将等质量的镁片、铁片加入足量的等浓度的稀硫酸中  D、加热一定质量的氧化汞
D、加热一定质量的氧化汞  7. 向盛有一定量的铝粉的小烧杯中逐滴加入稀硫酸至过量,如图是反应过程中烧杯中物质总质量Y随加入稀硫酸的质量X变化的关系,其中正确的是( )A、
7. 向盛有一定量的铝粉的小烧杯中逐滴加入稀硫酸至过量,如图是反应过程中烧杯中物质总质量Y随加入稀硫酸的质量X变化的关系,其中正确的是( )A、 B、
B、 C、
C、 D、
D、 8. 往CuSO4溶液中加入一定量的铁粉,充分反应后,有金属析出:过滤,洗涤后往滤渣中加入一定量的稀硫酸,有气泡产生,则下列说法错误的是( )A、滤渣中一定有Cu和Fe B、滤液一定呈浅绿色 C、滤液一定不含CuSO4 D、滤液一定含Fe2(SO4)39. 已知:①x+H2SO4= XSO4+H2↑; ②Y+2ZNO3= Y(NO3)2+2Z;③Y与稀硫酸不反应。则符合要求的X、Y、Z分别是( )A、Cu、Hg、Ag B、Fe、Cu、Ag C、Mg、Zn、Fe D、Zn、Fe、Cu10. 向AgNO3和Mg(NO3)2的混合溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法正确的是( )A、向滤渣中加入稀盐酸,一定有气泡产生; B、滤渣中一定含有Ag、Fe,一定不含Al; C、滤渣中一定含有Ag,可能含有Fe,一定不含Al; D、滤液中一定含有Fe(NO3)2和Mg(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3。
8. 往CuSO4溶液中加入一定量的铁粉,充分反应后,有金属析出:过滤,洗涤后往滤渣中加入一定量的稀硫酸,有气泡产生,则下列说法错误的是( )A、滤渣中一定有Cu和Fe B、滤液一定呈浅绿色 C、滤液一定不含CuSO4 D、滤液一定含Fe2(SO4)39. 已知:①x+H2SO4= XSO4+H2↑; ②Y+2ZNO3= Y(NO3)2+2Z;③Y与稀硫酸不反应。则符合要求的X、Y、Z分别是( )A、Cu、Hg、Ag B、Fe、Cu、Ag C、Mg、Zn、Fe D、Zn、Fe、Cu10. 向AgNO3和Mg(NO3)2的混合溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法正确的是( )A、向滤渣中加入稀盐酸,一定有气泡产生; B、滤渣中一定含有Ag、Fe,一定不含Al; C、滤渣中一定含有Ag,可能含有Fe,一定不含Al; D、滤液中一定含有Fe(NO3)2和Mg(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3。二、综合题
-
11. 化学为5G助力。(1)、承载基站的铁塔表面涂漆,是为了隔绝 , 从而防止锈蚀。(2)、基站供电系统的导线多为铜线,使用铜是因为它具有延展性和。(3)、使用人造金刚石薄膜做基体材料,是未来芯片研究的发展方向,金刚石与石墨物理性质有明显差异的原因是。12. 我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有铁Fe、锡Sn、铜Cu、银Ag、金Au等金属,如图是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
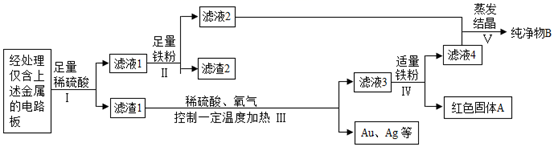 (1)、过程Ⅰ、Ⅲ、Ⅳ均涉及的操作是 , 该操作需要用到一种金属材料制成的仪器是。(2)、写出过程Ⅱ中反应的化学方程式、。(3)、写出过程Ⅲ中反应的化学方程式。(4)、滤液4的主要成分(水除外)是。13. 金属材料在我们生活中无处不在,从日常生活用品电热水壶,到电线、电缆等,都离不开金属材料(1)、电热水壶的内胆材料主要使用304不锈钢(铁的合金),不锈钢能用于做热水壶内胆是由于它具有性,久用的热水壶内胆通常会有水垢,这时可用稀盐酸浸泡热水壶,但浸泡过久会腐蚀热水壶内胆,原因是(用化学方程式表示),该反应的类型是反应。(2)、要探究铁、铜两种金属活动性顺序,实验前先用砂纸打磨铜丝和铁丝,除铁丝和铜丝外,下列能探究出两种金属活动性顺序的试剂有(填序号)。
(1)、过程Ⅰ、Ⅲ、Ⅳ均涉及的操作是 , 该操作需要用到一种金属材料制成的仪器是。(2)、写出过程Ⅱ中反应的化学方程式、。(3)、写出过程Ⅲ中反应的化学方程式。(4)、滤液4的主要成分(水除外)是。13. 金属材料在我们生活中无处不在,从日常生活用品电热水壶,到电线、电缆等,都离不开金属材料(1)、电热水壶的内胆材料主要使用304不锈钢(铁的合金),不锈钢能用于做热水壶内胆是由于它具有性,久用的热水壶内胆通常会有水垢,这时可用稀盐酸浸泡热水壶,但浸泡过久会腐蚀热水壶内胆,原因是(用化学方程式表示),该反应的类型是反应。(2)、要探究铁、铜两种金属活动性顺序,实验前先用砂纸打磨铜丝和铁丝,除铁丝和铜丝外,下列能探究出两种金属活动性顺序的试剂有(填序号)。①硝酸银溶液
②稀硫酸
③硫酸铜溶液
(3)、向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。当反应进行到b点时,过滤,滤液中溶有的物质是 。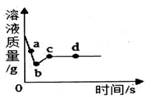 14. 人类的生活离不开金属材料。(1)、金属材料应用广泛,试回答下列生活中的问题:
14. 人类的生活离不开金属材料。(1)、金属材料应用广泛,试回答下列生活中的问题:①多数合金的熔点 (填 “高于”或“低于”)组成它的成分金属。
②家用热水瓶玻璃内胆壁的银白色金属是(填化学式),它在自然界中主要以(填“单质”、“化合物”)形式存在。
(2)、下图是实验室用一氧化碳与氧化铁反应的装置示意图,请回答下列问题。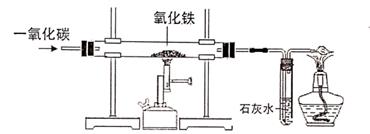
①实验过程中,先通入一氧化碳的目的是;
②实验中,硬质玻璃管处的现象 , 反应的化学方程式是;
③实验中,试管中的现象 , 反应的化学方程式是;
④右测导气管口放置点燃的酒精灯的目的是 , 反应的化学方程式是。
(3)、炼铁厂常以焦炭、赤铁矿、空气、石灰石为原料炼铁,反应过程如下:
写出①②两步的化学方程式、。
(4)、每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的和共同作用的结果:(5)、为了防止钢铁锈蚀,人们常采用的方法(任写一种)来达到目的。三、实验探究题
-
15. 炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置如下图。

对实验进行分析并回答下列问题。
(1)、给玻璃管加热的仪器叫酒精喷灯,要用其(填“外焰”“内焰”或“焰心”)进行加热。(2)、实验中玻璃管里氧化铁粉末的颜色变化是 , 观察到澄清石灰水的现象是。(3)、实验前“通入CO”与“开始加热”的顺序是;实验后“停止通人CO”与“停止加热”的顺序是。(4)、实验时要在装置末端a处点燃一盏酒精灯,其作用是。16. 结合下列与铁有关的实验,回答问题: (1)、A实验中铁丝燃烧的现象是;(2)、B实验中发生的反应可用化学方程式表示为;(3)、C实验中能够在铁丝表面观察到的明显现象是;(4)、D实验中,实验对比,能够证明铁生锈需要水。
(1)、A实验中铁丝燃烧的现象是;(2)、B实验中发生的反应可用化学方程式表示为;(3)、C实验中能够在铁丝表面观察到的明显现象是;(4)、D实验中,实验对比,能够证明铁生锈需要水。四、计算题