北京市海淀区2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-03-04 类型:期末考试
一、单选题
-
1. 下图为空气成分示意图(按体积计算),其中“a”代表的是()
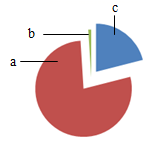 A、氧气 B、氮气 C、二氧化碳 D、稀有气体2. 下列含金属元素的物质是( )A、H2S B、P2O5 C、AgNO3 D、H2O3. 下列属于铁丝在氧气中燃烧的现象的是( )A、发出黄色火焰 B、生成有刺激性气味的气体 C、产生大量白烟 D、生成黑色固体4. 下列图标中,表示“禁止燃放鞭炮”的是( )
A、氧气 B、氮气 C、二氧化碳 D、稀有气体2. 下列含金属元素的物质是( )A、H2S B、P2O5 C、AgNO3 D、H2O3. 下列属于铁丝在氧气中燃烧的现象的是( )A、发出黄色火焰 B、生成有刺激性气味的气体 C、产生大量白烟 D、生成黑色固体4. 下列图标中,表示“禁止燃放鞭炮”的是( )
A、 B、
B、 C、
C、 D、
D、 5. 下列操作错误的是( )A、称量固体
5. 下列操作错误的是( )A、称量固体 B、加热液体
B、加热液体  C、点燃酒精灯
C、点燃酒精灯  D、取用固体粉末
D、取用固体粉末  6. 下列做法不利于保护环境的是( )A、垃圾分类处理 B、倡导使用一次性筷子 C、使用节水龙头 D、乘坐公共交通工具7. 下列不属于新能源的是( )A、潮汐能 B、太阳能 C、风能 D、化石能源8. 下列材料属于合金的是( )A、不锈钢 B、塑料 C、玻璃 D、陶瓷9. 下列饮品属于溶液的是( )A、蔗糖水 B、牛奶 C、果粒橙 D、豆浆10. 下列物质含有氢分子的是( )A、H2 B、H2O2 C、H2CO3 D、N2H411. 下列物质的用途中,利用其物理性质的是( )A、氧气用于炼钢 B、干冰用作制冷剂 C、乙醇用作燃料 D、氮气用作保护气12. 铝是地壳中含量最高的金属元素。元素周期表中铝元素的信息如图所示。下列关于铝原子的说法错误的是( )
6. 下列做法不利于保护环境的是( )A、垃圾分类处理 B、倡导使用一次性筷子 C、使用节水龙头 D、乘坐公共交通工具7. 下列不属于新能源的是( )A、潮汐能 B、太阳能 C、风能 D、化石能源8. 下列材料属于合金的是( )A、不锈钢 B、塑料 C、玻璃 D、陶瓷9. 下列饮品属于溶液的是( )A、蔗糖水 B、牛奶 C、果粒橙 D、豆浆10. 下列物质含有氢分子的是( )A、H2 B、H2O2 C、H2CO3 D、N2H411. 下列物质的用途中,利用其物理性质的是( )A、氧气用于炼钢 B、干冰用作制冷剂 C、乙醇用作燃料 D、氮气用作保护气12. 铝是地壳中含量最高的金属元素。元素周期表中铝元素的信息如图所示。下列关于铝原子的说法错误的是( ) A、核电荷数为13 B、质子数为13 C、核外电子数为13 D、相对原子质量为1313. 用H2O2溶液和MnO2制取O2时,一定不会用到的仪器是( )A、
A、核电荷数为13 B、质子数为13 C、核外电子数为13 D、相对原子质量为1313. 用H2O2溶液和MnO2制取O2时,一定不会用到的仪器是( )A、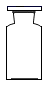 B、
B、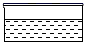 C、
C、 D、
D、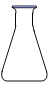 14. 下列关于空气的说法中,正确的是( )A、空气是由空气分子构成的 B、空气中氮气、氧气等分子均匀地混合在一起 C、空气中的氮气、氧气不再保持各自的化学性质 D、空气经液化、蒸发获得氧气的过程中,氮分子变成氧分子15. 下列灭火措施对应的灭火原理正确的是( )
14. 下列关于空气的说法中,正确的是( )A、空气是由空气分子构成的 B、空气中氮气、氧气等分子均匀地混合在一起 C、空气中的氮气、氧气不再保持各自的化学性质 D、空气经液化、蒸发获得氧气的过程中,氮分子变成氧分子15. 下列灭火措施对应的灭火原理正确的是( )选项
灭火措施
灭火原理
A
用灯帽盖灭酒精灯
降低着火点
B
风将蜡烛吹灭
隔绝空气
C
用锅盖盖灭着火的油锅
降低温度至着火点以下
D
将树木砍掉形成隔离带,扑灭森林火灾
移除可燃物
A、A B、B C、C D、D16. 下列实验不能达到实验目的的是( )选项
A
B
C
D
实验操作




实验目的
比较CO2和O2的密度
比较纯铜和黄铜的硬度
除去水中的泥沙
比较KMnO4在水和汽油中的溶解性
A、A B、B C、C D、D17. 下列关于N2+O2 2NO的说法错误的是( )A、表示氮气和氧气在高温条件下生成一氧化氮 B、该反应属于化合反应 C、反应前后原子数目不变 D、参加反应的氮气与氧气的质量比为1:118. 为探究铁生锈的影响因素,某兴趣小组做了如下实验。序号
①
②
③
④
实验

放置1周

放置1周

放置1周

放置1小时
现象
铁钉表面灰暗
铁钉表面光亮
铁钉表面光亮
铁钉表面光亮
下列说法正确的是( )
A、①说明铁生锈与氧气和水都有关 B、②③说明铁生锈与氧气有关 C、①②说明铁生锈与水有关 D、①④说明铁生锈与氧气浓度有关19. 在食品、药品包装中使用干燥剂,可防潮、防霉、除湿。化学干燥剂,如氧化钙干燥剂是通过与水发生化学反应而吸水;物理干燥剂,如硅胶干燥剂的内部为多孔结构,可以吸附水。下列说法错误的是( )A、干燥剂的使用可以防潮、防霉、除湿 B、氧化钙干燥剂吸水,水分子的数目发生了改变 C、硅胶干燥剂吸水,水分子的种类发生了改变 D、干燥剂吸水,既可以利用物理变化,也可以利用化学变化20. 乙烷(C2H6)是重要的化工原料,与氯气反应前后分子种类变化的微观示意图如下。下列说法正确的是( )
 A、甲中碳、氢元素质量比为1:3 B、乙的相对分子质量为71 C、甲和丙的元素组成相同 D、生成丙与丁的分子个数比为1:1
A、甲中碳、氢元素质量比为1:3 B、乙的相对分子质量为71 C、甲和丙的元素组成相同 D、生成丙与丁的分子个数比为1:1二、填空题
-
21. 2020年全国低碳日的活动主题是“绿色低碳,全面小康”。
 (1)、CO2属于(填序号)。
(1)、CO2属于(填序号)。a单质 b氧化物 c化合物
(2)、CO2过度排放会导致的环境问题有(写出1条即可)。(3)、减少化石燃料的使用可控制CO2的排放量。①化石燃料包括天然气、煤和。
②天然气的主要成分是CH4 , CH4完全燃烧的化学方程式为。
22. 水是宝贵的资源。(1)、生活中,常用来降低水的硬度的方法是。(2)、我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为。23. 烧烤中蕴含着丰富的化学原理。 (1)、用扇子扇炭火,可以让炭火更旺,原因是。(2)、食物烤制过程中香味四溢,从微观角度解释能闻到香味的原因:。24. 铁是全球年产量最高的金属。(1)、用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的原理是(用化学方程式表示)。(2)、铁锅可以用来炒菜,主要利用的铁的性质是。(3)、波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。不能用铁桶配制波尔多液的原因是(用化学方程式表示)。(4)、铁生锈的现象随处可见。防止铁生锈的措施有(写出1条即可)。
(1)、用扇子扇炭火,可以让炭火更旺,原因是。(2)、食物烤制过程中香味四溢,从微观角度解释能闻到香味的原因:。24. 铁是全球年产量最高的金属。(1)、用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的原理是(用化学方程式表示)。(2)、铁锅可以用来炒菜,主要利用的铁的性质是。(3)、波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。不能用铁桶配制波尔多液的原因是(用化学方程式表示)。(4)、铁生锈的现象随处可见。防止铁生锈的措施有(写出1条即可)。三、科普阅读题
-
25. 阅读下面科普短文。
维生素A是一种重要的营养素,具有抗氧化、调节免疫、促进生长发育等作用。维生素A只存在于动物体中,常见食物中维生素A的含量如表1所示。植物中虽不含有维生素A,但许多蔬菜、水果中含有胡萝卜素,它在小肠中可分解为维生素A。
表1每100g食物中维生素A的含量
食物种类
羊肝
牛奶
鸡蛋
河蟹
黄鱼
维生素A含量(μg/100 g)
20972
24
310
389
10
维生素A是由C、H、O元素组成的黄色固体,不溶于水,易溶于乙醇;易被氧化,特别是暴露于氧气、高温环境时,会加快这种氧化作用。因此,食品加工、生产过程会影响食品中维生素A的含量。
实验人员以不同原料为载体,模拟食品加工过程,研究了加工温度和加工时间对食品中维生素A含量的影响。实验过程中,先用维生素A标准溶液(溶剂为乙醇)对面粉进行强化处理,将处理后的面粉分别用水、鸡蛋清揉合成面团;再以此面团为研究对象,探究加工温度和加工时间对食品中维生素A含量的影响,测定结果如图1、2所示。


因此,在食品加工生产的过程中,科学地控制温度、时间对食品中维生素A的保留至关重要。
依据文章内容回答下列问题。
(1)、维生素A的物理性质有(写出1条即可)。(2)、表1所列出的几种食物中,维生素A含量最高的是。(3)、从实验设计看,涉及到的影响食品中维生素A含量的因素有加工温度、加工时间和。(4)、根据图1得出的关于加工时间对食品中维生素A含量影响的结论是。(5)、图2中,得出关于加工温度对食品中维生素A含量影响的结论,所依据的证据是。(6)、下列说法正确的是(填序号)。a维生素A是一种营养素 b维生素A中只含非金属元素
c维生素A能与氧气反应 d吃蔬菜对补充维生素A无益
四、流程题
-
26. 用冰铜(主要成分为FeS和Cu2S)为原料制备CuSO4的主要工艺流程如下:
 (1)、冰铜属于(填“纯净物”或“混合物”)。(2)、侧吹炉中发生反应:Cu2S+O2 2Cu+SO2 , 该反应所属的基本反应类型是。(3)、配平酸浸槽中反应的化学方程式:Cu+O2+H2SO4=CuSO4+H2O(4)、酸浸槽中,搅拌的目的是。27. 炼铜过程产生的烟气可用于制备硫酸,实现变废为宝,部分流程如下:
(1)、冰铜属于(填“纯净物”或“混合物”)。(2)、侧吹炉中发生反应:Cu2S+O2 2Cu+SO2 , 该反应所属的基本反应类型是。(3)、配平酸浸槽中反应的化学方程式:Cu+O2+H2SO4=CuSO4+H2O(4)、酸浸槽中,搅拌的目的是。27. 炼铜过程产生的烟气可用于制备硫酸,实现变废为宝,部分流程如下: (1)、SO2中,硫元素的化合价为。(2)、转化器中发生的反应是化合反应,反应物是SO2和空气中的。(3)、吸收塔中发生的是(填“物理”或“化学”)变化。
(1)、SO2中,硫元素的化合价为。(2)、转化器中发生的反应是化合反应,反应物是SO2和空气中的。(3)、吸收塔中发生的是(填“物理”或“化学”)变化。五、实验题
-
28. 在实验室中制取CO2 , 并验证其性质。(1)、实验室制取CO2反应的化学方程式为。(2)、下列装置中,制备、收集CO2的装置分别是、(填序号)。
 (3)、验证“CO2不支持燃烧”性质的实验操作:取一瓶收集好的CO2气体,。29. 用下图装置进行CO2的性质实验。
(3)、验证“CO2不支持燃烧”性质的实验操作:取一瓶收集好的CO2气体,。29. 用下图装置进行CO2的性质实验。 (1)、向澄清石灰水中通入CO2 , 观察到澄清石灰水变浑浊,产生该现象的原因是(用化学方程式表示)。(2)、向紫色石蕊稀溶液(由紫色石蕊和水配制而成)中通入CO2 , 观察到紫色溶液变红。
(1)、向澄清石灰水中通入CO2 , 观察到澄清石灰水变浑浊,产生该现象的原因是(用化学方程式表示)。(2)、向紫色石蕊稀溶液(由紫色石蕊和水配制而成)中通入CO2 , 观察到紫色溶液变红。①上述实验(填“能”或“不能”)得出“CO2可以和H2O发生反应”的结论,理由是。
②加热该红色溶液,可观察到的现象是。
30. 分别将盛有白磷、红磷的试管放入盛有80℃热水的,大烧杯中(如图),验证可燃物燃烧的条件。(已知:白磷的着火点为40℃,红磷的着火点为240℃。) (1)、实验过程中发现,试管1中红磷不燃烧,试管2中白磷燃烧,由此可验证的可燃物燃烧条件是。(2)、验证可燃物燃烧的另一个条件,需继续进行的实验操作是。31. 某兴趣小组同学进行如下图所示的2个实验。
(1)、实验过程中发现,试管1中红磷不燃烧,试管2中白磷燃烧,由此可验证的可燃物燃烧条件是。(2)、验证可燃物燃烧的另一个条件,需继续进行的实验操作是。31. 某兴趣小组同学进行如下图所示的2个实验。 (1)、实验1能验证质量守恒定律。
(1)、实验1能验证质量守恒定律。①红磷燃烧的化学方程式为。
②反应前称得质量为m1 , 红磷充分燃烧后冷却,称得质量为m2 , m1m2(填“>”“=”或“<”)。
③从微观角度分析,化学反应一定符合质量守恒定律的原因是。
(2)、实验2不能验证质量守恒定律,原因是。32. 用下图所示装置研究铝和铜的化学性质。实验装置
实验步骤

I 检查装置的气密性;
II 打开K1 , 关闭K2 , 用注射器向A中注入过量稀硫酸,直至液面浸没A中右侧导管口;
III 打开K2 , 关闭K1
(1)、用砂纸打磨铝片的目的是。(2)、检查装置气密性的操作;向B中加入蒸馏水至浸没导管口,关闭K1 , 打开K2 , 。(3)、步骤II,A中可以观察到的现象有。(4)、步骤III,A中液体进入B后,未观察到明显现象,原因是。六、科学探究题
-
33. 碘酸钾(KIO3)为白色固体,可溶于水,常作为补碘剂被添加到食盐中。小组同学实验探究其性质。(1)、(进行实验1)用下图装置完成实验,探究KIO3的热稳定性。记录如下:
序号
1-1
1-2
装置


现象
加热较长时间后,产生大量气泡
带火星的木条复燃
(解释与结论)
实验1-1结束时,应进行的操作是先 , 后。
(2)、1-2中现象说明,1-1中收集到的气体是。(3)、由实验1可知,KIO3受热(填“能”或“不能”)分解。(4)、(进行实验2)按下表数据、用下图装置进行实验,探究KIO3与维生素C的反应及其影响因素,记录如下表。资料:淀粉溶液遇I2变为蓝色,遇KIO3、维生素C(化学式为C6H8O6)、醋酸(化学式为C2H4O2)不变色。
装置
序号
溶液中溶质的质量/g
实验现象
KIO3
维生素C

2-1
0.1
0.1
溶液立即由无色变为蓝色
2-2
0.005
0.005
溶液逐渐由无色变为蓝色
2-3
0.0025
0.0025
一段时间后溶液无明显变化,再滴入5滴稀醋酸后,溶液逐渐变为浅蓝色
(解释与结论)
实验2-1中,KIO3溶液与维生素C溶液的溶质质量分数(填“相等”或“不相等”)。
(5)、对比实验2-1、2-2,可探究的影响KIO3与维生素C反应的因素是。(6)、由上述实验得到结论“KIO3能与维生素C反应生成I2”,实验证据是。(7)、(反思与评价)甲同学由实验2-3得出结论:醋酸会促进KIO3与维生素C的反应;乙同学认为不严谨,理由是。
七、计算题
-
34. 砂子主要成分是二氧化硅(SiO2)。人们以砂子为原料,先制成粗硅,然后提纯制成高纯硅,再用高纯硅制造集成电路。生产粗硅的化学反应如下:2C+SiO2 Si+2CO↑(1)、二氧化硅中,硅、氧原子个数比为。(2)、生成的Si与CO的质量比为。(3)、若所用砂子中SiO2的的质量分数为60%,则:
①200t砂子中SiO2的质量为t。
②请补全下列计算过程,求出用200t砂子理论上最多能生成的Si的质量。
解:设理论上最多能生成Si的质量为x。
x=(_)t
答:理论上最多能生成Si的质量为 t。
-
-