北京市昌平区2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-03-04 类型:期末考试
一、单选题
-
1. 空气成分中,体积分数最大的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体2. 地壳中含量最多的元素是( )A、硅 B、氧 C、铁 D、铝3. 下列属于氧化物的是( )A、O2 B、SO2 C、KCl D、NaOH4. 下列物质属于纯净物的是( )A、酱油 B、蒸馏水 C、碘酒 D、洁净的空气5. 下列食物富含蛋白质的是( )A、米饭 B、黄瓜 C、牛肉 D、苹果6. 为了防止骨质疏松,人体必须摄入的元素是( )A、钙 B、铁 C、锌 D、碘7. 下列物质加入水中,能形成溶液的是( )A、沙子 B、食盐 C、植物油 D、面粉8. 能够引起温室效应的主要气体是()A、O2 B、N2 C、H2 D、CO29. 下列物质通常不会损害人体健康的是( )A、一氧化碳 B、黄曲霉素 C、甲醛 D、水10. 废弃的易拉罐和塑料瓶属于( )A、厨余垃圾 B、其他垃圾 C、可回收物 D、有害垃圾11. 下列情况不会造成空气污染的是( )A、汽车排出的尾气 B、烧煤取暖 C、植物的光合作用 D、工厂排出的废气12. 下列实验操作正确的是( )A、
 倾倒液体
B、
倾倒液体
B、 检查气密性
C、
检查气密性
C、 加热液体
D、
加热液体
D、 过滤
13. 下列物质中,含有氧分子的是( )A、O2 B、MnO2 C、CO2 D、H2O214. 下列清洗方法中,利用乳化原理的是( )A、用自来水洗手 B、用洗涤剂清洗餐具 C、用盐酸除水垢 D、用汽油清洗油污15. 将木柴架空一些,可以使火燃烧更旺,这样做的目的是( )A、方便添加木柴 B、升高木柴的温度 C、木柴与空气充分接触 D、降低木柴的着火点16. “冰墩墩”是2022年北京冬奥会的吉祥物,某“冰墩墩”玩具的外用材料为纯羊毛,内充物为聚酯纤维,区别纯羊毛和聚酯纤维的最好方法是( )
过滤
13. 下列物质中,含有氧分子的是( )A、O2 B、MnO2 C、CO2 D、H2O214. 下列清洗方法中,利用乳化原理的是( )A、用自来水洗手 B、用洗涤剂清洗餐具 C、用盐酸除水垢 D、用汽油清洗油污15. 将木柴架空一些,可以使火燃烧更旺,这样做的目的是( )A、方便添加木柴 B、升高木柴的温度 C、木柴与空气充分接触 D、降低木柴的着火点16. “冰墩墩”是2022年北京冬奥会的吉祥物,某“冰墩墩”玩具的外用材料为纯羊毛,内充物为聚酯纤维,区别纯羊毛和聚酯纤维的最好方法是( ) A、闻气味 B、摸手感 C、是否溶于水 D、燃烧法17. 下列操作中,能鉴别空气、氧气和二氧化碳3瓶气体的是 ( )A、观察气体颜色 B、插入燃着的木条 C、闻气体的气味 D、倒入澄清石灰水18. 下列突发事件处理方法正确的是( )A、房间着火,立即开窗通风 B、煤气泄漏,立即开灯查看 C、电器着火,立即用水浇灭 D、油锅着火,立即盖上锅盖19. 下列做法中,不利于保护水资源的是( )
A、闻气味 B、摸手感 C、是否溶于水 D、燃烧法17. 下列操作中,能鉴别空气、氧气和二氧化碳3瓶气体的是 ( )A、观察气体颜色 B、插入燃着的木条 C、闻气体的气味 D、倒入澄清石灰水18. 下列突发事件处理方法正确的是( )A、房间着火,立即开窗通风 B、煤气泄漏,立即开灯查看 C、电器着火,立即用水浇灭 D、油锅着火,立即盖上锅盖19. 下列做法中,不利于保护水资源的是( )
A、使用节水型马桶 B、合理使用农药和化肥 C、生活污水任意排放 D、工业废水处理达标后排放20. 下列化学符号正确的是( )A、2个氢原子:2H B、2个氮分子:N2 C、钙离子: D、氧化铝:AlO21. 下列物质的用途,主要利用其化学性质的是( )A、石墨用作电极 B、氧气用于气焊 C、干冰用作人工降雨 D、稀有气体用作霓虹灯22. 下图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列有关该实验的说法中,正确的是( ) A、红磷熄灭后应立刻打开弹簧夹 B、点燃红磷前先用弹簧夹夹紧乳胶管 C、最终瓶中剩余的气体是纯净的氮气 D、实验时,只取用极少量红磷,可减少污染且不影响实验结果23. 用如图进行实验,下列说法错误的是( )
A、红磷熄灭后应立刻打开弹簧夹 B、点燃红磷前先用弹簧夹夹紧乳胶管 C、最终瓶中剩余的气体是纯净的氮气 D、实验时,只取用极少量红磷,可减少污染且不影响实验结果23. 用如图进行实验,下列说法错误的是( ) A、能证明分子在不断运动 B、浓盐酸与浓氨水都具有挥发性 C、氯化氢分子比氨分子运动得快 D、实验过程中发生了化学变化24. 为了探究“二氧化碳与水反应生成了酸性物质”应做的实验是(图中的小花为浸润过石蕊后烘干的纸花)( )
A、能证明分子在不断运动 B、浓盐酸与浓氨水都具有挥发性 C、氯化氢分子比氨分子运动得快 D、实验过程中发生了化学变化24. 为了探究“二氧化碳与水反应生成了酸性物质”应做的实验是(图中的小花为浸润过石蕊后烘干的纸花)( ) A、①④ B、③④ C、②③④ D、①②③④25. 氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下。下列说法错误的是( )
A、①④ B、③④ C、②③④ D、①②③④25. 氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下。下列说法错误的是( )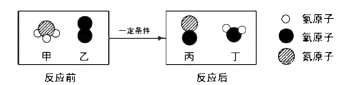 A、甲中氮、氢原子个数比为1:3 B、乙的相对分子质量为32 C、两种生成物均为化合物 D、生成的丙与丁的分子个数比为1:2
A、甲中氮、氢原子个数比为1:3 B、乙的相对分子质量为32 C、两种生成物均为化合物 D、生成的丙与丁的分子个数比为1:2二、填空题
-
26. 能源和人们的生产生活息息相关。(1)、目前人们使用的燃料大多数来自化石燃料。化石燃料包括天然气、煤、。(2)、天然气的主要成分是甲烷,甲烷燃烧的化学方程式为。(3)、化石燃料不可再生,目前人们正在积极开发和利用许多新能源,请例举一种。27. 2020年的中国,科技技术上再次有了质的飞跃,我们潜渊登峰、探月追星。(1)、“奋斗者”号下潜突破万米。载人仓采用新型高强度钛合金,钛在元素周期表中信息如图所示:

①钛属于(填“金属”或“非金属”)元素。
②一个钛原子核外有个电子。
(2)、中国珠峰高程测量登山队成功测得珠峰最新高程为8848.86米。为帮助登山人员解决呼吸困难的问题,应携带的物质是(填字母序号)A氢气B氧气C二氧化碳
(3)、嫦娥五号开启我国首次地外天体采样。“月球制氧机”可利用聚焦太阳能产生的高温加热月球土壤,制得氧气,可推测月球土壤中一定含有氧元素的依据是。28. 如图表是硝酸钾固体在不同温度时的溶解度,回答以下问题。温度/℃
0
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
(1)、硝酸钾溶液中的溶剂是。(2)、20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到(填“饱和”或“不饱和”)溶液。(3)、20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是。(4)、如图所示,小烧杯中盛放的是(2)中所得的硝酸钾溶液。若将下列物质分别缓慢地加入到大烧杯的水中,不断搅拌,能够使小烧杯中有固体析出的是。(填字母序号)
A冰 B硝酸铵 C干冰 D氢氧化钠
29. 电解水实验如下图所示。 (1)、试管2中生成的气体为。(2)、该反应的化学方程式为。30. 在农业生产中,常用溶质的质量分数为16%的NaCl溶液来选种。实验室配制100g此溶液:(1)、称量固体的质量为g。(2)、溶解用到的玻璃仪器是。(3)、在如图的标签中填上相应的内容。
(1)、试管2中生成的气体为。(2)、该反应的化学方程式为。30. 在农业生产中,常用溶质的质量分数为16%的NaCl溶液来选种。实验室配制100g此溶液:(1)、称量固体的质量为g。(2)、溶解用到的玻璃仪器是。(3)、在如图的标签中填上相应的内容。
三、科普阅读题
-
31. 阅读下面科普短文。
醋是酸味调味品,有效成分是乙酸,俗称醋酸,化学式为CH3COOH。用含碳水化合物(糖、淀粉)的液体转化成酒精(乙醇,化学式为C2H5OH)和二氧化碳,酒精再受某种细菌的作用与空气中氧气结合生成醋酸和水。食醋的味酸而醇厚,液香而柔和,在中国使用已有近3000年的历史。食醋中所含醋酸的量一般是5~8%。柿子醋是一种用成熟柿子酿造出来的醋,营养丰富,具有抗菌、消炎、降血糖、降血压的功效。柿子醋制作工艺流程如下:

柿浆流动性差,会造成加人的酵母菌、醋酸菌不能与柿浆充分接触,影响菌种活力,通过加入水将柿浆稀释。加水量对柿子醋产率的影响,数据如图所示:

依据文章内容回答下列问题。
(1)、乙醇(C2H5OH)、乙酸( CH3COOH)是(填“有机化合物”或“无机化合物”)。(2)、乙醇(C2H5OH)中有种元素。(3)、乙酸(CH3COOH)相对分子质量的计算式为。(4)、由图中数据可知,加水量对柿子醋产率的影响为。(5)、下列说法正确的是(填字母序号)。A酿醋先酿酒
B食醋是中国传统的调味品
C高血压、高血糖患者适宜选择柿子醋作为调味品
D柿子醋制作过程中的酵母菌和醋酸菌可以相互替代使用
四、流程题
-
32. 某净水厂正式通水后,南水北调的长江水替换了当地的高氟地下水作为生产和生活用水的主要水源。该厂的净水工艺流程如图:
 (1)、某种净水絮凝剂可由氯化铝(AlCl3)制得,氯化铝属于(填“单质”或“化合物”)。(2)、活性炭的主要作用是。(3)、长期饮用硬水对人体健康不利。区分硬水和软水的试剂是(填字母序号)。
(1)、某种净水絮凝剂可由氯化铝(AlCl3)制得,氯化铝属于(填“单质”或“化合物”)。(2)、活性炭的主要作用是。(3)、长期饮用硬水对人体健康不利。区分硬水和软水的试剂是(填字母序号)。A肥皂水 B食盐水
(4)、消毒药剂 NaClO中,氯元素的化合价是。(5)、NaClO的生产方法之一是氯气(Cl2)与氢氧化钠(NaOH)溶液反应,同时生成氯化钠和水。请你写出反应的化学方程式。五、实验题
-
33. 根据如图回答问题。
 (1)、实验室制取氧气时,选用的收集装置是(填字母序号,下同)。如图A所示,用高锰酸钾制取氧气的化学方程式为。如图E所示,铁丝与氧气反应的现象为。(2)、实验室用大理石和稀盐酸制取二氧化碳的化学方程式为 , 选用的发生装置是。如图F所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是。34. 如图是探究可燃物燃烧条件的实验,向C中加入少量白磷,再加入热水,塞好胶塞,使导管口浸入热水中,白磷不燃烧。打开K1 , 将A中溶液滴入B中,C中有气泡冒出,白磷燃烧。
(1)、实验室制取氧气时,选用的收集装置是(填字母序号,下同)。如图A所示,用高锰酸钾制取氧气的化学方程式为。如图E所示,铁丝与氧气反应的现象为。(2)、实验室用大理石和稀盐酸制取二氧化碳的化学方程式为 , 选用的发生装置是。如图F所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是。34. 如图是探究可燃物燃烧条件的实验,向C中加入少量白磷,再加入热水,塞好胶塞,使导管口浸入热水中,白磷不燃烧。打开K1 , 将A中溶液滴入B中,C中有气泡冒出,白磷燃烧。 (1)、B中发生反应的化学方程式为。(2)、此实验运用对比的方法研究了燃烧的一个条件,它是。35. 如图是探究“质量守恒定律”的实验过程,回答下列问题:
(1)、B中发生反应的化学方程式为。(2)、此实验运用对比的方法研究了燃烧的一个条件,它是。35. 如图是探究“质量守恒定律”的实验过程,回答下列问题:序号
实验装置
实验操作及现象
实验1

向澄清石灰水中通入二氧化碳,电子秤示数增大
实验2

点燃蜡烛,电子秤示数减小
(1)、实验1中,发生反应的化学方程式为。(2)、实验2中,点燃蜡烛后,电子秤示数逐渐减小。蜡烛减小的质量(填“大于”“等于”或“小于”)燃烧后生成物的总质量。六、科学探究题
-
36. 在研究化学反应伴随热量变化实验时,有的同学发现镁和铁都可以与酸反应,但反应的快慢有明显差异,提出问题并进行探究。
(提出问题)酸的浓度、金属的种类、金属的形状是否会影响金属与酸反应的快慢?
(进行实验)分别取20mL盐酸、2g金属。
实验编号
盐酸的浓度
金属种类
金属形状
收集50mL氢气所需时间/s
①
10%
镁
粉末
60
②
10%
铁
片状
120
③
10%
镁
片状
102
④
20%
铁
片状
110
(解释与结论)
(1)、镁与盐酸反应的实验现象是固体逐渐消失、放出大量热、。(2)、镁、铁与盐酸发生的反应相似(都生成+2价的化合物),补全化学反应方程式:(3)、对比实验①和③,得到的结论是。(4)、要比较不同种类的金属对反应快慢的影响,应选择的实验编号是。(5)、由上述实验可推知,影响金属与酸反应快慢的因素是。(6)、(反思与评价)该实验除了用收集等体积氢气所用时间来衡量反应的快慢外,其他实验方法是。
七、计算题
-
37. 氢气是最清洁的燃料,计算200g氢气完全燃烧消耗氧气的质量。
-
-
-