北京市密云区2019年中考化学一模试卷
试卷更新日期:2021-03-01 类型:中考模拟
一、单选题
-
1. 缺少下列元素会导致少年患佝偻病的是( )A、锌 B、铁 C、钙 D、碘2. 下列“水”能使无色酚酞溶液变红的是( )A、石灰水 B、汽水 C、冰水 D、食盐水3. 下列物质属于氧化物的是( )A、O2 B、CaO C、KMnO4 D、H2SO44. 下列物质俗称与化学式对应正确的是( )A、纯碱NaCl B、干冰-H2O C、苛性钠-NaOH D、生石灰-Ca(OH)25. 下列金属中,滴加稀盐酸后不会产生气泡的是( )A、锌 B、铝 C、铁 D、铜6. 铀是一种重要的工业原料,已知有一种铀原子中质子数为92,中子数为143,该原子的核外电子数为( )A、143 B、92 C、235 D、517. 我国自主研发的龙芯CPU已经应用于包括北斗卫星在内的十几种国家重器中,芯片作为所有电脑、智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。用化学方法制高纯硅的反应原理为:①2C+SiO2═2CO↑+Si(粗硅)②Si+2Cl2 SiCl4(液态)③2H2+SiCl4 4HCl+Si(高纯硅)。其中属于置换反应的是( )A、① B、①② C、②③ D、①③8. 下图所示的实验操作错误的是( )A、倾倒液体
 B、取用固体
B、取用固体  C、点燃酒精灯
C、点燃酒精灯  D、溶解固体
D、溶解固体  9. 纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法错误的是( )
9. 纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法错误的是( ) A、纳米铁粉燃烧的化学方程式为3Fe+2O2 Fe3O4 B、水可防止生成物溅落炸裂瓶底 C、激光手电照射使纳米铁粉的着火点降低 D、气球先膨胀后又变小10. 下图所示的四个实验中,不能达到实验目的的是( )
A、纳米铁粉燃烧的化学方程式为3Fe+2O2 Fe3O4 B、水可防止生成物溅落炸裂瓶底 C、激光手电照射使纳米铁粉的着火点降低 D、气球先膨胀后又变小10. 下图所示的四个实验中,不能达到实验目的的是( )



A.证明氨分子在不断运动
B.检查装置的气密性
C.探究燃烧需要温度达到着火点
D.证明水由氢元素、氧元素组成
A、A B、B C、C D、D二、选择题组
-
11. 20℃时,将20g a、b两种固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。(1)、图中所示一定是饱和溶液的是( )
 A、20℃时的A溶液 B、20℃时的B溶液 C、50℃时的A溶液 D、50℃时的B溶液(2)、50℃时a溶液的溶质质量分数为( )A、20% B、16.7% C、28.6% D、24.2%
A、20℃时的A溶液 B、20℃时的B溶液 C、50℃时的A溶液 D、50℃时的B溶液(2)、50℃时a溶液的溶质质量分数为( )A、20% B、16.7% C、28.6% D、24.2%三、填空题
-
12. 滑雪是同学们喜爱的冬季运动项目,滑雪场主要是利用造雪机来制造人工雪。造雪机的工作原理如图所示。
 (1)、B到C发生的是变化(填“物理”或“化学”)。(2)、A处空气被压缩,体积变小。从微粒的角度解释其原因是。13. 在导致全球气候变暖的“温室气体”中,二氧化碳的贡献为55%。因此,开展对二氧化碳的资源化利用的研究至关重要。研究发现:将乙烷(C2H6)和二氧化碳在一定条件下发生转化,可使制得乙烯(C2H4和一氧化碳,而乙烯是在国民经济中占有重要地位的工业原料,具有一定的经济效益和社会效益。此反应的微观示意图如下所示:
(1)、B到C发生的是变化(填“物理”或“化学”)。(2)、A处空气被压缩,体积变小。从微粒的角度解释其原因是。13. 在导致全球气候变暖的“温室气体”中,二氧化碳的贡献为55%。因此,开展对二氧化碳的资源化利用的研究至关重要。研究发现:将乙烷(C2H6)和二氧化碳在一定条件下发生转化,可使制得乙烯(C2H4和一氧化碳,而乙烯是在国民经济中占有重要地位的工业原料,具有一定的经济效益和社会效益。此反应的微观示意图如下所示: (1)、在
(1)、在 中将隐藏的微粒模型画出来。 (2)、要制备56kg的乙烯,可消耗二氧化碳kg。
中将隐藏的微粒模型画出来。 (2)、要制备56kg的乙烯,可消耗二氧化碳kg。四、科学探究题
-
14. 2018年2月9日,歼-20开始列装我国空军作战部队。它是一款具备高隐身性战斗机。其隐身材料是目前最新的纳米高分子复合材料。间苯二胺(C6H8N2)是生产这种材料的重要原料之一,试回答:
 (1)、间苯二胺由种元素组成。(2)、间苯二胺中,碳元素和氢元素的质量之比为(最简整数比)。15. 小峰同学在体育课上腿部擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
(1)、间苯二胺由种元素组成。(2)、间苯二胺中,碳元素和氢元素的质量之比为(最简整数比)。15. 小峰同学在体育课上腿部擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢? (1)、I.小峰准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
(1)、I.小峰准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。请写出过氧化氢分解的化学方程式。
(2)、若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到 , 说明生成的气体是氧气。(3)、II.小峰查阅了相关资料,并进行了探究实验(查阅资料)
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号
实验步骤
实验现象
实验结论
①
分两次进行实验,均注入5mL过氧化氢溶液
第一次在常温下进行
第二次将试管浸在37℃的温水中
量筒中2分钟收集到的气体体积均为5mL
②
分两次进行实验
第一次……
第二次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液
第一次,量筒中2分钟收集到的气体体积为5mL
第二次,量筒中2分钟收集到的气体体积为……..ml
过氧化氢分解加快是因为过氧化氢酶的作用
实验①得出的结论是。
(4)、实验②中“第一次”应进行的操作是。(5)、实验②中第二次收集到的氧气体积为mL。(6)、(实验反思)小峰反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶
不加过氧化氢酶
反应温度/℃
25
37
42
25
37
42
收集到气体体积/mL
39
56
34
5
5
5
通过这些数据,你能得出的新结论是
五、科普阅读题
-
16. 阅读下面科普短文(原文作者:董丽颖、张永刚等,原文有删改)
传统纸质纤维的易燃性是众多纸质文物损毁消失的一个主要原因。探索基于无机材料的新型耐火纸成为重要的研究课题。
羟基磷灰石(HAP)是一种天然矿物质,其组成可表示为Ca5(PO4)3(OH),呈现白色,是制造耐火纸的一种理想原料。
早期制备的HAP纳米线长度较短,一般小于10p*m,柔韧性较差。后经改进,制得的HAP超长纳米线的直径约为10nm,长度在几十微米到100ptm之间,具有超长的长度和超高的长径比,从而具有高柔韧性。
用HAP超长纳米线制备的新型无机耐火纸具有高柔韧性,可以任意卷曲,可耐高温,不燃烧,并且具有优良的书写和打印功能。这样的耐火纸有望应用于书籍、重要文件及档案的长久安全保存。
研究者还发现,HAP超长纳米线耐火纸对多种有机污染物具有较高的吸附量,可以用于处理废水,其对水中有机物的吸附量如图(a)所示;用回收的耐火纸再次吸附有机物,循环使用5次,每次的吸附量如图(b)所示。

近来,一种对PM:细颗粒物有吸附作用的新型HAP超长纳米线被研发出来,并制成口罩的滤芯,这种材料有望在空气净化领域发挥作用。
依据文章内容回答下列问题。
(1)、根据“Ca5(PO4)3(OH)是制造耐火纸的一种理想原料”可推测其具有的化学性质是。(2)、与传统纸张相比,HAP超长纳米线制成纸张的优点是(写出一个即可)。(3)、HAP超长纳米线耐火纸对氯仿的吸附量可以达到g•g-1(结果取整数)。(4)、吸附有机污染物时,HAP超长纳米线耐火纸(填“能”或“不能”)重复使用。(5)、下列说法合理的是(填字母序号)。A HAP纳米线的长度对耐火纸的柔韧性有较大影响
B HAP超长纳米线耐火纸难溶于水
C HAP超长纳米线耐火纸只对氯仿有吸附作用
六、简答题
-
17. 高纯氧化铁[Fe2O3]又称“引火铁”,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程示意图。
小贴士:氨水呈碱性(主要成分NH3•H2O是一种碱);(NH4)2CO3溶液呈碱性,40℃以上易分解。
 (1)、①处发生反应的化学方程式为。(2)、加入(NH4)2CO3后,该反应必须控制的条件是。
(1)、①处发生反应的化学方程式为。(2)、加入(NH4)2CO3后,该反应必须控制的条件是。七、流程题
-
18. “打好蓝天保卫战、治理大气污染”是提升人民生活质量的重要工作。二氧化硫(SO2)是一种大气污染物。工业上可以利用海水对二氧化硫进行吸收利用,变害为宝。其工艺流程见图:
 (1)、流程中将石灰石加水制成石灰石浆的目的是。(2)、其中硫元素的化合价在反应前后的变化为。.(3)、为了提升脱硫率(脱硫率是指已除去的二氧化硫的量占总二氧化硫量的百分比)与温度、烟气中SO2浓度的关系,技术人员进行了探究实验。实验结果如下:
(1)、流程中将石灰石加水制成石灰石浆的目的是。(2)、其中硫元素的化合价在反应前后的变化为。.(3)、为了提升脱硫率(脱硫率是指已除去的二氧化硫的量占总二氧化硫量的百分比)与温度、烟气中SO2浓度的关系,技术人员进行了探究实验。实验结果如下:实验序号
温度/℃
烟气中SO2浓度/10-2g•L-1
脱硫率
Ⅰ
23
2.5%
99.5
Ⅱ
23
3.2%
97.1
Ⅲ
40
2.5%
94.3
由表中实验数据可得出的结论是。
八、实验题
-
19. 看图并请从A或B两题中任选1个作答,若两题均作答,只一组计分。

A
B
⑴用装置A制备一瓶氧气,其制备原理为(写出化学反应的方程式)。
⑵氧气可用C装置收集,还可以用收集(填写装置编号)。
⑴装置B可用于实验室制取二氧化碳。写出制取CO2反应的化学方程式为。
⑵收集二氧化碳可选择(填写装置编号)。
20. “水”在化学实验室中是经常用到的一种试剂,以下图示实验中都用到了水。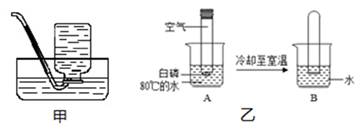 (1)、如图甲,用此装置收集氧气前要将集气瓶中灌满水,其目的是。(2)、如图乙装置可用来测定空气中氧气的含量。实验进行到“B”环节可看到的现象是;A烧杯中“80℃热水”的作用是。21. 如图,化学小组同学制作了一个微型实验装置用来验证二氧化碳的性质。异型玻璃管A内充满了二氧化碳气体(已检查装置气密性),注射器B内吸取了一定量的浓氢氧化钠溶液,广口瓶C中盛有一定量稀盐酸。实验开始前止水夹K处于关闭状态。
(1)、如图甲,用此装置收集氧气前要将集气瓶中灌满水,其目的是。(2)、如图乙装置可用来测定空气中氧气的含量。实验进行到“B”环节可看到的现象是;A烧杯中“80℃热水”的作用是。21. 如图,化学小组同学制作了一个微型实验装置用来验证二氧化碳的性质。异型玻璃管A内充满了二氧化碳气体(已检查装置气密性),注射器B内吸取了一定量的浓氢氧化钠溶液,广口瓶C中盛有一定量稀盐酸。实验开始前止水夹K处于关闭状态。 (1)、将注射器中氢氧化钠溶液全部推入A中之前要进行的操作是。(2)、当C中部分液体流入A中后迅速关闭止水夹K,片刻后可看到的现象是。22. 某小组同学利用如图所示装置探究铁生锈的条件。
(1)、将注射器中氢氧化钠溶液全部推入A中之前要进行的操作是。(2)、当C中部分液体流入A中后迅速关闭止水夹K,片刻后可看到的现象是。22. 某小组同学利用如图所示装置探究铁生锈的条件。 (1)、要证明铁生锈与氧气有关,需要进行的实验操作为。(2)、实验中能说明铁生锈与水有关的实验现象是。(3)、充分反应后,将装置A、B中分别注入少量稀盐酸,两个广口瓶中现象的不同点是: , 由此也可以证明铁丝生锈情况。A中反应的化学方程式是。
(1)、要证明铁生锈与氧气有关,需要进行的实验操作为。(2)、实验中能说明铁生锈与水有关的实验现象是。(3)、充分反应后,将装置A、B中分别注入少量稀盐酸,两个广口瓶中现象的不同点是: , 由此也可以证明铁丝生锈情况。A中反应的化学方程式是。
-
-
-
-