初中化学第一轮复习第一部分 专题1 溶解度和溶解曲线
试卷更新日期:2021-03-01 类型:一轮复习
一、单选题
-
1. 甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是( )
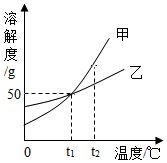 A、甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 B、t1℃时,甲、乙的溶解度均为50g C、t2℃时,将甲、乙两种物质的饱和溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 D、t1℃时,甲、乙溶液中溶质的质量分数不一定相等2. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )
A、甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 B、t1℃时,甲、乙的溶解度均为50g C、t2℃时,将甲、乙两种物质的饱和溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 D、t1℃时,甲、乙溶液中溶质的质量分数不一定相等2. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )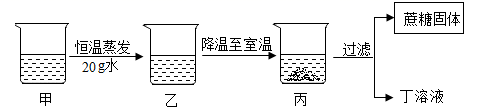 A、甲一定是不饱和溶液 B、甲和丙的溶质质量分数一定不相等 C、丙和丁一定是饱和溶液 D、乙的溶质质量分数一定比甲大3. 如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
A、甲一定是不饱和溶液 B、甲和丙的溶质质量分数一定不相等 C、丙和丁一定是饱和溶液 D、乙的溶质质量分数一定比甲大3. 如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )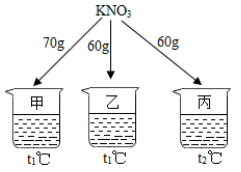
温度(℃)
t1
t2
KNO3的溶解度(g/100g水)
60
90
A、甲、乙混合后为t1℃的不饱和溶液 B、乙升温至t2℃,溶液质量增加 C、乙、丙溶液中溶质质量相等 D、丙降温至t1℃,有晶体析出4. 不随水的质量改变的是( )A、物质的溶解度 B、溶质质量分数 C、溶液的 pH 值 D、饱和溶液的状态5. 如图是 a、b、c 三种固体物质的溶解度曲线,下列叙述正确的是( )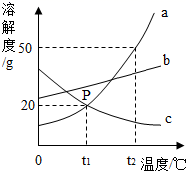 A、将 a、b、c 三种物质 t1℃时的饱和溶液升温至 t 2℃,所得溶液的溶质质量分数大小关系是 a>b>c B、t2℃时 30g 物质 a 加入到 50g 水中不断搅拌,形成 80g 溶液 C、t1℃时 a、b、c 三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是 b>a=c D、若 a 中混有少量 c,可以采用冷却热饱和溶液的方法提纯 a6. 如图是甲、乙、两三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( )
A、将 a、b、c 三种物质 t1℃时的饱和溶液升温至 t 2℃,所得溶液的溶质质量分数大小关系是 a>b>c B、t2℃时 30g 物质 a 加入到 50g 水中不断搅拌,形成 80g 溶液 C、t1℃时 a、b、c 三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是 b>a=c D、若 a 中混有少量 c,可以采用冷却热饱和溶液的方法提纯 a6. 如图是甲、乙、两三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( )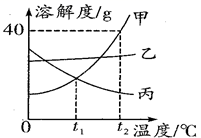 A、甲和丙的溶解度相等 B、在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g C、将t2℃时,甲的溶液降温到t1℃,一定有晶体析出 D、将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是乙>甲>丙7. 下列对“20℃时的溶解度为31.6g”的解释正确的是( )A、20℃时,31.6g溶解在水中 B、20℃时,100g溶液中含有31.6g C、3l.6g溶解在100g水中达到饱和状态 D、20℃时,31.6g溶解在100g水中达到饱和状态8. X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )
A、甲和丙的溶解度相等 B、在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g C、将t2℃时,甲的溶液降温到t1℃,一定有晶体析出 D、将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是乙>甲>丙7. 下列对“20℃时的溶解度为31.6g”的解释正确的是( )A、20℃时,31.6g溶解在水中 B、20℃时,100g溶液中含有31.6g C、3l.6g溶解在100g水中达到饱和状态 D、20℃时,31.6g溶解在100g水中达到饱和状态8. X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )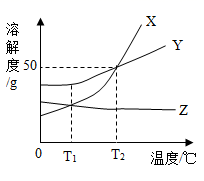 A、Y的溶解度为50g B、T2℃时,X、Y两种物质的溶解度相等 C、T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液9. 如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是( )
A、Y的溶解度为50g B、T2℃时,X、Y两种物质的溶解度相等 C、T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液9. 如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是( )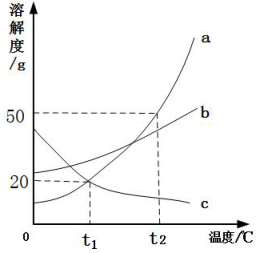 A、使a、c的饱和溶液析出晶体的方法都可以是降温结晶 B、t1℃时,a、c两种物质的溶液的溶质质量分数一定相等 C、在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80g D、t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c10. 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
A、使a、c的饱和溶液析出晶体的方法都可以是降温结晶 B、t1℃时,a、c两种物质的溶液的溶质质量分数一定相等 C、在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80g D、t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c10. 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )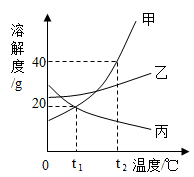 A、三种物质的溶解度都随温度升高而增大 B、t1℃时20g丙加入50g水中,充分搅拌得到70g溶液 C、甲的饱和溶液中混有少量乙,可通过降温结晶获得较纯净的甲 D、t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中甲和丙的溶质质量分数相等11. 甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( )
A、三种物质的溶解度都随温度升高而增大 B、t1℃时20g丙加入50g水中,充分搅拌得到70g溶液 C、甲的饱和溶液中混有少量乙,可通过降温结晶获得较纯净的甲 D、t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中甲和丙的溶质质量分数相等11. 甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( )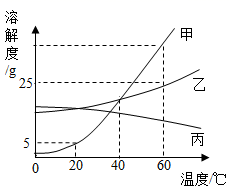 A、甲是易溶物 B、60℃时,将等质量的甲、乙饱和溶液降温至40℃,溶液的质量乙>甲 C、60℃时,将100g乙的饱和溶液配成质量分数为5%的溶液,需加水380g D、甲中混有少量丙,若要得到较纯净的甲,常采用蒸发结晶的方法12. 甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A、甲是易溶物 B、60℃时,将等质量的甲、乙饱和溶液降温至40℃,溶液的质量乙>甲 C、60℃时,将100g乙的饱和溶液配成质量分数为5%的溶液,需加水380g D、甲中混有少量丙,若要得到较纯净的甲,常采用蒸发结晶的方法12. 甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )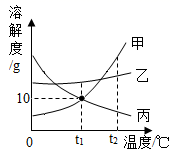 A、甲和丙都属于易溶物质 B、溶解度大小关系:甲>乙>丙 C、等质量甲、乙两种物质的溶液从t2℃降到t1℃时,析出晶体最多的是甲 D、三种物质的饱和溶液从t2℃降到t1℃,所得溶液溶质质量分数:乙>甲>丙13. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A、甲和丙都属于易溶物质 B、溶解度大小关系:甲>乙>丙 C、等质量甲、乙两种物质的溶液从t2℃降到t1℃时,析出晶体最多的是甲 D、三种物质的饱和溶液从t2℃降到t1℃,所得溶液溶质质量分数:乙>甲>丙13. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )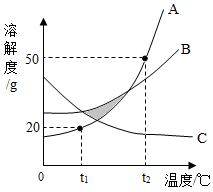 A、阴影区域中,A,C均处于不饱和状态 B、除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B C、将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>B D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%14. 硝酸钾的溶解度曲线如图所示,将100g60℃的KNO3饱和溶液分别进行如下操作后,所得溶液与原溶液相比,变化结果完全正确的是( )
A、阴影区域中,A,C均处于不饱和状态 B、除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B C、将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>B D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%14. 硝酸钾的溶解度曲线如图所示,将100g60℃的KNO3饱和溶液分别进行如下操作后,所得溶液与原溶液相比,变化结果完全正确的是( )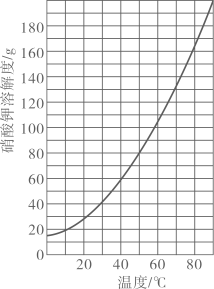
选项
操作
溶质质量
溶液质量
溶质的质量分数
KNO3的溶解度
A
升温
变大
变大
不变
变大
B
降温
变小
变小
不变
变小
C
加入KNO3固体
不变
变大
变大
变大
D
恒温蒸发部分水
变小
变小
不变
不变
A、A B、B C、C D、D15. 如图为Ca(OH)2的溶解度曲线;如表为20℃时溶解度的相对大小。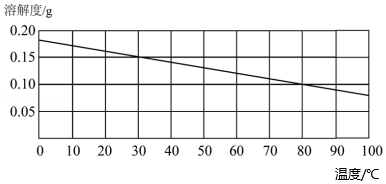
溶解度/g
一般称为
<0.01
难溶
0.01~1
微溶
1~10
可溶
>10
易溶
下列说法正确的是( )
A、Ca(OH)2属于易溶物质 B、Ca(OH)2的溶解度随温度的升高而增大 C、30℃时,Ca(OH)2的饱和溶液中溶质与溶剂的质量比为3:20 D、70℃时Ca(OH)2的饱和溶液,降温到50℃时没有析出固体二、填空题
-
16. a、b是常见的两种固体物质,根据图表的信息回答下列问题:
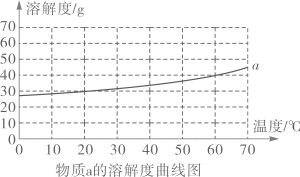
物质b的溶解度表
温度/℃
0
10
20
30
40
50
60
b的溶解度/g
14
20
30
45
65
85
110
(1)、60℃时,物质a的溶解度是g。(2)、20℃时,将20g物质b加入到50g水中,充分溶解后得到溶液的质量为g。(3)、将50℃时a、b两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为ab(填“>”、“=”或者“<”)。(4)、下列说法正确的组合是_______(填字母序号)。①所有物质的溶解度都随温度的升高面增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a
A、①④ B、①③ C、②③ D、②④17. 图中是a、b、c三种物质的溶解度曲线,回答下列问题。 (1)、P点的含义:。(2)、在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为g。(3)、b中混有少量a,提纯b的方法是(选填“蒸发结晶"或“降温结晶”)。(4)、分别将t3℃时a、b的饱和溶液降温到t2℃析出晶体的质量大小关系为(选填一个序号)。
(1)、P点的含义:。(2)、在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为g。(3)、b中混有少量a,提纯b的方法是(选填“蒸发结晶"或“降温结晶”)。(4)、分别将t3℃时a、b的饱和溶液降温到t2℃析出晶体的质量大小关系为(选填一个序号)。①a>b ②a<b ③a=b ④均有可能
三、综合题
-
18. 下图一为四种物质的溶解度曲线。如图二所示, X的饱和溶液加热时变浑浊。
 (1)、根据图一,10℃时,四种物质溶解度从大到小的顺序为(填序号),NH4H2PO4与NaCl大约在℃时,溶解度相等。(2)、根据图二信息,X对应的图一中的物质是(填序号)。(3)、当NH4H2PO4中混有少量NaCl杂质时,可采用方法提纯。
(1)、根据图一,10℃时,四种物质溶解度从大到小的顺序为(填序号),NH4H2PO4与NaCl大约在℃时,溶解度相等。(2)、根据图二信息,X对应的图一中的物质是(填序号)。(3)、当NH4H2PO4中混有少量NaCl杂质时,可采用方法提纯。若70gNH4H2PO4中混有5 g NaCl杂质,可按照以下步骤进行除杂。
①在℃下,用100g水溶解,确保固体刚好完全溶解。
②将①的饱和溶液降温到10℃时,溶液中析出 NH4H2PO4的质量应为g。
③再进行过滤、(填操作名称)、干燥,即可得到较纯净的NH4H2PO4。
(4)、10℃时,将20gCe2(SO4)3加入到100g水中,所得溶液的溶质质量分数为(结果精确到0.1%)。19. 如图1是甲、乙、丙三种固体的溶解度曲线,试回答: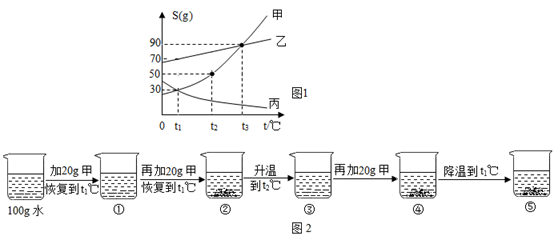 (1)、t2℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是。(2)、乙溶液中含有少量甲的杂质,提纯乙晶体的方法是。(3)、某同学在t1℃时开始如图2所示实验,得到相应的溶液,下列说法错误的是。
(1)、t2℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是。(2)、乙溶液中含有少量甲的杂质,提纯乙晶体的方法是。(3)、某同学在t1℃时开始如图2所示实验,得到相应的溶液,下列说法错误的是。A 在溶液①~⑤中,属于饱和溶液的是②④⑤
B 与溶液②溶质质量分数相等的是⑤
C 杯④中所得溶液的质量为160g
D 烧杯⑤中固体的质量为30g
(4)、t2℃时,要配制一瓶300g甲的饱和溶液,需要溶质甲的质量为 , 需要水的体积为。四、实验探究题
-
20. 我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物。
(资料)①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
温度/℃
0
10
20
30
50
溶解度/g
Ca(OH)2
0.18
0.17
0.16
0.15
0.14
K2CO3
107
109
110
114
121
KOH
97
103
112
126
140
(1)、20℃时,100 g 水中最多可溶解 K2CO3 的质量是g,溶质的质量分数为 50% 的 KOH 溶液属于 溶液(填“饱和”或“不饱和”)。(2)、某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示。则纵坐标可能表示的是(填序号)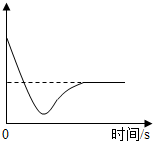
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
(3)、20℃时,将 1.38 g K2CO3 固体放入 100 g 水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为 1.5 g 的固体。所得滤液中的溶质是 , 加入氢氧化钙的质量是g。(4)、将纯净的氯化钠配制成溶液。20℃时,向 4 个盛有 200 g 水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4 组实验数据如下:实验序号
①
②
③
④
加入氯化钠的质量/g
9
36
81
90
溶液质量/g
209
236
272
272
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是g。关于上述实验的叙述正确的是(填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体
五、计算题
-
21.
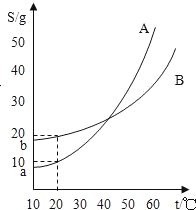
A和B两种化合物的溶解度曲线如右图,现要用结晶法从A、B的混合物中提取A(不考虑A、B共存于溶液中时对各自溶解度的影响).取得60克混合物,将它溶于100克热水,然后冷却至20℃,若使A析出而B不析出,则混合物中A的质量分数应在什么范围?
-