初中化学沪教版(上海)九年级下学期 第5单元 5.1生活中的酸和碱
试卷更新日期:2021-02-26 类型:同步测试
一、单选题
-
1. 酸的组成中一定含有( )A、金属元素 B、酸根 C、原子团 D、氧元素2. 分类是化学学习中常用的思维方法,下列有关物质分类正确的是( )A、酸:盐酸 硫酸 硝酸 B、碱:烧碱 纯碱 氨水 C、有机物:甲烷 乙醇 一氧化碳 D、混合物:高锰酸钾 海水 合金3. 下列既是二元酸又是含氧酸的是( )A、H2O B、H2SO4 C、H2S D、HNO34. 属于一元含氧酸是( )A、盐酸(HCl) B、碳酸(H2CO3) C、硫酸(H2SO4) D、硝酸(HNO3)5. 中和反应在生活中有广泛应用,下列应用不是利用中和反应原理的是( )A、用盐酸除铁锈 B、服用含有氢氧化镁的药物治疗胃酸过多 C、用熟石灰改良酸性土壤 D、用氢氧化钠溶液洗涤石油产品中的残留硫酸6. 往稀盐酸里面滴加氢氧化钠溶液,如图表示该反应前后溶液中存在的主要离子,下列说法不正确的是( )
 A、
A、 表示Na+
B、
表示Na+
B、 表示Cl-
C、向反应后的溶液中加入硝酸银溶液产生白色沉淀
D、向反应后的溶液中加入紫色石蕊试剂后溶液呈红色
7. 推理是一种重要的化学思维方法,以下推理合理的是( )A、元素的种类是由质子数决定的,则质子数相同的原子属于同种元素 B、溶液是均一、稳定的,所以均一、稳定的物质一定是溶液 C、洗涤剂去油污是利用了乳化作用,则汽油去油污也是利用了乳化作用 D、中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应8. 通过学习化学,我们总结或发现了许多知识具有规律性。下列说法正确的是()A、所有酸中一定都有氢元素 B、能够与酸反应生成气体的物质一定是碳酸盐 C、生成盐和水的反应一定是中和反应 D、显碱性的溶液一定是碱的溶液9. 下列反应属于中和反应的是( )A、2HCl+CuO═CuCl2+H2O B、2NaOH+CO2═Na2CO3+H2O C、2HCl+Cu(OH)2═CuCl2+2H2O D、CO2+H2O═H2CO310. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应 时,利用数字化传感器测得烧杯中溶液 pH 的变化,其图象如图所示,下列说法正确的是( )
表示Cl-
C、向反应后的溶液中加入硝酸银溶液产生白色沉淀
D、向反应后的溶液中加入紫色石蕊试剂后溶液呈红色
7. 推理是一种重要的化学思维方法,以下推理合理的是( )A、元素的种类是由质子数决定的,则质子数相同的原子属于同种元素 B、溶液是均一、稳定的,所以均一、稳定的物质一定是溶液 C、洗涤剂去油污是利用了乳化作用,则汽油去油污也是利用了乳化作用 D、中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应8. 通过学习化学,我们总结或发现了许多知识具有规律性。下列说法正确的是()A、所有酸中一定都有氢元素 B、能够与酸反应生成气体的物质一定是碳酸盐 C、生成盐和水的反应一定是中和反应 D、显碱性的溶液一定是碱的溶液9. 下列反应属于中和反应的是( )A、2HCl+CuO═CuCl2+H2O B、2NaOH+CO2═Na2CO3+H2O C、2HCl+Cu(OH)2═CuCl2+2H2O D、CO2+H2O═H2CO310. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应 时,利用数字化传感器测得烧杯中溶液 pH 的变化,其图象如图所示,下列说法正确的是( ) A、图中 c点所示溶液呈碱性 B、图中 a点所示溶液中,含有的溶质是 Na2SO4 和 H2SO4 C、该实验是将氢氧化钠溶液逐滴滴加到盛有硫酸的烧杯中 D、由 a 点到 b点的 pH 变化过程证明酸和碱发生了中和反应
A、图中 c点所示溶液呈碱性 B、图中 a点所示溶液中,含有的溶质是 Na2SO4 和 H2SO4 C、该实验是将氢氧化钠溶液逐滴滴加到盛有硫酸的烧杯中 D、由 a 点到 b点的 pH 变化过程证明酸和碱发生了中和反应二、综合题
-
11. 如图实验中,氢氧化钠溶液中加入无色酚酞溶液的作用是。实验观察到溶液由红色变成无色,此时烧杯中溶液的溶质成分(不考虑酚酞)有(写出所有的可能情况)。
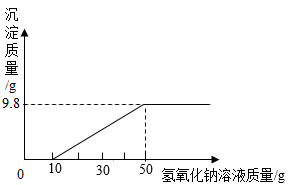
 12. 某化学兴趣小组的同学在进行微专题复习时,围绕酸、碱中和反应这一主题展开了深度学习。请你参与其中,按要求回答问题和开展探究。(1)、下列选项的应用与中和反应的原理无关的是____。A、使用浓硫酸干燥CO2气体 B、使用熟石灰改良酸性土壤 C、服用含有Al(OH)3的药物治疗胃酸过多症 D、利用氢氧化钠溶液洗涤石油产品中的残余硫酸(2)、某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液80g,洗涤后的溶液呈中性。这一定量石油产品中含硫酸的质量是g。(3)、做酸碱中和反应实验时,向烧杯内的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂。因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究。
12. 某化学兴趣小组的同学在进行微专题复习时,围绕酸、碱中和反应这一主题展开了深度学习。请你参与其中,按要求回答问题和开展探究。(1)、下列选项的应用与中和反应的原理无关的是____。A、使用浓硫酸干燥CO2气体 B、使用熟石灰改良酸性土壤 C、服用含有Al(OH)3的药物治疗胃酸过多症 D、利用氢氧化钠溶液洗涤石油产品中的残余硫酸(2)、某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液80g,洗涤后的溶液呈中性。这一定量石油产品中含硫酸的质量是g。(3)、做酸碱中和反应实验时,向烧杯内的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂。因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究。(提出问题)该烧杯中溶液的溶质是什么?
(猜想)猜想一:只含有CaCl2
猜想二:含有CaCl2、HCl和Ca(OH)2
猜想三:含有CaCl2和Ca(OH)2
猜想四:含有。
同学们讨论后一致认为猜想二不合理,理由是。
(查阅资料)氯化钙溶液呈中性。
(进行实验)同学们设计了如下不同的实验方案,证明猜想四是成立的。
请帮他们填写有关实验步骤和实验现象。
方案
实验步骤
实验现象
一
取少量烧杯中的溶液于试管中,滴加几滴紫色石蕊溶液。
二
将一颗生锈铁钉放入另一支试管中,取一定量烧杯中的溶液加入其中。
三
另取少量烧杯中的溶液于第三支试管中,加入
产生气泡
(反思与拓展)①要使烧杯内溶液的溶质只含有CaCl2 , 需要除去杂质,其中的一种方法是向烧杯中加入过量的某种物质,然后过滤,该除杂原理用化学方程式表示为。
②为了验证猜想三中不含有Ca(OH)2 , 小智的方案是:取少量烧杯中溶液于试管中,滴入几滴酚酞溶液,振荡,观察到酚酞溶液不变色,即说明猜想三不正确。你还有什么方案,请说出一种:。
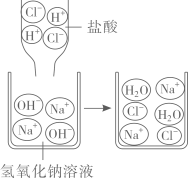
③结合下图,分析HCl和NaOH反应的实质:。
三、计算题