初中化学鲁教版九年级下学期 第七单元第二节 碱及其性质
试卷更新日期:2021-02-26 类型:同步测试
一、单选题
-
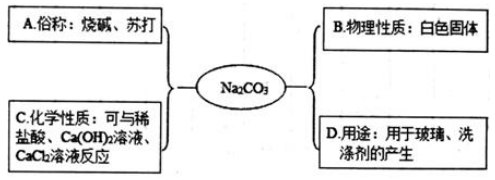
1. 下列关于酸、碱的说法错误的是( )A、苛性钠、烧碱、火碱都是氢氧化钠 B、氢氧化钙可以用来改良酸性土壤 C、稀盐酸能够使酚酞溶液变红 D、生活中许多常见的物质(如柠檬、柑橘)中含有酸2. 小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
 A、俗称:烧碱、苏打 B、物理性质:白色固体 C、化学性质:可与稀盐酸、Ca(OH)2溶液、CaCl2溶液反应 D、用途:用于玻璃、洗涤剂的产生3. A~F为初中化学常见物质,固体A在空气中易潮解,B和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所示(“→”表示反应能一步实现,“一”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是( )
A、俗称:烧碱、苏打 B、物理性质:白色固体 C、化学性质:可与稀盐酸、Ca(OH)2溶液、CaCl2溶液反应 D、用途:用于玻璃、洗涤剂的产生3. A~F为初中化学常见物质,固体A在空气中易潮解,B和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所示(“→”表示反应能一步实现,“一”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是( )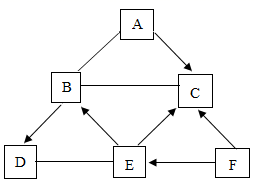 A、C和F组成元素可能相同 B、固体B可用于人工降雨 C、D和E在一定条件下反应生成B D、A~F属于酸、碱、盐、氧化物、单质中的四类物质4. 下列物质露置在空气中,质量会减少的是( )A、生石灰 B、苛性钠 C、浓硫酸 D、浓盐酸5. 下列关于Ca(OH)2的说法错误的是( )A、微溶于水,水溶液呈碱性 B、能与酸反应,可用于治疗胃酸过多 C、与CuSO4溶液按一定比例混合,可配制波尔多液 D、澄清溶液可用来检验CO26. 在100mL5%的硫酸中依次加入一定量的氧化铁和氢氧化钠溶液,有关说法一定正确的是( )A、有沉淀生成 B、溶液最终呈黄色 C、只发生两个反应 D、溶液中硫酸根的物质的量保持不变7. 一定温度下,向a g FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是( )
A、C和F组成元素可能相同 B、固体B可用于人工降雨 C、D和E在一定条件下反应生成B D、A~F属于酸、碱、盐、氧化物、单质中的四类物质4. 下列物质露置在空气中,质量会减少的是( )A、生石灰 B、苛性钠 C、浓硫酸 D、浓盐酸5. 下列关于Ca(OH)2的说法错误的是( )A、微溶于水,水溶液呈碱性 B、能与酸反应,可用于治疗胃酸过多 C、与CuSO4溶液按一定比例混合,可配制波尔多液 D、澄清溶液可用来检验CO26. 在100mL5%的硫酸中依次加入一定量的氧化铁和氢氧化钠溶液,有关说法一定正确的是( )A、有沉淀生成 B、溶液最终呈黄色 C、只发生两个反应 D、溶液中硫酸根的物质的量保持不变7. 一定温度下,向a g FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是( ) A、Fe(OH)3沉淀完全时消耗NaOH的质量为ng B、P点对应的溶液中 NaOH达到饱和状态 C、m=c-a D、生成Fe(OH)3的质量为(n-b+a)g8. 下列实验现象描述正确的是( )A、无色溶液中产生蓝色沉淀
A、Fe(OH)3沉淀完全时消耗NaOH的质量为ng B、P点对应的溶液中 NaOH达到饱和状态 C、m=c-a D、生成Fe(OH)3的质量为(n-b+a)g8. 下列实验现象描述正确的是( )A、无色溶液中产生蓝色沉淀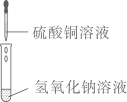 B、发出微弱的淡蓝色火焰,生成有刺激性气味的二氧化硫
B、发出微弱的淡蓝色火焰,生成有刺激性气味的二氧化硫 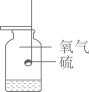 C、白色固体变成白色浆液,吸收大量的热
C、白色固体变成白色浆液,吸收大量的热 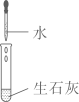 D、黑色固体表面有气泡冒出溶液由浅绿色变为无色
D、黑色固体表面有气泡冒出溶液由浅绿色变为无色 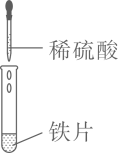
二、填空题
-
9. 检验溶液的酸碱性可以用和两种常用的酸碱指示剂;还可以用蓝色石蕊试纸或红色石蕊试纸来检验.蓝色石蕊试纸遇到性溶液能变红,红色石蕊试纸遇到性溶液变蓝色.10. 海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中或长途运输活鱼常常由于鱼多而缺氧,因此要设法增加水中的氧气含量。
材料一:已知过氧化钠(Na2O2)与水较快反应,反应方程式是 ,过氧化钙(CaO2)与Na2O2性质相似,与水缓慢反应放出氧气。
材料二:20℃时,NaOH的溶解度为109g,Ca(OH)2的溶解度为0.165g。
(1)、试写出CaO2与H2O反应的化学方程式;(2)、长途运输活鱼,人们选择CaO2而不选择Na2O2作增氧剂的理由可能是(写出一条即可)三、推断题
-
11. 图中A、B、C、D、E、F为初中化学常见的六种物质。D是胃液的主要成分,E是红棕色固体,F与D反应后所得溶液为浅绿色,C在工业上常用来生产肥皂。(图中用“一”表示两种物质能发生反应,用“→”或“
 ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:  (1)、请写出下列物质(或溶质)的化学式:
(1)、请写出下列物质(或溶质)的化学式:B;D;E;F。
(2)、E与足量的D反应的现象为;(3)、C转化为B的化学方程式为。12. 如图所示,A~F是初中化学常见的物质,它们分别是Fe、CuSO4、NaOH、H2SO4、Ca(OH)2、Na2CO3中的一种,A是黑色粉末,B和E可以用来配制波尔多液。方框内之间的连线表示二者可以发生反应,箭头表示一种物质可以转化为另一种物质。请回答下列问题:(以上反应或转化均在溶液中进行,且在初中范围内)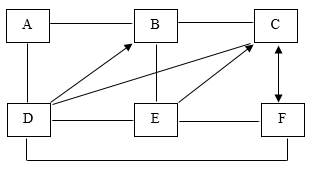 (1)、请写出A和F两种物质的化学式为:A , F。(2)、写出D与E反应的化学方程式;(3)、写出足量的C溶液加入到B溶液反应的实验现象为。
(1)、请写出A和F两种物质的化学式为:A , F。(2)、写出D与E反应的化学方程式;(3)、写出足量的C溶液加入到B溶液反应的实验现象为。四、实验探究题
-
13. 某化学兴趣小组的同学对酸、碱和盐的性质进行探究,请你参与。
[查阅资料]
20℃时,部分物质的溶解度。
物质
Ca(OH)2
NaOH
Na2CO3
NaHCO3
溶解度/g
0.16
109
21.8
9.6
(1)、探究一:探究氢氧化钙的性质20℃时,在盛有5g Ca(OH)2固体的A烧杯中加入40mL水,用玻璃棒搅拌,静置,取上层部分清液于B烧杯中。
①向A烧杯中滴加几滴酚酞溶液,观察到的现象是 , 再加入过量稀盐酸,反应的化学方程式为
②向B烧杯中通入CO2 , 观察到澄清石灰水变浑浊。
③由上述实验可知氢氧化钙的性质。
(2)、[实验拓展]向上述(1)反应后的A烧杯中滴加碳酸钠溶液,测得其pH随反应时间的变化如图。AB段的实验现象是 , BC段发生反应的化学方程式为
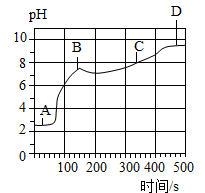 (3)、探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。
(3)、探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。[设计和实验] 20℃时,甲、乙两组同学设计如图装置分别进行实验。
甲组:从a端缓慢通入CO2 , 一段时间后II中变浑浊,停止通CO2 , I中溶质为X。打开活塞,滴加足量稀盐酸。
[解释与结论]
经分析X是NaHCO3。实验过程中,Ⅰ中产生的现象是
(4)、乙组:从a端缓慢通入CO2 , 一段时间后II中无明显现象,停止通CO2 , Ⅰ中溶质为Y。打开活塞,滴加足量稀盐酸,II 中变浑浊。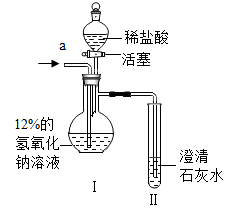
[解释与结论]
乙组同学认为Y只有Na2CO3。你认为该结论是否合理,结合分析Y的成分说明理由。I 中一定发生反应的化学方程式为。
五、综合题
-
14. 某实验小组开展了如图有关碱的化学性质探究活动:
 (1)、实验1的目的是;(2)、实验2中发生反应的化学方程式是;(3)、实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是。15. “探险队员”--盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过。(提示:铜和银不与稀盐酸反应)
(1)、实验1的目的是;(2)、实验2中发生反应的化学方程式是;(3)、实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是。15. “探险队员”--盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过。(提示:铜和银不与稀盐酸反应)
 (1)、请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)
(1)、请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)入口→→出口。
(2)、在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有个;其中能“吃掉”盐酸的盐是(填物质的名称)。(3)、在不能与盐酸反应的物质中,写出一个能与硝酸银溶液反应的化学方程式。(4)、如果将盐酸换成氢氧化钾溶液,它能沿着盐酸走出的路线“走出”这个迷宫吗,为什么?。16. 孔雀石的主要成分是CuCO3·Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。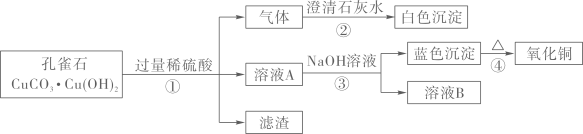 (1)、白色沉淀的化学式为。(2)、写出步骤③中发生反应的化学方程式。(3)、蓝色沉淀受热分解生成另一种氧化物的化学式是。(4)、若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达种。
(1)、白色沉淀的化学式为。(2)、写出步骤③中发生反应的化学方程式。(3)、蓝色沉淀受热分解生成另一种氧化物的化学式是。(4)、若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达种。
-