浙教版科学2020-2021学年九年级中考模拟冲刺专练:金属(2)
试卷更新日期:2021-02-02 类型:一轮复习
一、单选题
-
1. 下列四个实验中。“操作--图象--结论”对应关系正确的是( )
A
B
C
D
操作
分别向等质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸
一定温度下,向氢氧化钙溶液中加入氧化钙固体
向变质的氢氧化钠溶液中滴加稀盐酸
向H2SO4、MgSO4混合溶液中滴加NaOH溶液
图象




结论
三种金属与硫酸反应的剧烈程度: Mg>Fe>Zn
该氢氧化钙溶液已经饱和
氢氧化钠溶液已经全部变质
pH为7时水平线段表示硫酸镁和氢氧化钠反应
A、A B、B C、C D、D2. 将一定质量的铁粉加入含AgNO3和Zn(NO3)2两种溶质的溶液中,反应结束后过滤,分别向滤液和滤渣中加入稀盐酸,均无明显现象,下列对滤渣和滤液的说明中,不正确的是( )A、滤渣的成分只有银 B、滤液中的溶质是Zn(NO3)2、Fe (NO3)2 C、滤渣的成分可能是银、锌的混合物 D、所得滤液的质量小于反应前原溶液的质量3. 向硝酸银溶液中加入质量为m1的镁粉和锌粉的混合物,充分反应后经多次过滤洗涤,得到滤渣和无色滤液。将滤渣烘干,称得质量为m2。向滤液中滴入氯化钠溶液,发现有沉淀产生。则下列说法不正确的是( )A、滤液中只有硝酸银和硝酸镁 B、滤渣中只有银,没有镁和锌 C、m1<m2 D、滤渣中加入稀盐酸,没有气体放出4. 向一定质量的AgNO3和Cu(NO)2的混合溶液中不断加入铁粉,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程,下列说法错误的是( ) A、向a点溶液中滴加稀盐酸,有白色沉淀 B、bd段是铁粉与Cu(NO)2溶液反应 C、d点溶液中的溶质是Fe(NO)3 D、在e点时,能得到3种固体5. 有等质量的镁和铁,镁放入质量分数为10%的稀盐酸中,铁放入质量分数为10%的稀硫酸中,产生氢气的质量随反应时间变化曲线如图所示。下列结果可能的是( )
A、向a点溶液中滴加稀盐酸,有白色沉淀 B、bd段是铁粉与Cu(NO)2溶液反应 C、d点溶液中的溶质是Fe(NO)3 D、在e点时,能得到3种固体5. 有等质量的镁和铁,镁放入质量分数为10%的稀盐酸中,铁放入质量分数为10%的稀硫酸中,产生氢气的质量随反应时间变化曲线如图所示。下列结果可能的是( )
①反应后镁有剩余 ②反应后铁有剩余
③反应后稀硫酸有剩余 ④反应后稀盐酸有剩余
⑤消耗的铁和镁的质量相等 ⑥消耗的稀硫酸和稀盐酸质量相等
A、①③⑤ B、①②③ C、①②④ D、②③⑥6. 现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时 间的关系如图所示。则下列说法正确的是( ) A、金属X、Y的活动性关系为:X<Y B、金属完全反应时消耗稀盐酸的质量:X=Y C、X、Y的相对原子质量大小关系为:X<Y D、t3时烧杯中溶液的质量:X<Y7. 已知钠、钾都是活泼金属,都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说法错误的是( )
A、金属X、Y的活动性关系为:X<Y B、金属完全反应时消耗稀盐酸的质量:X=Y C、X、Y的相对原子质量大小关系为:X<Y D、t3时烧杯中溶液的质量:X<Y7. 已知钠、钾都是活泼金属,都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说法错误的是( ) A、曲线a表示钾与水反应的图象,曲线b表示钠与水反应的图象 B、参加反应的钠的质量小于钾的质量 C、参加反应的水的质量相等 D、反应后NaOH溶液的溶质质量分数大于KOH溶液的溶质质量分数8. 将一定量的锌粒投入到含溶质为Al(NO3)3、Cu(NO3)2、AgNO3的溶液中,充分反应后过滤,往滤液中滴加稀盐酸,无明显现象,则下列说法正确的是( )A、滤液中溶质为Al(NO3)3、Zn(NO3)3时,滤渣一定为Cu、Ag B、锌粒先跟Al(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象 C、锌粒先跟Cu(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象 D、锌粒先跟AgNO3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象9. 某溶液含有Cu(NO3)2和AgNO3 , 现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示)下列说法中不正确的是( )
A、曲线a表示钾与水反应的图象,曲线b表示钠与水反应的图象 B、参加反应的钠的质量小于钾的质量 C、参加反应的水的质量相等 D、反应后NaOH溶液的溶质质量分数大于KOH溶液的溶质质量分数8. 将一定量的锌粒投入到含溶质为Al(NO3)3、Cu(NO3)2、AgNO3的溶液中,充分反应后过滤,往滤液中滴加稀盐酸,无明显现象,则下列说法正确的是( )A、滤液中溶质为Al(NO3)3、Zn(NO3)3时,滤渣一定为Cu、Ag B、锌粒先跟Al(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象 C、锌粒先跟Cu(NO3)3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象 D、锌粒先跟AgNO3反应无剩余,因此往滤液中滴加稀盐酸,无明显现象9. 某溶液含有Cu(NO3)2和AgNO3 , 现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示)下列说法中不正确的是( ) A、Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱 B、当溶质种类为1种时,金属单质种类可能为1种 C、c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+ D、从m1变化到m2时,溶液中硝酸铜的质量分数变大10. 下列图像不能正确反映对应变化关系的是( )A、在一定量AgNO3和Zn(NO)2的混合溶液中加入铁粉
A、Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱 B、当溶质种类为1种时,金属单质种类可能为1种 C、c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+ D、从m1变化到m2时,溶液中硝酸铜的质量分数变大10. 下列图像不能正确反映对应变化关系的是( )A、在一定量AgNO3和Zn(NO)2的混合溶液中加入铁粉 B、向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
B、向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸  C、常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
C、常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体  D、向一定量的稀盐酸中加入过量的NaOH溶液
D、向一定量的稀盐酸中加入过量的NaOH溶液  11. 继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起。为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得钯金和铁的氯化物。经分析所得钯金的质量为10.6g,未反应的铁粉质量为4.4g,下列说法正确的是( )A、生成铁的氯化物质量为12.7g B、生成铁的氯化物质量为16.25g C、该反应说明钯金比铁活泼 D、生成铁的氯化物为FeCl312. 向一定质量AgNO3和Cu(NO3)2的混台溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )
11. 继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起。为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得钯金和铁的氯化物。经分析所得钯金的质量为10.6g,未反应的铁粉质量为4.4g,下列说法正确的是( )A、生成铁的氯化物质量为12.7g B、生成铁的氯化物质量为16.25g C、该反应说明钯金比铁活泼 D、生成铁的氯化物为FeCl312. 向一定质量AgNO3和Cu(NO3)2的混台溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( ) A、取a点溶液,滴加稀盐酸,无白色沉淀 B、图标上b~c段质量增加的原因是Zn与Cu(NO3)3溶液反应 C、c点和d点溶质种类不同,金属单质种类也不同 D、b点时溶液中金属离子有Zn2+、Cu2+ , 金属单质有Zn、Cu、Ag13. 小黄同学曾用如图所示装置进行实验(图中铁架台等仪器均已略去)。在I中加入试剂
A、取a点溶液,滴加稀盐酸,无白色沉淀 B、图标上b~c段质量增加的原因是Zn与Cu(NO3)3溶液反应 C、c点和d点溶质种类不同,金属单质种类也不同 D、b点时溶液中金属离子有Zn2+、Cu2+ , 金属单质有Zn、Cu、Ag13. 小黄同学曾用如图所示装置进行实验(图中铁架台等仪器均已略去)。在I中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊。符合以上实验现象的I和Ⅱ中( )

A
B
C
D
I
CaCO3
稀HCl
Na2CO3
稀H2SO4
Zn
稀H2SO4
Cu
稀H2SO4
Ⅱ
KNO3
NaCl
BaCl2
Ba(OH)2
A、A B、B C、C D、D14. 向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,一定有气泡产生②向滤液中加入稀盐酸,一定有沉淀产生 ③滤渣中一定含有Ag ④滤液中一定含有
Fe(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3。以上说法正确的个数为( )
A、3个 B、2个 C、1个 D、0个15. 将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量反应时间的关系如图所示,下列说法错误的是( ) A、反应结束后镁一定有剩余 B、反应消耗盐酸的总质量一定相等 C、0-t1时段,产生氢气的质量镁比铁大 D、0-t2时段,参加反应的镁的质量与铁相等16. 某化学小组在一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉充分反应后过滤,得到溶液甲和固体乙,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2
A、反应结束后镁一定有剩余 B、反应消耗盐酸的总质量一定相等 C、0-t1时段,产生氢气的质量镁比铁大 D、0-t2时段,参加反应的镁的质量与铁相等16. 某化学小组在一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉充分反应后过滤,得到溶液甲和固体乙,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2②固体乙中一定含有Ag,可能含有Cu和Zn ③若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2 ④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2。上述四种说法正确的个数为( )
 A、1个 B、2个 C、3个 D、4个17. 将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中充分反应后过滤,将滤渣放入稀盐酸溶液里,有气泡产生。则下列说法正确的是( )A、滤渣中有Ag、Cu;滤液中有Mg(NO3)2和Zn(NO3)2 B、滤渣中有Ag、Cu、Zn;滤液中有Mg(NO3)2和Zn(NO3)2 C、滤渣中有Ag、Cu、Zn、Mg;滤液中有Mg(NO3)2和Zn(NO3)2 D、滤渣中有Ag、Cu、Zn;滤液中有Mg(NO3)2、Cu(NO3)2、AgNO3和Zn(NO3)218. Mg和Al分别与过量的稀H2SO4反应,产生氢气的质量(m)与反应时间(t)关系如图,下列说法中正确的是( )
A、1个 B、2个 C、3个 D、4个17. 将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中充分反应后过滤,将滤渣放入稀盐酸溶液里,有气泡产生。则下列说法正确的是( )A、滤渣中有Ag、Cu;滤液中有Mg(NO3)2和Zn(NO3)2 B、滤渣中有Ag、Cu、Zn;滤液中有Mg(NO3)2和Zn(NO3)2 C、滤渣中有Ag、Cu、Zn、Mg;滤液中有Mg(NO3)2和Zn(NO3)2 D、滤渣中有Ag、Cu、Zn;滤液中有Mg(NO3)2、Cu(NO3)2、AgNO3和Zn(NO3)218. Mg和Al分别与过量的稀H2SO4反应,产生氢气的质量(m)与反应时间(t)关系如图,下列说法中正确的是( ) A、I线表示Al与稀H2SO4反应 B、Mg和Al参与反应的质量之比为3:4 C、Mg和Al与过量稀H2SO4完全反应所需时间不相等 D、Mg和Al与过量稀H2SO4完全反应产生H2的质量之比为4:319. 某黑色固体粉末可能是Fe、FeO、CuO、C中的一种或几种。为了探究其成分,小明同学按照下图所示流程进行了实验。
A、I线表示Al与稀H2SO4反应 B、Mg和Al参与反应的质量之比为3:4 C、Mg和Al与过量稀H2SO4完全反应所需时间不相等 D、Mg和Al与过量稀H2SO4完全反应产生H2的质量之比为4:319. 某黑色固体粉末可能是Fe、FeO、CuO、C中的一种或几种。为了探究其成分,小明同学按照下图所示流程进行了实验。
关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中一定有Fe;
②若步骤Ⅱ中无明显现象,则固体乙中最多只能有四种物质;
③若步骤Ⅱ中有气泡产生,则固体乙一定是C;
④若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO;
⑤若固体乙呈红色,则原固体中一定含有Fe和CuO。
以上说法中正确的个数是( )
A、1个 B、2个 C、3个 D、4个20. 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( ) A、取a点溶液,滴加稀盐酸,无白色沉淀 B、图标上b﹣c段质量增加的原因是Zn与Cu(NO3)2溶液反应 C、c点和d点溶质种类不同,金属单质种类也不同 D、b点时溶液中金属离子有Zn2+、Cu2+ , 金属单质有Zn、Cu、Ag21. 等质量的 X、Y 两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示。下列说法中不正确的是( )
A、取a点溶液,滴加稀盐酸,无白色沉淀 B、图标上b﹣c段质量增加的原因是Zn与Cu(NO3)2溶液反应 C、c点和d点溶质种类不同,金属单质种类也不同 D、b点时溶液中金属离子有Zn2+、Cu2+ , 金属单质有Zn、Cu、Ag21. 等质量的 X、Y 两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示。下列说法中不正确的是( ) A、t1 时,产生气体的质量:X>Y B、t2 时,消耗金属的质量:X>Y C、t3 时,消耗金属的质量:X=Y D、t3 时,消耗盐酸的质量:X=Y22. 小柯为比较Mg,Fe,Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )
A、t1 时,产生气体的质量:X>Y B、t2 时,消耗金属的质量:X>Y C、t3 时,消耗金属的质量:X=Y D、t3 时,消耗盐酸的质量:X=Y22. 小柯为比较Mg,Fe,Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )
①Mg2+
②Mg2+和Fe2+
③Fe2+和Cu2+
④Mg2+、Fe2+和Cu2+
A、①② B、①③ C、②④ D、③④23. 甲、乙两烧杯内盛有等质量、等质量分数的盐酸。将镁逐渐加入甲烧杯,铁逐渐加入乙杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△M,画出△M-m曲线oac和obc的示意图,如图所示。根据图中信息,下列说法错误的是( )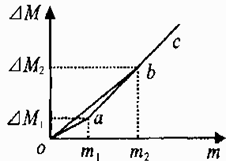 A、m1:m2=3:7 B、m1-△M1<m2-△M2 C、m曲线oac表示的是甲烧杯中△M与m的变化关系 D、当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种24. 往200g FeCl3和CuCl2的混合溶液中加入铁粉。已知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 、CuCl2+Fe=FeCl2+Cu。图为加入铁粉的质量与反应后剩余固体质量关系。则下列说法不正确的是( )
A、m1:m2=3:7 B、m1-△M1<m2-△M2 C、m曲线oac表示的是甲烧杯中△M与m的变化关系 D、当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种24. 往200g FeCl3和CuCl2的混合溶液中加入铁粉。已知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 、CuCl2+Fe=FeCl2+Cu。图为加入铁粉的质量与反应后剩余固体质量关系。则下列说法不正确的是( ) A、该200g溶液中的CuCl2 质量分数为6.75% B、B点后溶液的颜色为蓝色 C、取DE两点间的剩余固体加入盐酸,均有气泡产生 D、D点对应纵坐标为6.425. 向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,完全反应后过滤,下列情况不可能存在的是( )
A、该200g溶液中的CuCl2 质量分数为6.75% B、B点后溶液的颜色为蓝色 C、取DE两点间的剩余固体加入盐酸,均有气泡产生 D、D点对应纵坐标为6.425. 向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,完全反应后过滤,下列情况不可能存在的是( )
A、滤纸上有 Ag,滤液中有 Ag+、Cu2+、Zn2+ B、滤纸上有 Ag、Cu,滤液中有Ag+、Zn2+ C、滤纸上有 Ag、Cu、Zn,滤液中有 Zn2+ D、滤纸上有 Ag,滤液中有Cu2+、Zn2+