黑龙江省齐齐哈尔市龙沙区2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-02-02 类型:期末考试
一、单选题
-
1. 下列传统工艺品的制作过程中,一定发生了化学变化的是( )A、南阳玉雕 B、洛阳剪纸 C、开封汴绣 D、汝州瓷器2. 下列有关操作错误的是( )A、读
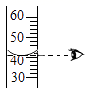 B、闻
B、闻  C、拿
C、拿 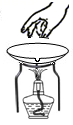 D、滴
D、滴 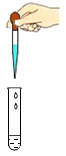 3. 下列有关实验现象的描述正确的是( )A、硫在空气中燃烧发出淡蓝色火焰,生成二氧化硫气体 B、铜和黄铜相互刻画,铜上留有痕迹 C、干燥的石蕊纸花放到二氧化碳气体中变为红色 D、把酒精滴入水(含少量红墨水)中,振荡、静置后,上下分层4. 在高压锅炉水处理时,肼(N2H4)用于脱除氧气以防锅炉腐蚀,其反应的化学方程式为: 。根据质量守恒定律,X的化学式为( )A、H2O B、NO C、H2 D、HNO35. 2020年6月23日,“北斗三号”收官之星发射成功,标志着我国“北斗”信号实现全球覆盖。发射用的火箭燃料之一为液氢,下列关于该燃料的说法不合理的是( )A、热值高,推力大 B、反应方程式是 C、绿色无污染 D、贮存、运输和加注都容易6. 下列物质的用途主要利用其物理性质的是( )A、焦炭用于冶炼金属 B、氧气用于医疗急救 C、钛镍用于形状记忆合金 D、氮气用于食品保护气7. 甲醇(CH3OH)制氢具有工艺简单、节能环保等优点,其中一种转化反应的微观示意图如下。下列有关该反应的说法正确的是( )
3. 下列有关实验现象的描述正确的是( )A、硫在空气中燃烧发出淡蓝色火焰,生成二氧化硫气体 B、铜和黄铜相互刻画,铜上留有痕迹 C、干燥的石蕊纸花放到二氧化碳气体中变为红色 D、把酒精滴入水(含少量红墨水)中,振荡、静置后,上下分层4. 在高压锅炉水处理时,肼(N2H4)用于脱除氧气以防锅炉腐蚀,其反应的化学方程式为: 。根据质量守恒定律,X的化学式为( )A、H2O B、NO C、H2 D、HNO35. 2020年6月23日,“北斗三号”收官之星发射成功,标志着我国“北斗”信号实现全球覆盖。发射用的火箭燃料之一为液氢,下列关于该燃料的说法不合理的是( )A、热值高,推力大 B、反应方程式是 C、绿色无污染 D、贮存、运输和加注都容易6. 下列物质的用途主要利用其物理性质的是( )A、焦炭用于冶炼金属 B、氧气用于医疗急救 C、钛镍用于形状记忆合金 D、氮气用于食品保护气7. 甲醇(CH3OH)制氢具有工艺简单、节能环保等优点,其中一种转化反应的微观示意图如下。下列有关该反应的说法正确的是( ) A、生成3种分子 B、属于化合反应 C、丙为CO D、催化剂不断减少8. 下列关于青蒿素(化学式为C15H22O6)的说法正确的是( )A、青蒿素中含有42个原子 B、青蒿素中碳元素、氢元素、氧元素的质量比为15:22:6 C、青蒿素是由三种元素组成 D、青蒿素中氢元素的质量分数最大9. 对比是学习化学的重要方法,下列关于二氧化碳和一氧化碳的比较,完全正确的是( )A、组成:CO2、CO均由碳元素和氧元素组成 B、性质:CO2、CO都有可燃性 C、用途:CO2可用于灭火;CO可用于人工降雨 D、危害:CO2会导致酸雨;CO会引起中毒10. 下列有关金属说法错误的是( )A、合金中只含有金属元素 B、钛合金可用来制造人造骨 C、钢铁表面生的铁锈要及时除去 D、不能用铁壶长期存放波尔多液11. 下列有关溶液说法正确的是( )A、凡是均一、稳定的液体一定是溶液 B、饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液 C、固体物质的溶解度都随温度的升高而增大 D、喝下汽水后,常会打嗝,说明气体的溶解度随温度的升高而增大12. 推理是学习化学常用的思维方法,下列推理正确的是( )A、在化学变化中原子不能再分,所以在化学变化中离子也不能再分 B、洗涤剂除油污的原理是乳化,所以汽油除油污的原理也是乳化 C、CO2使饱和石灰水变浑浊是化学变化,所以升温使饱和石灰水变浑浊也是化学变化 D、化合物是由不同种元素组成的物质,所以由同种元素组成的物质一定不是化合物13. 下列图像能正确表示对应关系的是( )A、分别向等质量的CaCO3和Na2CO3中加入足量的稀盐酸
A、生成3种分子 B、属于化合反应 C、丙为CO D、催化剂不断减少8. 下列关于青蒿素(化学式为C15H22O6)的说法正确的是( )A、青蒿素中含有42个原子 B、青蒿素中碳元素、氢元素、氧元素的质量比为15:22:6 C、青蒿素是由三种元素组成 D、青蒿素中氢元素的质量分数最大9. 对比是学习化学的重要方法,下列关于二氧化碳和一氧化碳的比较,完全正确的是( )A、组成:CO2、CO均由碳元素和氧元素组成 B、性质:CO2、CO都有可燃性 C、用途:CO2可用于灭火;CO可用于人工降雨 D、危害:CO2会导致酸雨;CO会引起中毒10. 下列有关金属说法错误的是( )A、合金中只含有金属元素 B、钛合金可用来制造人造骨 C、钢铁表面生的铁锈要及时除去 D、不能用铁壶长期存放波尔多液11. 下列有关溶液说法正确的是( )A、凡是均一、稳定的液体一定是溶液 B、饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液 C、固体物质的溶解度都随温度的升高而增大 D、喝下汽水后,常会打嗝,说明气体的溶解度随温度的升高而增大12. 推理是学习化学常用的思维方法,下列推理正确的是( )A、在化学变化中原子不能再分,所以在化学变化中离子也不能再分 B、洗涤剂除油污的原理是乳化,所以汽油除油污的原理也是乳化 C、CO2使饱和石灰水变浑浊是化学变化,所以升温使饱和石灰水变浑浊也是化学变化 D、化合物是由不同种元素组成的物质,所以由同种元素组成的物质一定不是化合物13. 下列图像能正确表示对应关系的是( )A、分别向等质量的CaCO3和Na2CO3中加入足量的稀盐酸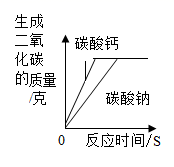 B、分别向等质量的镁和铝中加入足量的稀硫酸
B、分别向等质量的镁和铝中加入足量的稀硫酸 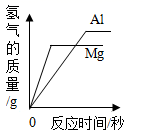 C、向一定量的过氧化氢溶液中加入少量的二氧化锰
C、向一定量的过氧化氢溶液中加入少量的二氧化锰 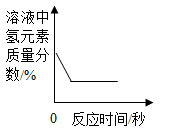 D、氢气和氧气在密闭容器中燃烧
D、氢气和氧气在密闭容器中燃烧 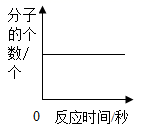
二、多选题
-
14. 除去下列物质中的杂质,所选试剂及操作方法均正确的是( )
选项
物质(括号内为杂质)
选用试剂及操作方法
A
二氧化碳(一氧化碳)
将气体点燃
B
氯化钙溶液(稀盐酸)
加入过量碳酸钙,过滤
C
硫酸亚铁溶液(硫酸铜溶液)
加入足量锌粉,过滤
D
氯化钾(二氧化锰)
加入足量的水,溶解、过滤、蒸发结晶
A、A B、B C、C D、D15. 将一定质量的Zn加入到Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,滤液仍为浅绿色,则下列判断正确的是( )A、滤渣一定为Ag、Fe B、滤液中一定含有Zn(NO3)2、Mg(NO3)2、Fe(NO3)2 C、滤液中最多含有三种溶质 D、反应前后金属固体的质量可能不变三、填空题
-
16. 用适当的元素符号与数字的组合填空:(1)、二个氧原子。(2)、亚铁离子。(3)、氦气。(4)、标出氨气中氮元素的化合价。17. 下图是A、B、C、D四种元素的原子结构示意图及氟元素在元素周期表中的信息。根据图示回答下列问题。
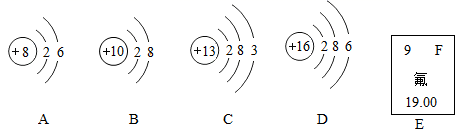 (1)、与A化学性质相似的原子是(填字母)(2)、具有相对稳定结构的原子是(填字母)(3)、C元素在元素周期表中位于第周期。(4)、根据E图示所给信息,推出氟元素原子的核外电子总数为。18. 水是一种重要的物质,与人类的生产和生活息息相关。(1)、用水可以获得氢气。请写出一个由水生成氢气的化学方程式。(2)、水还可以用于鉴別物质。水鉴別氯化钠和硝酸铵依据的是。(3)、水是最常见的溶剂。
(1)、与A化学性质相似的原子是(填字母)(2)、具有相对稳定结构的原子是(填字母)(3)、C元素在元素周期表中位于第周期。(4)、根据E图示所给信息,推出氟元素原子的核外电子总数为。18. 水是一种重要的物质,与人类的生产和生活息息相关。(1)、用水可以获得氢气。请写出一个由水生成氢气的化学方程式。(2)、水还可以用于鉴別物质。水鉴別氯化钠和硝酸铵依据的是。(3)、水是最常见的溶剂。①下列溶液用水作溶剂的是(填字母序号)。
a、生理盐水 b、碘酒 c、葡萄糖溶液
②将100g溶质质量分数为98%的浓硫酸稀释为溶质质量分数为10%的稀硫酸,需加水的质量为g。
19. 在高温条件下,碳单质不仅能与金属氧化物反应,还能与非金属氧化物反应,请写出碳与二氧化碳反应的化学方程式 , 其中发生还原反应的物质是 , 该反应是反应(填“放热”或“吸热”)。20. 甲、乙两种固体的溶解度曲线如图一所示: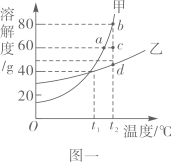
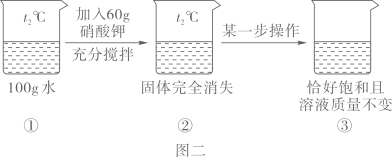 (1)、t1℃时,溶解度大小关系为:甲乙(填“>”、“<”或“=”);(2)、t2℃时,配制180g甲物质的饱和溶液,需称量甲的质量g;(3)、由图二推测硝酸钾是图一中的物质;(4)、图二“某一部操作”前后的溶液状态变化过程可以在图一中表示为(填序号)。
(1)、t1℃时,溶解度大小关系为:甲乙(填“>”、“<”或“=”);(2)、t2℃时,配制180g甲物质的饱和溶液,需称量甲的质量g;(3)、由图二推测硝酸钾是图一中的物质;(4)、图二“某一部操作”前后的溶液状态变化过程可以在图一中表示为(填序号)。A b点→a点 B c点→a点 C b点→c点 D c点→d点
21. 化学是研究物质性质、组成、结构与变化规律的科学。请回答下列问题:(1)、为什么灯泡里的灯丝用钨制而不用锡制?(2)、生铁和钢都是铁的合金,二者性能差异很大的原因是什么?(3)、金刚石和石墨都是由碳元素组成,为什么它们的物理性质存在着明显差异?22. 从下图选择仪器配置50g溶质质量分数为10%的NaCl溶液,回答有关问题: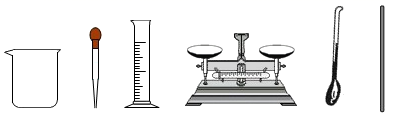 (1)、需要称量NaCl的质量为g。(2)、溶解时用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。
(1)、需要称量NaCl的质量为g。(2)、溶解时用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。四、流程题
-
23. 某废弃物中可能含有Cu、CuO、Mg、Zn中的一种或几种,为确定其成分井回收金属,取样品进行如图实验:
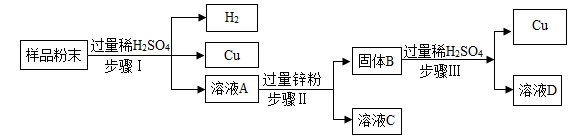 (1)、步骤Ⅱ的操作是。(2)、步骤Ⅱ中产生的现象是。(3)、若溶液C中只含一种溶质,则样品的成分是。
(1)、步骤Ⅱ的操作是。(2)、步骤Ⅱ中产生的现象是。(3)、若溶液C中只含一种溶质,则样品的成分是。五、简答题
-
24. 化学与生活息息相关,请用化学知识解释下列问题:(1)、在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?(2)、从灭火原理角度回答,为什么用扇子扇蜡烛火焰一扇就灭?(3)、天气闷热时,鱼塘里的鱼为什么总是接近水面游动?25. 目前环境问题日趋严重,保护环境势在必行。请回答下列问题:(1)、工业废水、生活污水的任意排放会导致水体污染。请写出水体污染的一点危害;(2)、写出一种汽车尾气的污染物和一条减少汽车尾气污染的措施。26. 下图是初中化学教科书中的一些实验示意图,回答下列问题:
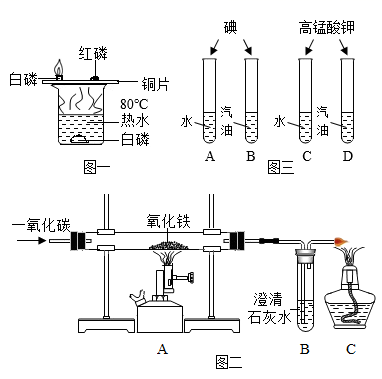 (1)、图一中验证可燃物燃烧需要温度达到着火点的现象是。(2)、图二中A处玻璃管内观察到的现象 , 实验结束时先熄灭酒精喷灯待装置冷却后再停止通CO,原因是。(3)、对比试管A和试管B,碘在水中几乎不溶解,在汽油中完全溶解,该实验说明了影响物质溶解性的因素是 , 对比试管A、C的目的是。
(1)、图一中验证可燃物燃烧需要温度达到着火点的现象是。(2)、图二中A处玻璃管内观察到的现象 , 实验结束时先熄灭酒精喷灯待装置冷却后再停止通CO,原因是。(3)、对比试管A和试管B,碘在水中几乎不溶解,在汽油中完全溶解,该实验说明了影响物质溶解性的因素是 , 对比试管A、C的目的是。六、实验题
-
27. 请结合下列实验装置,回答问题:
 (1)、写出标号①仪器的名称。(2)、写出实验室用高锰酸钾制取氧气的化学方程式。可选择装置(填序号)作为气体发生装置,但在该装置中还需要补充的是。(3)、实验室常用大理石和稀盐酸制取二氧化碳气体,写出反应的化学方程式 , 收集气体应选用装置(填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,通过观察到的现象说明二氧化碳具有物理性质是。
(1)、写出标号①仪器的名称。(2)、写出实验室用高锰酸钾制取氧气的化学方程式。可选择装置(填序号)作为气体发生装置,但在该装置中还需要补充的是。(3)、实验室常用大理石和稀盐酸制取二氧化碳气体,写出反应的化学方程式 , 收集气体应选用装置(填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,通过观察到的现象说明二氧化碳具有物理性质是。七、科学探究题
-
28. 金属防腐是科学研究中的重大课题。某校学习小组以铁的腐蚀为项目进行如下研究。(1)、(认识铁的腐蚀)
下列环境中的铁制品最容易生锈的是(填字母序号)。
A 未擦干的铁锅 B 除油漆的栏杆 C 盛水的不锈钢水杯
(2)、铁锈的主要成分是Fe2O3·xH2O,其中铁元素的化合价是。(3)、(探究铁的腐蚀)该小组用下图甲装置进行实验,起始时量筒内水面处于50 mL刻度处,之后水面缓慢上升。几天后水面最终处于约(填“40”或“10”)mL刻度处,原因是。
 (4)、(拓展探究)
(4)、(拓展探究)小强同学进行如下实验:取铁钉用砂纸打磨,称其质量,按上图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
温度/℃
10
20
30
40
50
60
70
铁钉质量增加/g
0.02
0.04
0.08
0.16
0.18
0.18
0.18
小强同学的实验是探究因素对铁钉腐蚀快慢的影响,结论是。
(5)、有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因:;改进实验方案证明你的分析:。八、计算题
-
-