黑龙江省哈尔滨市南岗区2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-02-02 类型:期末考试
一、单选题
-
1. 食品的种类繁多,营养丰富。下列食品中含维生素相对较多是( )A、
 酱牛肉
B、
酱牛肉
B、 豆腐
C、
豆腐
C、 凉拌西蓝花
D、
凉拌西蓝花
D、 纯碱馒头
2. 规范的实验操作可以避免一些危险和试剂的污染等,下列实验操作不规范的是( )A、
纯碱馒头
2. 规范的实验操作可以避免一些危险和试剂的污染等,下列实验操作不规范的是( )A、 蒸发食盐水
B、
蒸发食盐水
B、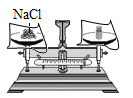 称取一定量氯化钠固体
C、
称取一定量氯化钠固体
C、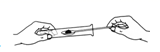 向试管中加入食盐粉末
D、
向试管中加入食盐粉末
D、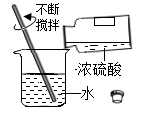 稀释浓硫酸
3. 下列过程中主要发生化学变化的是( )A、
稀释浓硫酸
3. 下列过程中主要发生化学变化的是( )A、 用氢氧化钠溶液制叶脉书签
B、
用氢氧化钠溶液制叶脉书签
B、 海水晒盐
C、
海水晒盐
C、 比较合金和纯金属的硬度
D、
比较合金和纯金属的硬度
D、 用餐具洗涤剂洗碗
4. 下列物质的用途错误的是( )A、
用餐具洗涤剂洗碗
4. 下列物质的用途错误的是( )A、 用石灰浆粉刷树木
B、
用石灰浆粉刷树木
B、 大理石做建筑材料
C、
大理石做建筑材料
C、 钛合金制造人造骨
D、
钛合金制造人造骨
D、 用生铁制造自行车架
5. 下列有关生活中的一些做法错误的是( )A、蚊虫叮咬后,为减轻痛痒,在皮肤的患处上涂牙膏 B、用食盐水除热水瓶胆内壁上沉积的水垢 C、被雨水淋湿的自行车,先用干布擦净后再用带油的布擦 D、做馒头时在面粉中加入适量的发酵粉6. 下列实验现象描述错误的是( )A、一氧化碳还原氧化铁:红棕色固体逐渐变成银白色 B、氢氧化钠固体放置于空气中:白色固体表面潮湿并逐渐溶解 C、铜丝浸入硝酸银溶液中:紫红色固体表面有银白色固体产生,溶液由无色变为蓝色 D、熟石灰与氯化铵混合研磨:白色固体中产生有氨味的气体7. 下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )A、铝单质放在空气中形成氧化膜 4Al+3O2=2Al2O3 化合反应 B、用氢氧化铝治疗胃酸过多症 Al(OH)3+3HCl=AlCl3+3H2O 中和反应 C、用稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O 复分解反应 D、比较锌和铜的活动性强弱 Cu(OH)2+Zn=Cu+Zn(OH)2↓ 置换反应8. “关爱生命,拥抱健康”是人类永恒的主题。下列叙述错误的是( )A、人类食物所供给的总能量中,有60%-70%来自糖类 B、如果人体摄入过多的油脂,容易引发肥胖和心脑血管疾病 C、人体每天约需3-5g的食盐以满足人体的正常需要 D、人体缺乏维生素A,会引起坏血病9. 蛋白质是由多种氨基酸构成的极为复杂的化合物,甘氨酸是构成人体蛋白质的氨基酸之一,如图是甘氨酸的分子结构模型图,下列对甘氨酸的叙述错误的是( )
用生铁制造自行车架
5. 下列有关生活中的一些做法错误的是( )A、蚊虫叮咬后,为减轻痛痒,在皮肤的患处上涂牙膏 B、用食盐水除热水瓶胆内壁上沉积的水垢 C、被雨水淋湿的自行车,先用干布擦净后再用带油的布擦 D、做馒头时在面粉中加入适量的发酵粉6. 下列实验现象描述错误的是( )A、一氧化碳还原氧化铁:红棕色固体逐渐变成银白色 B、氢氧化钠固体放置于空气中:白色固体表面潮湿并逐渐溶解 C、铜丝浸入硝酸银溶液中:紫红色固体表面有银白色固体产生,溶液由无色变为蓝色 D、熟石灰与氯化铵混合研磨:白色固体中产生有氨味的气体7. 下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )A、铝单质放在空气中形成氧化膜 4Al+3O2=2Al2O3 化合反应 B、用氢氧化铝治疗胃酸过多症 Al(OH)3+3HCl=AlCl3+3H2O 中和反应 C、用稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O 复分解反应 D、比较锌和铜的活动性强弱 Cu(OH)2+Zn=Cu+Zn(OH)2↓ 置换反应8. “关爱生命,拥抱健康”是人类永恒的主题。下列叙述错误的是( )A、人类食物所供给的总能量中,有60%-70%来自糖类 B、如果人体摄入过多的油脂,容易引发肥胖和心脑血管疾病 C、人体每天约需3-5g的食盐以满足人体的正常需要 D、人体缺乏维生素A,会引起坏血病9. 蛋白质是由多种氨基酸构成的极为复杂的化合物,甘氨酸是构成人体蛋白质的氨基酸之一,如图是甘氨酸的分子结构模型图,下列对甘氨酸的叙述错误的是( ) A、甘氨酸中含有四种原子 B、甘氨酸分子中含有10个原子核 C、甘氨酸中碳、氧元素质量比为3:4 D、甘氨酸是由多原子分子构成的化合物10. 下列有关资源的叙述正确的是( )A、地壳中含量最多是金属元素是铁,目前提取量最大的也是铁 B、海水中含有80多种元素,含量最多的非金属元素是氯 C、世界上铜的年产量已超过了铝,位于铁之后,居第二位 D、目前世界上已有50%以上的铁得到了回收利用11. 对下列事实的解释错误的是( )
A、甘氨酸中含有四种原子 B、甘氨酸分子中含有10个原子核 C、甘氨酸中碳、氧元素质量比为3:4 D、甘氨酸是由多原子分子构成的化合物10. 下列有关资源的叙述正确的是( )A、地壳中含量最多是金属元素是铁,目前提取量最大的也是铁 B、海水中含有80多种元素,含量最多的非金属元素是氯 C、世界上铜的年产量已超过了铝,位于铁之后,居第二位 D、目前世界上已有50%以上的铁得到了回收利用11. 对下列事实的解释错误的是( )选项
事实
解释
A
酒精溶液不能导电
溶液中没有自由移动的带电粒子
B
稀硫酸、稀盐酸都能使紫色石蕊溶液变红色
溶液中都含有氢离子
C
白色纸张沾浓硫酸后变黑
浓硫酸具有吸水性,能使纸张炭化
D
硫酸铜和氯化铜溶液都呈蓝色
溶液中都含有铜离子
A、A B、B C、C D、D12. 实验室里,区分下列各组物质的两个实验设计方案都合理的是( )选项
A
B
C
D
需区分的物质
生铁和钢
木炭粉和氧化铜
氯化钠和氢氧化钠
磷矿粉和碳酸氢铵
第一方案
分别取样,加入硫酸铜溶液,观察现象
分别取样,观察颜色
分别取样,分别加适量水溶解后,测温度变化
分别取样,观察颜色
第二方案
分别用磁铁吸引,观察现象
分别取样,再分别加入稀盐酸,观察现象
分别取样,分别加适量水溶解后,再加入稀盐酸,观察现象
分别取样,加入试管中,再分别加入稀盐酸,观察现象
A、A B、B C、C D、D13. 如图是a、b两种固体物质的溶解度曲线。下列说法中错误的是( )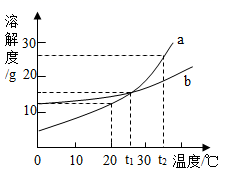 A、a、b两种物质都属于易溶性物质 B、t2℃时,将a、b的饱和溶液分别降温到t1℃时,析出的晶体的质量a比b多 C、t1℃时,a、b两种物质饱和溶液中溶质的质量分数相等 D、当a中含有少量b时,可以用降温结晶法提纯a14. 除去下列物质中的少量的杂质(括号内为杂质),所用的试剂和操作方法都错误的是( )
A、a、b两种物质都属于易溶性物质 B、t2℃时,将a、b的饱和溶液分别降温到t1℃时,析出的晶体的质量a比b多 C、t1℃时,a、b两种物质饱和溶液中溶质的质量分数相等 D、当a中含有少量b时,可以用降温结晶法提纯a14. 除去下列物质中的少量的杂质(括号内为杂质),所用的试剂和操作方法都错误的是( )选项
待提纯的物质及杂质
选用的试剂
操作方法
A
H2(CO2)
NaOH溶液
将气体通过盛有足量NaOH溶液的洗气瓶,再通过盛有足量浓硫酸的洗气瓶
B
BaSO4(BaCO3)
稀盐酸
加入足量的稀盐酸充分反应后,过滤,洗涤,干燥
C
NaCl溶液(Na2CO3)
Ba(NO3)2溶液
加入适量的Ba(NO3)2溶液,过滤,洗涤,干燥
D
ZnSO4(CuSO4)
水,锌粉
加入足量的水,再加过量锌粉,充分反应,过滤,蒸发结晶
A、A B、B C、C D、D15. 为测定某石灰石样品的纯度,将质量为12.5g的石灰石样品(杂质不含钙元素,不溶于水,也不发生任何化学反应)高温煅烧一段时间后,向所得固体中加入100g稀盐酸,恰好完全反应,过滤,所得滤液质量为105.6g,则石灰石样品的纯度为( )A、20% B、40% C、50% D、80%二、填空题
-
16. 黑龙江省是中国主要的粮食产区。黑龙江省是国内玉米、大豆的主产地之一,其中大豆(也称黄豆)产量约占全国总产量的45%,为国家粮食产量作出巨大贡献。请回答下列有关问题及填写下列空白:(1)、大豆中含有丰富的蛋白质,该营养素对人体的作用是:是构成细胞的基本物质,是机体①的主要原料,为人体活动②。(2)、如图是大豆生长时出现的症状,图中的大豆秧的一片叶子边缘发黄,若从施用化学肥料的角度看,缺少的化肥是①(填化肥的种类),这种化肥的作用是可以促进植物生长,还具有增强植物②等功能。
 17. 2020年11月19日,哈尔滨的大雪给人们出行带来诸多不便,清雪车为广大市民做出很大贡献。请回答下列问题:
17. 2020年11月19日,哈尔滨的大雪给人们出行带来诸多不便,清雪车为广大市民做出很大贡献。请回答下列问题: (1)、清雪车采用的燃料是“国V车用柴油”,这种柴油的优点是:燃烧好,油耗低,污染物排放低。这种清雪车行驶时的能量转化为(用“→”表示转化)。(2)、制造清雪车外壳用到最多的材料的种类是材料,这种材料表面要进行喷漆处理以达到防锈目的,其防锈原理是。(3)、清雪车的雪铲是采用金属材料中的锰钢制成的,这主要利用锰钢的等性能(填字母)。
(1)、清雪车采用的燃料是“国V车用柴油”,这种柴油的优点是:燃烧好,油耗低,污染物排放低。这种清雪车行驶时的能量转化为(用“→”表示转化)。(2)、制造清雪车外壳用到最多的材料的种类是材料,这种材料表面要进行喷漆处理以达到防锈目的,其防锈原理是。(3)、清雪车的雪铲是采用金属材料中的锰钢制成的,这主要利用锰钢的等性能(填字母)。A 耐高温、硬度大 B 韧性好、硬度大 C 密度小熔点低
(4)、制造清雪车的雪铲的材料是锰钢。工业上制取锰的主要原理:以软锰矿(主要成分为MnO2)为原料,用过量的焦炭作还原剂,在高温下制金属锰,同时得到一种有毒的氧化物,写出该反应的化学方程式 , 反应前后碳元素化合价的变化为。18. 分类、类比是初中化学常用的学习方法,分析和处理信息的能力也是学生必备的。(1)、不同物质根据不同标准,可以有不同的分类方法。如根据用途、性质、组成、构成等,对物质进行分类。根据所学知识,自拟分类标准,对以下物质进行分类:a 氯化钠 b 碳酸钠 c 氧化钙 d 氢氧化钠 e 氧化铁 f 浓硫酸
分类标准为① , 共包括三种物质为②(填字母)。
(2)、请根据“溶解性”表推测,硝酸铅(Pb(NO3)2)的溶解性为①(填“可溶”或“不溶”);酸可以和盐发生复分解反应,如硝酸银和盐酸发生反应的化学方程式:AgNO3+HCl=AgCl↓+HNO3 , 通过化学方程式还可以得出AgCl不溶于硝酸。根据上述规律,写出氢硫酸(H2S)与硝酸铅溶液反应的化学方程式② , 通过化学方程式还可以得出PbS在稀硝酸中③(填“可溶”或“不溶”)。三、实验题
-
19. 一般情况下,金属活动性越强,与酸反应的速度越快。为了探究金属镁、锌、铁与酸反应的快慢,某研究性学习小组设计了如下的实验。
(实验步骤)
①取A、B、C三支试管,分别加入2mL浓度相同的盐酸。
②分别将过量的、颗粒大小相同的镁、锌、铁三种金属粉末,放入相同的气球中。
③小心的把三个气球分别套在各个试管口上,如图所示。
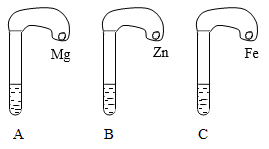
④分别将三种金属粉末倒入试管中。
(实验预测与分析)
(1)、写出锌与盐酸反应的化学方程式。(2)、气球膨胀最快的是。(填“A或B或C”)(3)、铁粉与盐酸反应的现象是。(4)、步骤④是实验获得成功的关键,你认为该操作应该注意的是:。20. 实验室现有氯酸钾、稀盐酸、石灰石等药品及下列仪器和火柴等用品,请回答问题: (1)、利用上述仪器和药品在实验室可以制取的气体是 , 反应的化学方程式为。(2)、若在实验室制取氧气,需要补充的一种药品是 , 制取氧气时,首先,要 , 确定装置不漏气后,拔开橡胶塞,在试管中装入药品。用带有导管的橡胶塞塞紧管口,③固定在铁架台上,加热过程中,因试管内 , 压强增大,大于外界压强,在压强差的作用下收集到氧气。(3)、若要制取纯净的氧气,需要将制得的气体通过盛有的洗气瓶,若用10号装置,进气孔应从(填“b”或“c”)口进入。
(1)、利用上述仪器和药品在实验室可以制取的气体是 , 反应的化学方程式为。(2)、若在实验室制取氧气,需要补充的一种药品是 , 制取氧气时,首先,要 , 确定装置不漏气后,拔开橡胶塞,在试管中装入药品。用带有导管的橡胶塞塞紧管口,③固定在铁架台上,加热过程中,因试管内 , 压强增大,大于外界压强,在压强差的作用下收集到氧气。(3)、若要制取纯净的氧气,需要将制得的气体通过盛有的洗气瓶,若用10号装置,进气孔应从(填“b”或“c”)口进入。四、推断题
-
21. 如图所示,A~F是初中化学常见的物质,它们分别是Fe、CuSO4、NaOH、H2SO4、Ca(OH)2、Na2CO3中的一种,A是黑色粉末,B和E可以用来配制波尔多液。方框内之间的连线表示二者可以发生反应,箭头表示一种物质可以转化为另一种物质。请回答下列问题:(以上反应或转化均在溶液中进行,且在初中范围内)
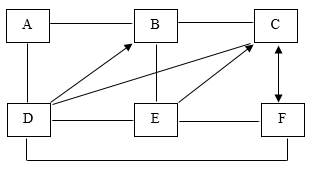 (1)、请写出A和F两种物质的化学式为:A , F。(2)、写出D与E反应的化学方程式;(3)、写出足量的C溶液加入到B溶液反应的实验现象为。
(1)、请写出A和F两种物质的化学式为:A , F。(2)、写出D与E反应的化学方程式;(3)、写出足量的C溶液加入到B溶液反应的实验现象为。五、综合应用题
-
22. 张南和化学兴趣小组的同学为了测定铁样品中铁的质量分数(杂质不含铁元素,不溶于水,也不与其他物质发生反应),进行了如下实验:

请回答下列问题:
(1)、上述实验过程中发生反应的化学方程式为;(2)、根据已知条件列出求解所加稀硫酸中溶质质量(x)的比例式;(3)、此铁样品中铁的质量分数为;(4)、用98%的浓硫酸配制100g上述稀硫酸,所需浓硫酸的质量为;(5)、所得不饱和溶液A中溶质的质量分数为;(6)、若要用含氧化铁80%的赤铁矿生产上述铁样品1000t,需要赤铁矿的质量为。六、科学探究题
-
23. 有一包白色粉末,含有硝酸钠、碳酸钠和硫酸钡,张南将这包白色粉末与稀盐酸(水足量)混合后,固体质量随时间变化关系如图所示。张南和小岗同学想对所得溶液溶质的成分进行实验探究,请你帮助两位同学完成如下实验及回答相关问题。
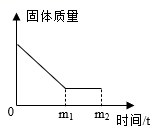
(提出问题)烧杯中溶液的溶质成分是什么?
(1)、(猜想与假设)张南同学猜想溶质成分是:NaNO3、NaCl、HCl
小岗同学猜想溶质成分是:NaNO3、NaCl、Na2CO3
你的猜想是;
张南猜想的理由是。
(2)、(实验验证)张南同学为了验证自己的猜想取少量滤液于试管中,向其中滴加少量硝酸银溶液观察到有白色沉淀的实验现象,于是得出结论:自己的猜想正确。请对张南同学由实验得出的的结论进行评价;
(3)、小岗同学取少量滤液于试管中,向其中滴加少量稀硫酸,观察到有气泡产生的实验现象,于是得出结论:同学的猜想正确。(4)、则由图像得出有关硫酸钡的性质有。(5)、(反思与总结)通过上述张南、小岗两位同学对溶液溶质成分的猜想,总结出猜想所得溶液中溶质成分时除需考虑可溶性的生成物和可溶性的反应物外,还需考虑的物质。
-
-