黑龙江省大庆市肇源县2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-02-02 类型:期末考试
一、单选题
-
1. 3月22日是“世界水日”,下列关于水的说法正确的是()A、生活中用肥皂水鉴别硬水和软水,利用活性炭的吸附性来降低水的硬度 B、自然界水的循环过程中实现了水的自身净化 C、自来水厂净水的过程有静置沉淀、过滤、吸附、蒸馏 D、从电解水得到H2和O2 , 可知水是由氢分子和氧分子组成的2. 下列实验不能成功的是()A、用注射器压缩空气证明分子之间有间隔 B、用铁丝在空气中燃烧的方法证明铁与氧气在点燃的条件下能发生反应 C、将氢气通过灼热的氧化铜证明氢气具有还原性 D、在敞口容器中进行铁和硫酸铜溶液的反应证明质量守恒定律3. 下列关于金属的说法正确的是( )A、焊锡是纯净的锡 B、铝制品属 于不可回收垃圾 C、铁在潮湿空气中容易生锈 D、纯铜的硬度大于青铜4. 化学使生活更美好,下列做法不可行的是( )A、用洗洁精的乳化作用,清洗衣服上沾的油污 B、增大压强,使汽水中溶有的CO2更多 C、苹果汁呈酸性,用于治疗胃酸过多 D、用医用氯化钠,可配制浓度为0.9%的生理盐水5. 氢化锂(LiH)是一种生氢原料,其中氢元素的化合价为( )A、-1 B、+1 C、0 D、-26. 在生产三氧化铬的化学方程式 中,X的化学式为( )A、H2SO4 B、H2SO3 C、H2S D、SO27. 如图是电解水的简易实验装置,下列有关叙述错误的是( )
 A、a、b分别是电源的正极、负极 B、在水中加入少许硫酸钠不能增强导电性 C、电解水实验表明,溶液中的离子可以导电 D、理论上若得到的氧气约amL,可同时得到约2amL氢气8. 进行量筒里液体读数时,开始仰视读数为29.0mL,倒出一部分液体后,俯视读数为12.3mL,则实际倒出的液体体积为( )A、16.7mL B、大于16.7mL C、小于16.7mL D、无法确定9. 下列关于碳和碳的氧化物的说法正确的是( )A、石墨和C540都是碳原子构成的混合物 B、CO2能使被石蕊染为紫色的干花变红 C、高温下,CO和C都能与CuO发生置换反应 D、CO具有还原性、可燃性等化学性质,一定条件下可转变为CO210. 向盛有一定量的铝粉的小烧杯中逐滴加入稀硫酸至过量,如图是反应过程中烧杯中物质总质量Y随加入稀硫酸的质量X变化的关系,其中正确的是( )A、
A、a、b分别是电源的正极、负极 B、在水中加入少许硫酸钠不能增强导电性 C、电解水实验表明,溶液中的离子可以导电 D、理论上若得到的氧气约amL,可同时得到约2amL氢气8. 进行量筒里液体读数时,开始仰视读数为29.0mL,倒出一部分液体后,俯视读数为12.3mL,则实际倒出的液体体积为( )A、16.7mL B、大于16.7mL C、小于16.7mL D、无法确定9. 下列关于碳和碳的氧化物的说法正确的是( )A、石墨和C540都是碳原子构成的混合物 B、CO2能使被石蕊染为紫色的干花变红 C、高温下,CO和C都能与CuO发生置换反应 D、CO具有还原性、可燃性等化学性质,一定条件下可转变为CO210. 向盛有一定量的铝粉的小烧杯中逐滴加入稀硫酸至过量,如图是反应过程中烧杯中物质总质量Y随加入稀硫酸的质量X变化的关系,其中正确的是( )A、 B、
B、 C、
C、 D、
D、 11. 如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置。并在装置中盛放大约半瓶蒸馏水。以下说法正确的是( )
11. 如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置。并在装置中盛放大约半瓶蒸馏水。以下说法正确的是( ) A、b导管连接供给氧气的钢瓶 B、a导管连接病人吸氧气的塑胶管 C、如果用此装置收集氧气,先在瓶中装满水,然后氧气应该从a导管进入 D、如果用此装置收集氧气,先在瓶中装满水,然后氧气应该从b导管进入12. 与以下三个实验操作相对应的溶液pH变化的图象正确的是( )
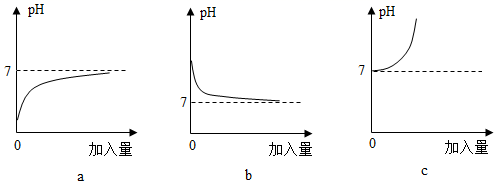
A、b导管连接供给氧气的钢瓶 B、a导管连接病人吸氧气的塑胶管 C、如果用此装置收集氧气,先在瓶中装满水,然后氧气应该从a导管进入 D、如果用此装置收集氧气,先在瓶中装满水,然后氧气应该从b导管进入12. 与以下三个实验操作相对应的溶液pH变化的图象正确的是( )①氢氧化钠溶液中加水;②水中加入氢氧化钠溶液;③盐酸中加水。
 A、a、b、c B、c、a、b C、b、c、a D、a、c、b13. 下列图像能正确反映其对应实验的是( )A、往一定量的双氧水中加入少量二氧化锰
A、a、b、c B、c、a、b C、b、c、a D、a、c、b13. 下列图像能正确反映其对应实验的是( )A、往一定量的双氧水中加入少量二氧化锰 B、用两份等质量、等浓度的过氧化氢溶液分别制取氧气
B、用两份等质量、等浓度的过氧化氢溶液分别制取氧气  C、将水通电一段时间
C、将水通电一段时间  D、等质量的铁和锌与足量的稀盐酸反应
D、等质量的铁和锌与足量的稀盐酸反应  14. 6月5日为世界环境日,2018年我国环境日的主题是“美丽中国,我是行动者”。下列认识或做法错误的是( )
14. 6月5日为世界环境日,2018年我国环境日的主题是“美丽中国,我是行动者”。下列认识或做法错误的是( )
A、倡导“低碳”生活,多乘公共交通工具 B、减少化石燃料的使用,降低SO2和NO2等气体的排放 C、分类回收废旧电池,有利于保护环境 D、为使粮食增产,应大量使用农药化肥15. 化学就在我们身边,只要你注意就会发现。下列说法中错误的是( )A、热固性塑料成型后再受热不会软化,可用于制造电源插座、开关 B、合成橡胶的弹性、耐磨性、绝缘性等性能优良,广泛应用于轮胎和制鞋工业 C、脂肪、糖类、动物蛋白都是人体必需的营养素,人们可以大量摄入,多吃无害 D、人体缺铁会导致贫血,人们可以食用加入铁强化剂的酱油来预防16. 下列归纳总结完全正确的一组是( )化学与健康
化学与能源
①要牢记“吸烟有害健康”、“毒品万万试不得”
②人体缺乏维生素A会引起夜盲症
①煤、石油、天然气都是不可再生的化石燃料
②电池充电时,化学能转化为电能
化学与安全
化学与环境
①皮肤沾上浓硫酸,用大量水冲洗后涂上 的碳酸氢钠溶液
②用工业用盐一一亚硝酸钠腌渍咸菜
①多建设火电厂,增加电力供应
②绿色化学就是指人类绿化环境、植树造林
A、A B、B C、C D、D17. 下列四个图像中,能正确反映对应变化关系的是( )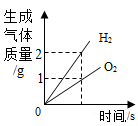
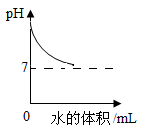
A.用CuFe2O4-x做催化剂,光分解水制氢气与氧气
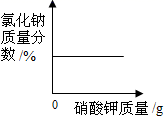
B.向氯化钠的饱和溶液中加入硝酸钾
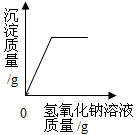
C.向混有少量硫酸的硫酸铜溶液中加入氢氧化钠溶液
D.向一定质量的碳酸钠溶液中加水
A、A B、B C、C D、D18. 现有CO2和SO3两种物质,它们中氧元素的质量比为1:1,则碳元素与硫元素的质量比为( )A、9:16 B、16:9 C、6:5 D、5:619. 推理是研究和学习化学的一种重要方法。正电子、负质子都是反粒子,它们跟通常所说的电子、质子相比较,质量相等,但电性相反。科学家已发现反氢原子。你推测反氢原子的结构可能是( )A、由一个带正电的质子和一个带负电的电子构成 B、只由一个带正电的电子构成 C、只由一个带负电的质子构成 D、由一个带负电的质子和一个带正电的电子构成20. M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物质M进行了如图2所示实验。下列说法错误的是( ) A、物质M是硝酸钾 B、溶液②中溶质质量分数为37.5% C、溶液①②③中,溶质质量分数的关系是②>③>① D、溶液①为不饱和溶液,溶液②和③为饱和溶液
A、物质M是硝酸钾 B、溶液②中溶质质量分数为37.5% C、溶液①②③中,溶质质量分数的关系是②>③>① D、溶液①为不饱和溶液,溶液②和③为饱和溶液二、流程题
-
21. 我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有铁Fe、锡Sn、铜Cu、银Ag、金Au等金属,如图是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
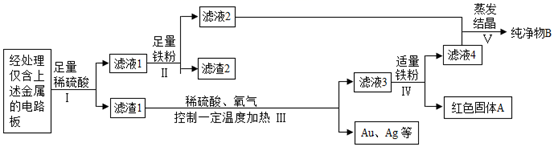 (1)、过程Ⅰ、Ⅲ、Ⅳ均涉及的操作是 , 该操作需要用到一种金属材料制成的仪器是。(2)、写出过程Ⅱ中反应的化学方程式、。(3)、写出过程Ⅲ中反应的化学方程式。(4)、滤液4的主要成分(水除外)是。
(1)、过程Ⅰ、Ⅲ、Ⅳ均涉及的操作是 , 该操作需要用到一种金属材料制成的仪器是。(2)、写出过程Ⅱ中反应的化学方程式、。(3)、写出过程Ⅲ中反应的化学方程式。(4)、滤液4的主要成分(水除外)是。三、综合应用题
-
22. 水和溶液与我们的生活息息相关。(1)、将厨房中的下列物质:胡椒、花生油、面粉、白糖分别放入水中,能形成溶液的是。(2)、消毒液碘酒中的溶剂是(写名称)。(3)、甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:

①在t2℃时,甲的溶解度为 , 把30g甲溶解在50g水中得到溶液的质量为克。
②把N点甲的溶液转化为M点溶液的方法(写一种)。
③将甲、乙、丙三种物质的饱和溶液从t3℃降到t2℃,溶质质量分数由大到小的顺序是。
④要配制等质量t3℃的甲、乙、丙三种物质的饱和溶液,所需水的质量最多是。配制过程中若量取水时仰视读数,则会造成所配溶液的溶质质量分数。(“偏大”或“偏小”)
四、填空题
-
23. 化学就在我们身边,它与我们的生产、生活息息相关。(1)、选用下列物质的标号填空。
A.碳酸钙 B.钛合金 C.臭氧 D.硫酸 E.干冰
①鸡蛋壳的主要成分是;②可用于人工降雨的是;③可用于金属表面除锈的是;④可用于制作眼镜架的材料是;⑤主要分布在距地面10~50km的高空,能吸收大部分紫外线,保护地球生物的是。
(2)、①目前,人类使用的燃料大多来自化石燃料,如、石油和天然气等。②埋藏于海底,将来可能会替代化石燃料的新能源是(填“可燃冰”“氢气”或“汽油”)。
五、科学探究题
-
24. 小晨同学从课外读物中得知:在加热条件下,钠与CO2反应的产物可能有C、CO、Na2CO3、Na2O。于是设计实验对产物成分进行探究。
(查阅资料)①BaCl2溶液呈中性;②4Na+O2=2Na2O;③Na2O+H2O=2NaOH;④2Na+2H2O=2NaOH+H2↑;⑤CO通入PdCl2溶液中有黑色沉淀生成。
(提出问题)在加热条件下,钠与CO2反应的产物有哪些?
(猜想假设)猜想一:产物中一定有C 猜想二:产物中一定有CO
猜想三:产物中一定有Na2CO3猜想四:产物中一定有Na2O
(1)、(实验验证)用下图所示装置(夹持装置已略去)进行实验探究。
装置A中发生反应的化学方程式为;装置C的作用是。
序号
实验操作
实验现象
实验结论
⑴
待钠完全反应后,将装置D中的固体置于烧杯中,加蒸馏水溶解
有黑色不溶物
猜想正确
⑵
将实验(1)所得混合物过滤,取滤液加入过量BaCl2溶液
猜想三正确
⑶
猜想二正确
(2)、(反思与评价)小晨同学向实验(2)所得溶液中滴入几滴酚酞溶液,溶液呈红色。 于是得出结论:在加热条件下,钠与CO2反应一定产生Na2O。该结论是否严谨?(填“是”或“否”),理由是。25. 学习了铁在空气中生锈条件后,小明和小红对铜在空气中生锈条件产生了浓厚的兴趣,他们进行了如下探究过程:(查阅资料)铜锈是绿色的,俗称铜绿,主要成分是碱式碳酸铜 ,铜绿加热能分解生成一种常见的氧化物。
(1)、(猜测)小红猜测铜生锈与空气中的下列物质有关:①CO2②O2③N2④H2O小明认为铜生锈与氮气一定无关,依据是。
(2)、(实验探究)小明设计了如图所示的实验,几天后观察到,A试管中铜片在水面附近有绿色物质,B、C、D试管中铜片均无明显现象。请帮助分析实验过程并回答下列问题:
根据上述实验得出,铜生锈与空气中相关物质有。
(3)、通过A试管现象,上述实验 (用序号表示)对比说明铜生锈与氧气一定有关。(4)、(实验反思)通过学习,他们认为铁和铜在空气中更易生锈的是;理由是。(5)、(探究拓展)设计实验探究铜绿受热分解的生成物是什么?有CO2生成,检验生成CO2的化学方程式为。
(6)、生成物中有氧化铜,可观察到的现象是。(7)、请写出铜绿受热分解的化学方程式。六、计算题
-
26. 碳酸锶(SrCO3)可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO3和NaCl固体混合物中SrCO3的质量分数,在三个烧杯中进行相关实验,实验所用稀盐酸的溶质的质量分数相同。所得数据如下表所示:
烧杯编号
①
②
③
稀盐酸质量/g
100
200
300
固体混合物质量/g
100
100
100
反应后烧杯中物质的质量/g
195.6
291.2
391.2
试求:
(1)、烧杯②中产生CO2的质量为g。(2)、原固体混合物中SrCO3的质量分数(计算结果精确到0.1%)。(提示:SrCO3+2HCl=SrCl2+CO2↑+H2O)
-
-
-