2016年黑龙江省大庆市中考化学试卷
试卷更新日期:2016-07-12 类型:中考真卷
一、选择题(本大题共10小题,每小题4分,共40分.每小题只有一个选项符合要求)
-
1. 如图所示的实验操作,正确的是( )A、
 酒精灯使用
B、
酒精灯使用
B、 液体的量取
C、
液体的量取
C、 向试管中加入固体
D、
向试管中加入固体
D、 用滴管滴液
2. 下列叙述属于化学变化的是( )A、石蜡熔化成液体 B、稀释浓盐酸 C、碘的升华 D、生石灰遇水转变为熟石灰3. 根据你所学过的化学知识,判断下列说法错误的是( )A、炒完菜后,应及时擦掉锅底水分,这样可以防止铁锅生锈 B、碳酸氢钠俗称小苏打,可用做治疗胃酸的胃药 C、被蚊虫叮咬后可以涂抹肥皂水或小苏打水以减轻疼痛 D、工业酒精有杀菌消毒的作用,主要成分为甲醇4. “分类法”是学习化学的重要方法之一,某同学对所学的部分化学物质进行分类,其中完全正确的是( )
用滴管滴液
2. 下列叙述属于化学变化的是( )A、石蜡熔化成液体 B、稀释浓盐酸 C、碘的升华 D、生石灰遇水转变为熟石灰3. 根据你所学过的化学知识,判断下列说法错误的是( )A、炒完菜后,应及时擦掉锅底水分,这样可以防止铁锅生锈 B、碳酸氢钠俗称小苏打,可用做治疗胃酸的胃药 C、被蚊虫叮咬后可以涂抹肥皂水或小苏打水以减轻疼痛 D、工业酒精有杀菌消毒的作用,主要成分为甲醇4. “分类法”是学习化学的重要方法之一,某同学对所学的部分化学物质进行分类,其中完全正确的是( )选项
甲
乙
丙
丁
A
氧化物
NO
H2O2
CuO
B
污染物
CO2
PM2.5
SO2
C
有机物
CH4
CO
C2H5OH
D
纯净物
空气
盐酸
CaCO3
A、A B、B C、C D、D5. “冰毒”是毒性极强的毒品之一,其化学式为C10H15N,下列有关冰毒解释错误的是( )A、冰毒是由碳、氢、氮三种元素组成的化合物 B、冰毒是一种有机物,完全燃烧只生成CO2和H2O C、冰毒中氮原子的原子结构示意图为 D、冰毒中碳、氢两种元素质量比为25:3
6. 下列化学方程式与事实相符且正确的是( )A、碳在氧气中完全燃烧2C+O2
D、冰毒中碳、氢两种元素质量比为25:3
6. 下列化学方程式与事实相符且正确的是( )A、碳在氧气中完全燃烧2C+O2 2CO
B、用足量澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O
C、用稀盐酸除铁锈:2HCl+FeO═FeCl2+H2O
D、用足量NaOH溶液在加热条件下检验NH4HCO3中NH4+:NaOH+NH4HCO3
2CO
B、用足量澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O
C、用稀盐酸除铁锈:2HCl+FeO═FeCl2+H2O
D、用足量NaOH溶液在加热条件下检验NH4HCO3中NH4+:NaOH+NH4HCO3 NH3↑+NaHCO3
7. 除去下列物质中少量杂质所加入试剂合理的是( )
NH3↑+NaHCO3
7. 除去下列物质中少量杂质所加入试剂合理的是( )选项
物质
所含杂质
除去杂质所加试剂
A
Ca(OH)2
CaCO3
盐酸
B
MgCl2
NaCl
硝酸银溶液
C
C
Fe
稀硫酸
D
CO2
HCl
氢氧化钠溶液
A、A B、B C、C D、D8. 下列说法错误的是( )A、铁丝在氧气中燃烧有黑色固体生成 B、浓硫酸可做干燥剂是因为浓硫酸具有脱水性 C、废水中含有酸性物质必须先用碱性物质中和成中性以后才能排放 D、石墨质软滑腻,能导电、导热、耐高温9. 如图所示的四个图象,能正确反映对应变化关系的是( )A、 Ca(OH)2的溶解度与温度的变化曲线
B、
Ca(OH)2的溶解度与温度的变化曲线
B、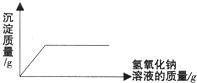 向硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
C、
向硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
C、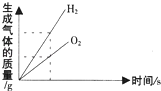 水的电解
D、
水的电解
D、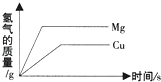 分别向等质量的镁和铜固体中逐滴加入盐酸
10.
分别向等质量的镁和铜固体中逐滴加入盐酸
10.铜屑表面呈绿色,欲利用其制取胆矾,某课外活动小组同学设计了如下制取流程,有关该流程说法正确的是( )
 A、操作①所用的玻璃仪器有烧杯、玻璃棒 B、铜屑表面呈绿色的物质俗称铜绿,化学式为Cu2(OH)2CO3 C、由固体B制取硫酸铜溶液的过程中,方法1更符合绿色化学要求 D、操作②的步骤为将硫酸铜溶液加热蒸干
A、操作①所用的玻璃仪器有烧杯、玻璃棒 B、铜屑表面呈绿色的物质俗称铜绿,化学式为Cu2(OH)2CO3 C、由固体B制取硫酸铜溶液的过程中,方法1更符合绿色化学要求 D、操作②的步骤为将硫酸铜溶液加热蒸干二、填空题(本大题包括5小题,共29分)
-
11. 回答下列问题:(1)、空气中含量最多的是 . (填化学式)(2)、防毒面具中使用了活性炭,这是利用了活性炭的作用.(3)、天然气的主要成分为 . (填化学式)(4)、煤燃烧生成CO2、SO2、CO等气体,其中会引起温室效应的是;溶于水会形成酸雨的是;能与人体血红蛋白结合的是 .12. 已知Na2O2为淡黄色粉末,常温下可与H2O剧烈反应,化学方程式为2Na2O2+2H2O═4NaOH+O2↑,因此Na2O2可用于制取O2 .
根据以上信息回答下列问题:
(1)、Na2O2中氧元素的化合价为 .(2)、若用Na2O2与H2O反应制取O2 , 可以选用图中哪个发生装置 .

若用同样装置还可选用、物质(填化学式)制取O2 , 写出该反应的化学方程式 .
13.室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
 (1)、由如图可知,盐酸与氢氧化钠溶液中和反应是(填“吸热”或“放热”或“无热量变化”)反应.(2)、在A处溶液中加入石蕊,溶液呈色.(3)、B处溶液的溶质是(填化学式).(4)、B到C的过程中溶液的pH逐渐(填“增大”或“减小”或“无变化”).(5)、在C点溶液中加入碳酸钙,现象为 , 化学方程式为 .14.
(1)、由如图可知,盐酸与氢氧化钠溶液中和反应是(填“吸热”或“放热”或“无热量变化”)反应.(2)、在A处溶液中加入石蕊,溶液呈色.(3)、B处溶液的溶质是(填化学式).(4)、B到C的过程中溶液的pH逐渐(填“增大”或“减小”或“无变化”).(5)、在C点溶液中加入碳酸钙,现象为 , 化学方程式为 .14.A~H表示初中化学常见物质,它们之间转化关系如图所示(部分生成物已略去)

其中A为红棕色固体,反应①为冶金工业的重要反应,且B、D组成元素相同,C、F为金属单质,其它物质为化合物,其中F为紫红色,H为白色沉淀.
请按要求填空:
(1)、写出下列物质的化学式:ADE(2)、①~④的反应中属于置换反应的是(填序号).(3)、反应①的化学方程式为 .15.有一工业过程:

按要求回答下列问题:
(1)、请将电石与水反应的化学方程式补充完整:CaC2+2H2O═Ca(OH)2+↑.(2)、有关物质常温下的溶解度如表:物质
Ca(ClO3)2
CaCl2
KClO3
KCl
溶解度/g
209.0
74.5
7.3
34.2
上述流程中加入了KCl粉末,KCl与(填化学式)发生了复分解反应得KClO3晶体,该过程得到KClO3晶体的原因是 .
(3)、写出向CaCl2溶液中通入两种气体生成CaCO3的化学方程式: .三、实验题(本大题包括2小题,共23分)
-
16.
氨对工业及国防具有重要意义,下图为某化学小组同学模拟工业合成氨原理设计如图实验.

完成以下实验中相关问题:
检查装置气密性.
(1)、关闭ac,打开b,从长颈漏斗中加入稀盐酸,A中发生反应生成氢气的化学方程式为 , 在E出口处收集H2并验纯.(2)、关闭a、b、c在盛满空气的多孔玻璃钟罩内用激光点燃足量白磷,此操作的目的是 .(3)、待多孔玻璃钟罩冷却到室温,先打开a,再加热D处的酒精灯,最后打开止水夹 , H2、N2在催化剂的作用下生成NH3 , 该反应的化学方程式为 . 实验过程中C装置的作用是 , E装置的现象为 , 此现象说明NH3溶于水后溶液呈性.(4)、实验室用固体Ca(OH)2和固体NH4Cl混合在加热条件下制NH3 , 应选用如图哪个装置(填“A”或“B”),该反应的化学方程式为 .
 17. Ⅰ.小茗同学利用硫酸铜溶液进行趣味实验,他将浸泡了硫酸铜溶液的滤纸在酒精灯火焰上点燃,观察到滤纸颜色变白,由湿变干后燃烧,在燃烧后的灰烬中出现了红色固体,他很好奇,进行了相关探究,请填写有关空白.
17. Ⅰ.小茗同学利用硫酸铜溶液进行趣味实验,他将浸泡了硫酸铜溶液的滤纸在酒精灯火焰上点燃,观察到滤纸颜色变白,由湿变干后燃烧,在燃烧后的灰烬中出现了红色固体,他很好奇,进行了相关探究,请填写有关空白.[实验目的]探究红色固体组成
(1)、[查阅资料]①温度达200℃时,白色CuSO4开始分解生成CuO和另一种氧化物,此反应前后各元素化合价保持不变,请写出CuSO4开始分解时的化学方程式 .
②温度超过1000℃时,CuO分解生成Cu2O,Cu2O呈红色,可与稀硫酸反应,化学方程式为:Cu2O+H2SO4═CuSO4+Cu+H2O
(2)、[做出猜想]假设红色固体成分:①可能是Cu②可能是Cu2O③还可能是的混合物.(3)、[实验探究及推理]若取少量红色固体于试管中,加入稀硫酸:①若固体不溶解,溶液仍呈无色,确定红色固体为 , 同时也说明滤纸燃烧时的温度低于℃.
②若固体溶解,溶液呈蓝色,是否可以确定红色固体成分(填“是”或“否”),原因是 .
③Ⅱ.小茗同学又做了氢气还原氧化铜的实验,结果试管内壁上粘有紫红色物质,老师给了一瓶稀盐酸,请问在实验室条件下如何洗净该试管?简述操作过程 .
四、计算题(共8分)
-
18. 向含10g NaOH的溶液中通入一定量的CO2 , 然后在低压条件下蒸干得12.6g白色固体,通过计算确定该白色固体的成分及其各组成成分的质量(写出计算过程).
[查阅资料]1、Na2CO3+CO2+H2O═2NaHCO32、NaHCO3溶液在低压蒸干条件下得到的固体不分解.