山西省太原市2020-2021学年高一上学期化学期中考试试卷
试卷更新日期:2021-01-26 类型:期中考试
一、单选题
-
1. 分子学说的提出,使人们对物质结构的认识发展到一个新的阶段。提出分子学说的科学家是( )A、拉瓦锡
 B、门捷列夫
B、门捷列夫  C、阿伏加德罗
C、阿伏加德罗  D、道尔顿
D、道尔顿  2. 进行焰色试验时,用于清洗铂丝的液体是( )A、水 B、酒精 C、稀盐酸 D、稀硫酸3. 下列物质中,含有氯分子的是( )A、漂白粉 B、氯水 C、氯化氢气体 D、氯化铜溶液4. 图中X所表示的基本类型的反应是( )
2. 进行焰色试验时,用于清洗铂丝的液体是( )A、水 B、酒精 C、稀盐酸 D、稀硫酸3. 下列物质中,含有氯分子的是( )A、漂白粉 B、氯水 C、氯化氢气体 D、氯化铜溶液4. 图中X所表示的基本类型的反应是( ) A、化合反应 B、分解反应 C、置换反应 D、复分解反应5. 电视剧《三十而已》中多次提及的“蓝色烟花”,是烟花设计师心中的最高梦想。制作“蓝色烟花”的盐不常见,且稳定性差,该盐可能是( )A、NaCl B、KOH C、Na2CO3 D、CuCl6. 下列生成CO2的反应中,属于非氧化还原反应的是( )A、C+O2 CO2 B、H2CO3=H2O+CO2↑ C、CH4+2O2 CO2+2H2O D、CO+CuO Cu+CO27. 在无色透明的溶液中能大量共存的一组离子是( )A、Na+、K+、 、 B、Fe2+、K+、 、 C、K+、Ca2+、 、 D、Na+、H+、 、8. 朱自清在(荷塘月色》中写道:“薄薄的青雾浮起在荷塘里….…光是隔了树照过来的,高处丛生的灌木落下参差的斑驳的黑影……”。下列关于“月光穿过薄雾”的说法,正确的是( )A、光是一种胶体 B、发生了丁达尔效应 C、雾的分散质是空气 D、雾中的小水滴直径大于100nm9. 实现“I-→I2”的转化,需要加入( )A、氧化剂 B、还原剂 C、氧化产物 D、还原产物10. 在200mL0.5mol/LCaCl2溶液中,Cl-的物质的量浓度是( )A、0.1mol/L B、0.2mol/L C、0.5mol/L D、1mol/L11. 向某溶液中加入Ba(OH)2溶液后生成白色沉淀,加入足量稀盐酸后沉淀部分溶解,同时有无色无味的气体生成,将该气体通入澄清石灰水,澄清石灰水变浑浊。下列离子组符合上述现象的是( )A、 、 B、 、 C、Cl-、 D、 、OH-12. 石墨烯是用微机械剥离法从石墨中分离出的单层石墨,被认为是一种未来革命性的材料。下列说法正确的是( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应5. 电视剧《三十而已》中多次提及的“蓝色烟花”,是烟花设计师心中的最高梦想。制作“蓝色烟花”的盐不常见,且稳定性差,该盐可能是( )A、NaCl B、KOH C、Na2CO3 D、CuCl6. 下列生成CO2的反应中,属于非氧化还原反应的是( )A、C+O2 CO2 B、H2CO3=H2O+CO2↑ C、CH4+2O2 CO2+2H2O D、CO+CuO Cu+CO27. 在无色透明的溶液中能大量共存的一组离子是( )A、Na+、K+、 、 B、Fe2+、K+、 、 C、K+、Ca2+、 、 D、Na+、H+、 、8. 朱自清在(荷塘月色》中写道:“薄薄的青雾浮起在荷塘里….…光是隔了树照过来的,高处丛生的灌木落下参差的斑驳的黑影……”。下列关于“月光穿过薄雾”的说法,正确的是( )A、光是一种胶体 B、发生了丁达尔效应 C、雾的分散质是空气 D、雾中的小水滴直径大于100nm9. 实现“I-→I2”的转化,需要加入( )A、氧化剂 B、还原剂 C、氧化产物 D、还原产物10. 在200mL0.5mol/LCaCl2溶液中,Cl-的物质的量浓度是( )A、0.1mol/L B、0.2mol/L C、0.5mol/L D、1mol/L11. 向某溶液中加入Ba(OH)2溶液后生成白色沉淀,加入足量稀盐酸后沉淀部分溶解,同时有无色无味的气体生成,将该气体通入澄清石灰水,澄清石灰水变浑浊。下列离子组符合上述现象的是( )A、 、 B、 、 C、Cl-、 D、 、OH-12. 石墨烯是用微机械剥离法从石墨中分离出的单层石墨,被认为是一种未来革命性的材料。下列说法正确的是( ) A、石墨烯是有机物 B、石墨烯由分子构成 C、石墨与金刚石互为同素异形体 D、石墨能导电,所以石墨是电解质13. 下列有关Na2CO3和NaHCO3的说法,正确的是( )A、NaHCO3溶于水时吸热 B、Na2CO3的俗名是小苏打 C、Na2CO3比NaHCO3的溶解度小 D、Na2CO3溶液比NaHCO3溶液的pH小14. 下列离子方程式书写正确的是( )A、向氧化铜中滴加稀盐酸O2-+2H+=H2O B、铁片插入硝酸银溶液中Fe+Ag+=Fe2++Ag C、氯化亚铁溶液与稀硫酸混合Fe2++ =FeSO4 D、稀硝酸滴在大理石上CaCO3+2H+=Ca2++H2O+CO2↑15. 下列有关氧化物的说法正确的是( )A、CO属于酸性氧化物 B、氧化物中氧元素一定为-2价 C、大多数金属氧化物属于碱性氧化物 D、碱性氧化物与酸反应不一定生成盐和水16. 2019年国庆庆典,天安门前放飞了7万颗气球,其中填充的是比氢气更为安全的氦气。下列对于同温同压下,相同体积的氢气和氦气的比较,错误的是( )A、质量之比为1:2 B、原子数之比为1:1 C、密度之比为1:2 D、物质的量之比为1:117. 如图是NaCl固体溶解并形成水合离子的示意图,下列说法正确的是( )
A、石墨烯是有机物 B、石墨烯由分子构成 C、石墨与金刚石互为同素异形体 D、石墨能导电,所以石墨是电解质13. 下列有关Na2CO3和NaHCO3的说法,正确的是( )A、NaHCO3溶于水时吸热 B、Na2CO3的俗名是小苏打 C、Na2CO3比NaHCO3的溶解度小 D、Na2CO3溶液比NaHCO3溶液的pH小14. 下列离子方程式书写正确的是( )A、向氧化铜中滴加稀盐酸O2-+2H+=H2O B、铁片插入硝酸银溶液中Fe+Ag+=Fe2++Ag C、氯化亚铁溶液与稀硫酸混合Fe2++ =FeSO4 D、稀硝酸滴在大理石上CaCO3+2H+=Ca2++H2O+CO2↑15. 下列有关氧化物的说法正确的是( )A、CO属于酸性氧化物 B、氧化物中氧元素一定为-2价 C、大多数金属氧化物属于碱性氧化物 D、碱性氧化物与酸反应不一定生成盐和水16. 2019年国庆庆典,天安门前放飞了7万颗气球,其中填充的是比氢气更为安全的氦气。下列对于同温同压下,相同体积的氢气和氦气的比较,错误的是( )A、质量之比为1:2 B、原子数之比为1:1 C、密度之比为1:2 D、物质的量之比为1:117. 如图是NaCl固体溶解并形成水合离子的示意图,下列说法正确的是( ) A、NaCl固体中不存在离子 B、NaCl溶液中存在自由移动的离子 C、该过程可以表示为NaCl+H2O=Na++Cl-+H++OH- D、熔融的NaCl中也存在水合钠离子和水合氯离子18. 下列选项中,“甲→乙→丙”的每一步转化,不能通过一步反应实现的是( )
A、NaCl固体中不存在离子 B、NaCl溶液中存在自由移动的离子 C、该过程可以表示为NaCl+H2O=Na++Cl-+H++OH- D、熔融的NaCl中也存在水合钠离子和水合氯离子18. 下列选项中,“甲→乙→丙”的每一步转化,不能通过一步反应实现的是( )甲
乙
丙
A
Cu
CuO
Cu(OH)2
B
CaO
Ca(OH)2
CaCO3
C
Na
NaOH
Na2SO4
D
O2
H2O
H2
A、A B、B C、C D、D19. NA表示阿伏加德罗常数的值,下列说法正确的是( )A、27gAl3+所含电子数为3NA B、常温常压下,28g氮气所含原子数为2NA C、0.1mol·L-1NaOH溶液中含OH-数为0.1NA D、标准状况下,4.48L乙醇所含分子数为0.2NA20. 同学们用手持技术对新制饱和氯水在光照条件下0~150s内的导电率进行监测,下列图像正确的是( )A、 B、
B、 C、
C、 D、
D、
二、综合题
-
21. 在抗击2020年春季新冠疫情的过程中,由H、C、O、Na、Cl等元素组成的物质发挥了巨大的作用。(1)、请用上述元素组成相应的物质,完成下列问题。
物质类别
①
②
盐
有机物
化学式
Cl2
HClO
③
④
消毒对象
自来水
自来水
游泳池、家俱、地板
人体皮肤
表格中的①②③④分别是① , ②,③ , ④。
(2)、同学们设计了两种方案生产HClO:方案一:Cl2→HClO
方案二:③→HClO
你认为方案较好,理由是。
22. 钠在生活、生产、科研中有重要应用。(1)、钠灯是道路照明的主要光源。钠灯照明时产生色光,其穿雾能力很强。(2)、用镊子取一小块钠,用滤纸吸干表面的后,进行图I所示的实验(夹持仪器已略去),试管中发生反应的化学方程式是。充分反应后,待试管冷却,进行图II所示的实验,发生反应的化学方程式是 , 再向其中滴加几滴酚酞溶液,可能观察到的现象是。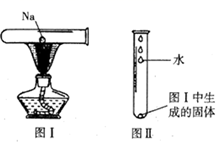 23. 碱式硫酸铁[化学式Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,可由FeSO4和KClO3在水溶液中反应得到,有关反应的化学方程式如下:6FeSO4+KClO3+_=6Fe(OH)SO4+KCl(1)、请将上述化学方程式补充完整。(2)、用双线桥法标出上述反应中转移电子的方向和数目。(3)、上述反应中的还原剂是 , 被还原的元素是 , 每1molFeSO4参加反应,转移电子mol。24. 同学们在实验室中用下图装置制备纯净干燥的氯气。
23. 碱式硫酸铁[化学式Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,可由FeSO4和KClO3在水溶液中反应得到,有关反应的化学方程式如下:6FeSO4+KClO3+_=6Fe(OH)SO4+KCl(1)、请将上述化学方程式补充完整。(2)、用双线桥法标出上述反应中转移电子的方向和数目。(3)、上述反应中的还原剂是 , 被还原的元素是 , 每1molFeSO4参加反应,转移电子mol。24. 同学们在实验室中用下图装置制备纯净干燥的氯气。 (1)、仪器a的名称是 , 装置A中发生反应的化学方程式是。(2)、装置B的作用是 , 装置C中盛装的药品是。(3)、虚线框内连接装置E时,接口顺序应该是b→→c(填管口字母)。(4)、装置D中发生反应的化学方程式是。
(1)、仪器a的名称是 , 装置A中发生反应的化学方程式是。(2)、装置B的作用是 , 装置C中盛装的药品是。(3)、虚线框内连接装置E时,接口顺序应该是b→→c(填管口字母)。(4)、装置D中发生反应的化学方程式是。某同学在实验室配制80mL1mol·L-1的NaOH溶液用于上述实验:
①该同学应选择mL的容量瓶,需称取NaOH的质量为g。
②下图是配制过程中的几个步骤。

正确步骤的顺序是(填字母),若所配溶液浓度偏大,可能的一个原因是。
25. 用纯净干燥的氯气与铜反应,装置如下图所示。(已知:生成物为粉末状,易潮解) (1)、实验前先通一会儿氯气以排出装置内的空气,判断氯气已充满整个装置的简单方法是。(2)、干燥的氯气通过灼热铜粉时,A中可观察到 , 有关反应的化学方程式是。(3)、用氯气将A中的生成物吹入B中进行冷却收集,B与A相连的导管较粗,其目的是。实验结束后,取下B,向其中倒入水,振荡,观察到溶液的颜色是 , 说明其中含有离子。26. 为了探究铁与氯气的反应,某同学设计了如下实验装置。(部分夹持仪器已略去)
(1)、实验前先通一会儿氯气以排出装置内的空气,判断氯气已充满整个装置的简单方法是。(2)、干燥的氯气通过灼热铜粉时,A中可观察到 , 有关反应的化学方程式是。(3)、用氯气将A中的生成物吹入B中进行冷却收集,B与A相连的导管较粗,其目的是。实验结束后,取下B,向其中倒入水,振荡,观察到溶液的颜色是 , 说明其中含有离子。26. 为了探究铁与氯气的反应,某同学设计了如下实验装置。(部分夹持仪器已略去) (1)、实验开始前需进行的一项操作是。(2)、加热玻璃管中的铁丝约1min,打开弹簧夹,推动注射器的活塞注入一定量氯气,玻璃管内的现象是 , 有关反应的化学方程式是。(3)、用氯气将玻璃管内的少量生成物吹入氢氧化钠溶液中,预测试管中可能产生的现象是。连接B与C的导管较粗,其目的是。27. 我国近代化学工业的奠基人之一侯德榜发明的“侯氏制碱法”,将制碱技术发展到了一个新的水平,在此基础上,将工业纯碱(含Mg2+、Fe3+、Cl-等杂质)进行提纯。工艺流程如下:
(1)、实验开始前需进行的一项操作是。(2)、加热玻璃管中的铁丝约1min,打开弹簧夹,推动注射器的活塞注入一定量氯气,玻璃管内的现象是 , 有关反应的化学方程式是。(3)、用氯气将玻璃管内的少量生成物吹入氢氧化钠溶液中,预测试管中可能产生的现象是。连接B与C的导管较粗,其目的是。27. 我国近代化学工业的奠基人之一侯德榜发明的“侯氏制碱法”,将制碱技术发展到了一个新的水平,在此基础上,将工业纯碱(含Mg2+、Fe3+、Cl-等杂质)进行提纯。工艺流程如下:
请回答下列问题。
(1)、母液I中含有NH4Cl,NH4Cl的电离方程式是。(2)、反应II的化学方程式是。(3)、流程中加入NaOH除去的杂质离子是。(4)、结晶后的Na2CO3晶体表面附着有NaCl等杂质,需洗涤除去。检验NaCl是否已被洗涤除尽,需进行的操作和现象是 , 有关反应的离子方程式是。28. A~E为中学化学常见纯净物,其中A可用于焙制糕点,B是生活中常用的一种调味品,也是重要的化工原料。D、E均为气体,F的水溶液是一种强酸。它们之间的转化关系如下。(部分反应物、生成物已略去)
请回答下列问题:
(1)、写出下列物质的化学式:A , B , C。(2)、A→B的离子方程式是。(3)、D与E反应的化学方程式是 , 反应现象是。29. A~F为中学化学常见纯净物,其中A、B的水溶液均显碱性,B是一种可用于制药的盐。C是生活中常用的一种调味品也是重要的化工原料。F的水溶液是一种强酸。它们之间的转化关系如下。(部分反应物、生成物和反应条件已略去)
请回答下列问题:
(1)、写出下列物质的化学式:A , B , C , F。(2)、A→B的化学方程式是。(3)、C的溶液通电后,发生反应的离子方程式是。三、计算题