浙教版科学 八年级下 第二章 第3节 原子结构的模型
试卷更新日期:2021-01-20 类型:同步测试
一、单选题
-
1. 如图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
 A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子中b与c的数目一定相同 D、原子中a与c的数目一定相同2. 原子论开辟了从微观世界认识物质及其变化的新纪元。下列哪位科学家最早提出了原子的概念( )A、牛顿 B、爱因斯坦 C、道尔顿 D、阿基米德3. 我国著名科学家张青莲教授主持测定了铕等9种原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( )A、63 B、89 C、152 D、2154. 决定元素种类的是( )A、电子数 B、中子数 C、最外层电子数 D、质子数5. 下列关于原子核构成的说法正确的是( )A、一般由质子和电子构成 B、一般由质子和中子构成 C、一般由电子和中子构成 D、一般由质子、中子和电子构成6. 俄罗斯科学家利用第72号元素铪和第74号元素钨精确测出月球至少比地球早700万年形成。铪、钨两种元素原子本质的不同是( )A、核内质子数目 B、核内中子数目 C、核外电子数目 D、相对原子质量7. 下列关于元素的理解,正确的是( )A、元素的种类取决于该元素原子的核外电子数 B、中子数相等的原子的统称叫元素 C、元素既论种数,也可计个数 D、自然界中所有的物质都是由元素组成的8. 科学家用质子数为20的钙离子,轰击核电荷数为98的锎元素靶,使两种元素的原子核合并在一起,合成核电荷数为118的新元素。对此理解正确的是( )A、新元素的原子核外电子数为116 B、新元素的原子序数为118 C、新元素的原子中子数为118 D、变化过程中元素种类没有发生变化9. 随着世界经济的快速增长,对能源的需求也越来越大,核能作为清洁的能源,对于缓解能源紧张局面,减轻环境污染具有积极作用。已知某核电站的核原料为铀235,其原子核内含有92个质子和143个中子,那么( )A、该原子核外有143个电子 B、该元素是非金属元素 C、该原子的相对质量为235克 D、该原子核带92个单位的正电荷10. 根据下列表格信息可知,互为同位素原子的是( )
A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子中b与c的数目一定相同 D、原子中a与c的数目一定相同2. 原子论开辟了从微观世界认识物质及其变化的新纪元。下列哪位科学家最早提出了原子的概念( )A、牛顿 B、爱因斯坦 C、道尔顿 D、阿基米德3. 我国著名科学家张青莲教授主持测定了铕等9种原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( )A、63 B、89 C、152 D、2154. 决定元素种类的是( )A、电子数 B、中子数 C、最外层电子数 D、质子数5. 下列关于原子核构成的说法正确的是( )A、一般由质子和电子构成 B、一般由质子和中子构成 C、一般由电子和中子构成 D、一般由质子、中子和电子构成6. 俄罗斯科学家利用第72号元素铪和第74号元素钨精确测出月球至少比地球早700万年形成。铪、钨两种元素原子本质的不同是( )A、核内质子数目 B、核内中子数目 C、核外电子数目 D、相对原子质量7. 下列关于元素的理解,正确的是( )A、元素的种类取决于该元素原子的核外电子数 B、中子数相等的原子的统称叫元素 C、元素既论种数,也可计个数 D、自然界中所有的物质都是由元素组成的8. 科学家用质子数为20的钙离子,轰击核电荷数为98的锎元素靶,使两种元素的原子核合并在一起,合成核电荷数为118的新元素。对此理解正确的是( )A、新元素的原子核外电子数为116 B、新元素的原子序数为118 C、新元素的原子中子数为118 D、变化过程中元素种类没有发生变化9. 随着世界经济的快速增长,对能源的需求也越来越大,核能作为清洁的能源,对于缓解能源紧张局面,减轻环境污染具有积极作用。已知某核电站的核原料为铀235,其原子核内含有92个质子和143个中子,那么( )A、该原子核外有143个电子 B、该元素是非金属元素 C、该原子的相对质量为235克 D、该原子核带92个单位的正电荷10. 根据下列表格信息可知,互为同位素原子的是( )质子数 中子数 电子数 M 12 12 10 N 10 10 10 O 11 11 11 P 11 12 10 Q 11 12 11
A、M、N、P B、O、Q C、O、P D、O、P、Q二、填空题
-
11. 月球上的23He蕴藏量巨大,地球上的氦元素主要以24He形式存在。从原子的构成来看,23He、24He两种原子的数不同,化学性质基本相同,互称为原子。12. 在原子中,核电荷数==。原子核和核外电子所带的电量大小相等,电性相反,因而原子呈电。13. 原子不是构成物质的最小微粒,它还能再分,原子是由带正电荷的和带负电荷的构成的。原子核在原子中所占的体积 , 核外电子在核外空间做。通过实验,科学家们最终发现,原子核是由更小的两种粒子——和构成。14. 下表是小明收集的一些微粒的资料,请根据表格数据,回答下列问题。
粒子名称
质子数
中子数
电子数
A
14
14
14
B
26
30
24
C
14
14
18
D
14
18
14
(1)、B微粒所带的电性为。(填“不带电”、“带正电”或“带负电”)(2)、与A互为同位素原子的是。15. 如图,其中①②③表示三种原子,“ ”“O,.“o”表示原子中的不同微粒。
”“O,.“o”表示原子中的不同微粒。 ②原子中质子数为;①②③中属于同种元素的原子是。

三、实验探究题
-
16. 人们为了揭示原子结构的奥秘,经历了漫长的探究过程。以下是英国科学家卢瑟福进行的探究。
【过程与现象】1911年英国科学家卢瑟福进行了著名的α粒子(带正电)轰击金箔实验。结果发现:绝大多数α粒子穿过金箔后仍沿原方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的几乎达到180°,像是被金箔弹了回来。
【解释与结论】
(1)、绝大多数α粒子穿过金箔后方向不变,说明;(2)、通过上述实验,可推出的原子结构模型为;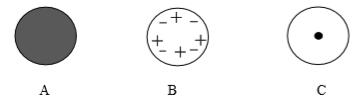 (3)、【分析与应用】当α粒子轰击金箔时,如图所示的运动轨迹不可能是(填字母)。
(3)、【分析与应用】当α粒子轰击金箔时,如图所示的运动轨迹不可能是(填字母)。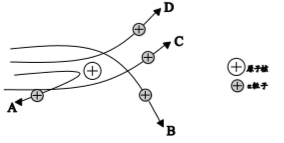 17. 人类对原子结构的认识永无止境。请根据所学知识回答:(1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均 (填“正确”或“错误”)。
17. 人类对原子结构的认识永无止境。请根据所学知识回答:(1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均 (填“正确”或“错误”)。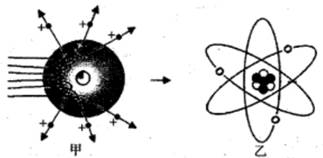 (2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。
(2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。四、解答题
-
18. 伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是:一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆森通过实验发现了电子,进一步发展了原子、分子论。汤姆森主要是纠正了“道尔顿原子论”中的观点。
1911年,卢瑟福又通过实验,推测原子是由和核外电子构成,并提出了沿用至今的现代原子结构理论。
(2)、道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样,对实验现象进行解释的过程叫做。原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了来表达他们的理论成果。
