浙教版科学 八年级下 第三章 第4节 二氧化碳
试卷更新日期:2021-01-20 类型:同步测试
一、单选题
-
1. 在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。下图是他的主要实验步骤,其中操作有误的是( )A、
 加入药品
B、
加入药品
B、 收集气体
C、
收集气体
C、 检查装置气密性
D、
检查装置气密性
D、 验满
2. 如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化。据此,你认为该同学应该( )
验满
2. 如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化。据此,你认为该同学应该( ) A、继续用大针筒向澄清石灰水压入空气 B、撤去大针筒,用嘴向澄清石灰水吹气 C、得出空气中没有二氧化碳的结论 D、得出空气中含有少量二氧化碳的结论3. 证明空气中含有CO2气体,最合理的做法是( )A、仔细闻空气,是否有二氧化碳气味 B、通过吸管往装有澄清石灰水的试管中吹气,石灰水变浑浊 C、用打气筒向装有澄清石灰水的试管中压入空气,石灰水变浑浊 D、燃着的木条放在空气中观察是否熄灭4. 实验室制CO2时,一般有如下五个步骤:①检查装置的气密性;②按要求装配好仪器;③向长颈漏斗注入稀盐酸;④向反应器中放入几块大理石;⑤收集二氧化碳气体.正确的顺序是( )A、①②③④⑤ B、①②④③⑤ C、②①④③⑤ D、②④①③⑤5. 下列关于实验室制取二氧化碳气体的说法不正确的是( )A、不能用排水法收集二氧化碳是因为二氧化碳能溶于水 B、一般不选用粉末状的碳酸钠与稀盐酸反应,因为二者反应速率太快 C、能选用石灰石与稀硫酸作原料,生产二氧化碳气体 D、实验室制取二氧化碳和利用双氧水制取氧气的装置相同,因为都是反应物状态相同且不需要加热6. 在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”.如图是他的主要实验步骤,其中操作有误的是( )A、
A、继续用大针筒向澄清石灰水压入空气 B、撤去大针筒,用嘴向澄清石灰水吹气 C、得出空气中没有二氧化碳的结论 D、得出空气中含有少量二氧化碳的结论3. 证明空气中含有CO2气体,最合理的做法是( )A、仔细闻空气,是否有二氧化碳气味 B、通过吸管往装有澄清石灰水的试管中吹气,石灰水变浑浊 C、用打气筒向装有澄清石灰水的试管中压入空气,石灰水变浑浊 D、燃着的木条放在空气中观察是否熄灭4. 实验室制CO2时,一般有如下五个步骤:①检查装置的气密性;②按要求装配好仪器;③向长颈漏斗注入稀盐酸;④向反应器中放入几块大理石;⑤收集二氧化碳气体.正确的顺序是( )A、①②③④⑤ B、①②④③⑤ C、②①④③⑤ D、②④①③⑤5. 下列关于实验室制取二氧化碳气体的说法不正确的是( )A、不能用排水法收集二氧化碳是因为二氧化碳能溶于水 B、一般不选用粉末状的碳酸钠与稀盐酸反应,因为二者反应速率太快 C、能选用石灰石与稀硫酸作原料,生产二氧化碳气体 D、实验室制取二氧化碳和利用双氧水制取氧气的装置相同,因为都是反应物状态相同且不需要加热6. 在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”.如图是他的主要实验步骤,其中操作有误的是( )A、 加入药品
B、
加入药品
B、 收集气体
C、
收集气体
C、 检查装置的气密性
D、
检查装置的气密性
D、 验满
7. 下列实验方法和操作中,正确的是( )
验满
7. 下列实验方法和操作中,正确的是( )①实验室用石灰石和稀硫酸制备二氧化碳时,收满二氧化碳的集气瓶应正立在桌面上
②实验室用锌和稀硫酸制备氢气时,收满氢气的集气瓶应倒立在桌面上
③点燃任何可燃性气体前,必须先验纯
④制备任何气体时,都要把反应装置中的空气排尽后,再用排水法收集.
A、①②③④ B、①②③ C、②③ D、②④8. 下列有关二氧化碳的实验中,只能证明二氧化碳物理性质的是( )A、 将二氧化碳通入滴有石蕊试液的水中
B、
将二氧化碳通入滴有石蕊试液的水中
B、 将二氧化碳倒入放有阶梯蜡烛的烧杯中
C、
将二氧化碳倒入放有阶梯蜡烛的烧杯中
C、 将呼出的气体吹入澄清石灰水中
D、
将呼出的气体吹入澄清石灰水中
D、 将二氧化碳倒入一侧的“空”纸袋中
9. 若用二氧化碳气体吹肥皂泡,并用燃着的木条击破肥皂泡,现象分别是( )A、肥皂泡上升,木条火焰不熄灭 B、肥皂泡时升时降,木条继续燃烧 C、肥皂泡下沉,木条燃烧更旺 D、肥皂泡下沉,木条火焰熄灭10. 将足量的二氧化碳气体持续不断地通入澄清石灰水中时,通入的二氧化碳体积与产生沉淀质量变化符合下列图像中的( )A、
将二氧化碳倒入一侧的“空”纸袋中
9. 若用二氧化碳气体吹肥皂泡,并用燃着的木条击破肥皂泡,现象分别是( )A、肥皂泡上升,木条火焰不熄灭 B、肥皂泡时升时降,木条继续燃烧 C、肥皂泡下沉,木条燃烧更旺 D、肥皂泡下沉,木条火焰熄灭10. 将足量的二氧化碳气体持续不断地通入澄清石灰水中时,通入的二氧化碳体积与产生沉淀质量变化符合下列图像中的( )A、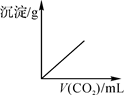 B、
B、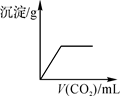 C、
C、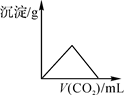 D、
D、 11. 如图,集气瓶中充满二氧化碳,大烧杯中燃着2支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
11. 如图,集气瓶中充满二氧化碳,大烧杯中燃着2支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )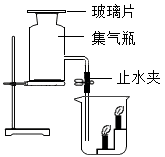 A、将观察到高的蜡烛先熄灭 B、不移开玻璃片,实验现象更明显 C、蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点 D、去掉烧杯中的1支蜡烛,也能得出同样的实验结论12. 为研究二氧化碳与氢氧化钠是否发生反应,王新兴同学设计的下列方案最不可行的是( )A、
A、将观察到高的蜡烛先熄灭 B、不移开玻璃片,实验现象更明显 C、蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点 D、去掉烧杯中的1支蜡烛,也能得出同样的实验结论12. 为研究二氧化碳与氢氧化钠是否发生反应,王新兴同学设计的下列方案最不可行的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题
-
13.
小晨同学在研究二氧化碳气体的性质时,进行了如图所示的实验。
 (1)、二氧化碳通常用大理石和稀盐酸反应制取,一般用法收集。(2)、向漏斗中倾倒二氧化碳,燃着的蜡烛自下而上熄灭,由此说明二氧化碳具有的性质是。14. 二氧化碳的相对分子质量为 , 密度比空气(填“大”或“小“),可用法收集.15. 二氧化碳的用途:①. 作气体肥料,可促进植物的 。②. 工业和食品原料,可用于制 、尿素和汽水。③.灭火,二氧化碳既不能 也不支持 ,密度比空气 。④制冷剂,干冰升华 热,可用于人工降雨。16. 二氧化碳的物理性质:常温常压下为无色气体,密度比空气 ; 溶于水。加压、降温,二氧化碳可转化为固态;固态的二氧化碳叫做 。17. 二氧化碳在空气中只占 , 但它是绿色植物进行作用中并不可少的原料之一。通常状况下,二氧化碳是一种色 味的气体,其密度比空气的密度 ,溶于水。在一定条件下,二氧化碳变成固体,俗称 。18. 二氧化碳在空气中只占 , 但它是作用中并不可少的物质之一.通常状况下,二氧化碳是一种 色 味的气体,其密度比空气的密度 , 溶于水.在一定条件下,二氧化碳变成固体,俗称 .
(1)、二氧化碳通常用大理石和稀盐酸反应制取,一般用法收集。(2)、向漏斗中倾倒二氧化碳,燃着的蜡烛自下而上熄灭,由此说明二氧化碳具有的性质是。14. 二氧化碳的相对分子质量为 , 密度比空气(填“大”或“小“),可用法收集.15. 二氧化碳的用途:①. 作气体肥料,可促进植物的 。②. 工业和食品原料,可用于制 、尿素和汽水。③.灭火,二氧化碳既不能 也不支持 ,密度比空气 。④制冷剂,干冰升华 热,可用于人工降雨。16. 二氧化碳的物理性质:常温常压下为无色气体,密度比空气 ; 溶于水。加压、降温,二氧化碳可转化为固态;固态的二氧化碳叫做 。17. 二氧化碳在空气中只占 , 但它是绿色植物进行作用中并不可少的原料之一。通常状况下,二氧化碳是一种色 味的气体,其密度比空气的密度 ,溶于水。在一定条件下,二氧化碳变成固体,俗称 。18. 二氧化碳在空气中只占 , 但它是作用中并不可少的物质之一.通常状况下,二氧化碳是一种 色 味的气体,其密度比空气的密度 , 溶于水.在一定条件下,二氧化碳变成固体,俗称 .三、实验探究题
-
19. 科学是一门以实验为基础的学科,实验是学习科学的一条重要途径。下面我们就实验室制取二氧化碳的收集问题作如下讨论:根据二氧化碳的性质,它可溶于水也能与水反应生成碳酸,通常采用排空气集气法收集,二氧化碳真的就不能用排水法收集吗?
资料一:文献表明1体积水要完全溶解1体积二氧化碳,至少需要约7天的时间。如果是1天时间,则1体积水大约只能溶解 体积的二氧化碳。
资料二:对任何气体的收集,凡能用排水法收集的气体,最好用排水法收集,这样既可以观察集气的快慢,又可以提高被收集气体的纯度。
资料三:二氧化碳不溶于饱和的碳酸氢钠溶液。
(1)、你认为在中学科学实验中是否可以用排水法收集二氧化碳气体? , 你的观点是。(2)、要使实验室收集二氧化碳达到最优化,你是否还有更好的建议:。20. 如图是教材中“二氧化碳的溶解性实验”﹣﹣向一个收集满二氧化碳气体的质地较软的塑料瓶中加入约 体积的水,立即旋紧瓶盖,观察塑料瓶的变化.请问 (1)、指出仪器A的名称 .(2)、实验操作中,旋紧瓶盖后,还须进行的操作是 .(3)、最后可观察到的实验现象是 .(4)、实验时得出的结论是二氧化碳能溶于水,化学方程式 .21.
(1)、指出仪器A的名称 .(2)、实验操作中,旋紧瓶盖后,还须进行的操作是 .(3)、最后可观察到的实验现象是 .(4)、实验时得出的结论是二氧化碳能溶于水,化学方程式 .21.如图所示是实验室制取气体的常用装置,请根据要求回答问题:
 (1)、仪器b的名称是;
(1)、仪器b的名称是;
(2)、实验室制取二氧化碳应选择的发生装置和收集装置分别为和;(3)、利用装置A制取氧气时,反应的化学方程式是;(4)、下面是排水集气法的实验操作,正确的顺序是(填序号).①待集气瓶内充满气体后,盖上玻璃片再移出水槽
②等到气泡连续且均匀时,再将导管口移入集气瓶
③将集气瓶注满水,用玻璃盖盖上瓶口,倒立在盛水的水槽中.
(5)、甲烷(CH4)密度比空气小,难溶于水,实验室常用加热无水醋酸钠晶体与和碱石灰的混合物来制备甲烷.请你从上图中选出制取一瓶甲烷所需要的装置组合为 .
22. 某种大理石的主要成分为CaCO3 , 还含有少量的硫化物。小金用这种大理石、质量分数为36%的浓盐酸等制取CO2 , 并测定CO2的相对分子质量。请回答:(1)、若要将溶质质量分数为36%的浓盐酸稀释成溶质质量分数为10%的稀盐酸,需要的仪器有烧杯、玻璃棒和(2)、为了得到纯净的二氧化碳以测定CO2的相对分子质量,设计了如图所示装置,请你分析:
①用这种大理石和稀盐酸反应制备的CO2气体中,可能含有的杂质是。
②如图装置中,B物质不可能是。
A.五氧化二磷 B.无水氯化钙 C.碱石灰 D.生石灰
③如果B物质失效,并用如图实验得到的气体测定CO2的相对分子质量,测定结果(填“偏高”“偏低”或“不受影响”)。
23. 学习了 CO2的相关知识之后,小明对 CO2 的性质进行三个实验。
图一:探究 CO2 在水中的溶解能力。
①试剂瓶加满蒸馏水后,恰好 200 mL,塞紧橡皮塞;
②用针筒抽取 200 mLCO2;连接装置,缓慢推动活塞,将 CO2 注入瓶内;
③当注入 CO2 气体体积达到 120 mL 时,红色油柱开始向上移动。则表明在该条件下,1体积水中能溶解体积 CO2。
图二:验证 CO2 的密度比空气大,应选装置易成功。
图三:验证 CO2 能否与 NaOH、Ca(OH)2 反应。
①关闭 K1 , 打开 K2 , 缓缓通入 600 mL CO2 , 丙、丁容器中均无明显现象;
②打开 K1 , 打开 K2 , 继续通入 CO2 , 丁容器中出现浑浊。
根据上述现象,可推断 CO2。
A.一定能与 NaOH 反应 B.可能与 NaOH 反应
C.一定能与 Ca(OH)2 反应 D.可能与 Ca(OH)2 反应。
下列对NaOH和Ca(OH)2的性质叙述:
①都是白色固体 ②都易溶于水放出大量热 ③溶液都使酚酞试液变红
④都能与酸发生反应 ⑤溶液通入CO2都变浑浊 ⑥与Na2CO3反应都变浑浊以上表述错误的是。
四、解答题
-
24. 为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各 6 克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图。每 2 分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前 18 分钟数据如下。

时间/分
0
2
4
6
8
10
12
14
16
18
大理石碎屑生成的 CO2 质量/克
0
1.45
1.75
1.98
2.18
2.30
2.36
2.40
2.40
2.40
块状大理石生成的 CO2 质量/克
0
0.45
0.80
1.10
1.36
1.60
1.81
1.98
2.11
2.20
(1)、实验过程中,通过观察如图装置中的哪一现象可判断反应结束?。(2)、结合表格分析,块状大理石与稀盐酸反应最多能生成克二氧化碳?(3)、当反应进行到18 分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(写出计算过程)