江西省吉安市七校联盟2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-01-20 类型:期中考试
一、单选题
-
1. 下列变化中,只发生了物理变化的是( )
A、铁生锈 B、纸张燃烧 C、葡萄酿成酒 D、水结成冰2. 空气是一种宝贵的自然资源,由多种物质组成。下列说法错误的是( )A、稀有气体可制成多种用途的电光源 B、氧气可用作火箭发射的燃料 C、二氧化碳是植物光合作用的基本原料 D、氮气可用作保护气3. 正确的化学实验操作是实验成功的重要保证.下列实验操作正确的是( )A、 倾倒液体
B、
倾倒液体
B、 过滤
C、
过滤
C、 检查气密性
D、
检查气密性
D、 检验氧气是否收集满
4. 交警使用的一种酒精检测仪中装有重铬酸钾(K2Cr2Ox),能够和酒精发生化学反应,通过反应现象判断驾驶员是否饮酒。K2Cr2Ox中铬元素的化合价为+6价,则X的值为( )A、4 B、5 C、6 D、75. 下列实验现象的描述中,正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、硫在氧气中燃烧,发出蓝紫色火焰 C、细铁丝在空气中燃烧,火星四射,生成黑色固体 D、镁条在空气中燃烧发出耀眼的白光,生成氧化镁6. 科学家研制出以锶原子为钟摆的“晶格钟”成为世界上最精准的钟.锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )
检验氧气是否收集满
4. 交警使用的一种酒精检测仪中装有重铬酸钾(K2Cr2Ox),能够和酒精发生化学反应,通过反应现象判断驾驶员是否饮酒。K2Cr2Ox中铬元素的化合价为+6价,则X的值为( )A、4 B、5 C、6 D、75. 下列实验现象的描述中,正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、硫在氧气中燃烧,发出蓝紫色火焰 C、细铁丝在空气中燃烧,火星四射,生成黑色固体 D、镁条在空气中燃烧发出耀眼的白光,生成氧化镁6. 科学家研制出以锶原子为钟摆的“晶格钟”成为世界上最精准的钟.锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )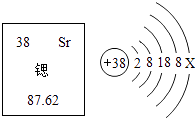 A、Sr为金属元素 B、乙图中X=2 C、锶原子的质量为87.62g D、锶原子的质子数是387. 下列对宏观事实的微观解释错误的是( )A、夏天钢轨之间的缝隙变小——原子受热时体积变大 B、闻到远处饭菜的香味——分子在不断地运动 C、氢气和液氢都可做燃料——相同物质的分子,其化学性质相同 D、水的三态变化一一分子的间隔发生了改变8. 根据下列三种微粒结构示意图,所获取信息正确的是( )
A、Sr为金属元素 B、乙图中X=2 C、锶原子的质量为87.62g D、锶原子的质子数是387. 下列对宏观事实的微观解释错误的是( )A、夏天钢轨之间的缝隙变小——原子受热时体积变大 B、闻到远处饭菜的香味——分子在不断地运动 C、氢气和液氢都可做燃料——相同物质的分子,其化学性质相同 D、水的三态变化一一分子的间隔发生了改变8. 根据下列三种微粒结构示意图,所获取信息正确的是( ) A、②③化学性质相同 B、②表示的元素是非金属元素 C、它们表示两种元素 D、①表示的是原子,②表示的是阴离子9. 逻辑推理是一种重要的化学思维方法,下列推理合理的是( )A、单质是由一种元素组成的,所以由一种元素组成的物质一定是单质。 B、氧化物是含有氧元素的化合物,所以含氧元素的化合物一定是氧化物。 C、离子是带电的原子或原子团,所以带电的粒子一定是离子 D、化学变化中分子发生改变,所以分子发生改变的变化一定是化学变化10. 下列图像能正确反映对应变化关系的是( )A、
A、②③化学性质相同 B、②表示的元素是非金属元素 C、它们表示两种元素 D、①表示的是原子,②表示的是阴离子9. 逻辑推理是一种重要的化学思维方法,下列推理合理的是( )A、单质是由一种元素组成的,所以由一种元素组成的物质一定是单质。 B、氧化物是含有氧元素的化合物,所以含氧元素的化合物一定是氧化物。 C、离子是带电的原子或原子团,所以带电的粒子一定是离子 D、化学变化中分子发生改变,所以分子发生改变的变化一定是化学变化10. 下列图像能正确反映对应变化关系的是( )A、 将水通电电解一段时间
B、
将水通电电解一段时间
B、 加热一定量的高锰酸钾固体
C、
加热一定量的高锰酸钾固体
C、 加热等质量的氯酸钾
D、
加热等质量的氯酸钾
D、 向一定量的二氧化锰中加入过氧化氢溶液
向一定量的二氧化锰中加入过氧化氢溶液
二、选择填充题
-
11. 下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是()
A.H B.Ne C.O2 D.
12. 化学是一门以实验为基础的学科,下列实验操作正确的是()A.用镊子小心地将块状固体放入垂直的试管中
B.用玻璃棒搅拌加快过滤
C.用10mL量筒量取9.5 mL NaCl溶液
D.用酒精灯烧杯中的液体加热需要垫
13. 下列化学用语中“2”表示的含义正确的是()A 2H:“2”表示2个氢分子
B Mg2+:“2”表示镁元素的化合价为+2
C CO2:“2”表示1个CO2分子中含有2个氧原子
D Fe2+:“2”表示
14. 分类是研究物质的常用方法。如图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圆圈表示纯净物,则下列物质属于Z的范围的是()
A.氧气 B.干冰 C.氯酸钾 D.
15. “苏丹红1号”(C16H12N2O)是一种工业染料,属致癌物质,严禁作为食用色素,有关“苏丹红1号”的叙述正确的是()A.氢元素和氮元素的质量比为3:7
B.属于氧化物
C.“苏丹红1号”中含有31个原子
D.
三、填空题
-
16. 请根据题目要求,用化学用语填空:(1)、地壳中含量最多的金属元素:。(2)、2个硫酸根离子:。(3)、氦气的化学式:。(4)、碳的氧化物中碳元素的化合价为+4:。17. 如图中A是锡元素在周期表中的信息,B、C分别为两种粒子的结构示意图,D为元素周期表中的部分信息,请根据图中信息回答。
 (1)、锡元素的相对原子质量是。(2)、B表示的原子,其核外电子数是;若C表示氯离子,则X= , 该粒子符号为。(3)、元素在周期表中的分布是有规律的,D中甲的原子序数(填“大于”或“小于”)乙的原子序数。乙所代表的元素,属于(填“金属”或“非金属”)元素。18. 水是一种重要的资源,爱护水资源,人人有责。(1)、某同学用如图所示的装置进行电解水实验,实验前向水中加入少量硫酸钠,其目的 , 该反应的文字表达式是。(2)、下列做法会造成水体污染的是(填序号)。
(1)、锡元素的相对原子质量是。(2)、B表示的原子,其核外电子数是;若C表示氯离子,则X= , 该粒子符号为。(3)、元素在周期表中的分布是有规律的,D中甲的原子序数(填“大于”或“小于”)乙的原子序数。乙所代表的元素,属于(填“金属”或“非金属”)元素。18. 水是一种重要的资源,爱护水资源,人人有责。(1)、某同学用如图所示的装置进行电解水实验,实验前向水中加入少量硫酸钠,其目的 , 该反应的文字表达式是。(2)、下列做法会造成水体污染的是(填序号)。①工业废水处理达标后排放
②随意丢弃废旧电池
③提倡使用无磷洗衣粉
④合理使用化肥和农药
(3)、下列净化水的过程中,说法错误的是(填字母)。
A 活性炭可吸附水中的色素和有异味的物质
B 明矾可以使硬水转化为软水
C 自来水厂净化水的方法主要有沉淀、过滤、吸附、消毒杀菌
(4)、我省部分地县多年干旱,严重缺水,因地制宜利用水资源迫在眉睫。打井取用地下水,可用检验地下水是硬水还是软水,日常生活中可以利用的方法降低水的硬度。19. 在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如下图所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟。请你根据所学知识回答下列问题:
 (1)、上述反应过程可用上图表示,则氨气的化学式为 , 该反应中各元素化合价的说法正确的是(填字母);
(1)、上述反应过程可用上图表示,则氨气的化学式为 , 该反应中各元素化合价的说法正确的是(填字母);A 所有元素化合价都不变
B 有一种元素化合价改变
C 有两种元素化合价改变
D 所有元素化合价都改变
(2)、分析以上微观模拟图,你能得出的结论是:①;②。(3)、如果这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是。四、综合题
-
20. 现有A-G七种物质,“→”表示一种物质经一步反应可以转化为另一种物质(部分反物、生成物及反条件已略去)。A生成气体C的同时还会生成B和D,D是实验室制取C的一种催化剂,E和F常温下为液体且组成元素相同,C生成G的过程中有火星四射的现象。请回答下列问题:
 (1)、写出物质A的化学式:;(2)、物质C的一种用途:;(3)、反应E→F的基本反应类型:;(4)、写出反应C→G的文字表达式:。21. 实验桌上摆放有如图所示的装置,请回答下列问题:
(1)、写出物质A的化学式:;(2)、物质C的一种用途:;(3)、反应E→F的基本反应类型:;(4)、写出反应C→G的文字表达式:。21. 实验桌上摆放有如图所示的装置,请回答下列问题: (1)、编号为①的仪器名称为。(2)、不经改进的B装置不能用作气体发生装置,其原因是 , 若用D装置收集氧气,检验氧气是否收集满的方法是。(3)、实验室用高锰酸钾制氧气的反应属于反应(填基本反应类型),用E装置收集氧气时,应该时开始收集。(4)、实验室常用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷。已知甲烷极难溶于水,密度比空气小,若要制取并收集一瓶较纯净的甲烷,下列说法错误的是(填序号)。
(1)、编号为①的仪器名称为。(2)、不经改进的B装置不能用作气体发生装置,其原因是 , 若用D装置收集氧气,检验氧气是否收集满的方法是。(3)、实验室用高锰酸钾制氧气的反应属于反应(填基本反应类型),用E装置收集氧气时,应该时开始收集。(4)、实验室常用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷。已知甲烷极难溶于水,密度比空气小,若要制取并收集一瓶较纯净的甲烷,下列说法错误的是(填序号)。A应该选择A、E装置进行组合
B 加入药品前应该检查装置气密性,气密性良好才能加入药品
C 集气瓶瓶口有大气泡冒出时,先将导管移出水面,再熄灭酒精灯
D 生成的气体也可以采用向上排空气法收集
22. 某兴趣小组同学对实验室制备氧气的催化剂进行如下探究。(提出问题)二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
(1)、(查阅资料)研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用,分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:氧化铁
氧化铝
氧化铜
氧化镁
开始反应
420
515
305
490
剧烈反应
490
540
350
545
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的氧化物是。
(2)、(设计并完成实验)Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
(实验现象分析)将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同。Ⅲ中X的值应为 , 实验Ⅰ和Ⅲ比较可证明。
(3)、(结论)氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的文字表达式为。(4)、(实验反思)a.实验Ⅱ和Ⅲ对比的目的是。
b.在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量;
②测量。
23. 某实验小组利用如图所示装置测定空气中氧气的含量。
(查阅资料)白磷的着火点为40℃。
(提出问题)空气中氧气的体积分数是多少?
(实验准备)锥形瓶内空气体积为220mL,注射器内水的体积为50mL。
(实验过程)装入药品,连接好仪器,夹紧弹簧夹。先将锥形瓶下部放入80℃热水中白磷被引燃,然后将锥形瓶从热水中取出。待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹。
(1)、(现象分析)白磷被点燃时,锥形瓶内的实验现象是 , 整个实验过程中气球的变化是 , 气球在实验中的作用是。(2)、白磷燃烧反应的文字表达式是。(3)、打开弹簧夹,观察到注射器内的水自动向下喷出来,原因是 , 最终注射器中的水剩余约mL时停止下流。(4)、如果实验操作严格按照上述实验过程进行,测定的氧气的含量小于空气体积的1/5,原因有可能是(写出一条即可)。(5)、写出该实验装置的一个优点:。五、计算题
-
24. 适量补充钙元素可以预防幼儿及青少年出现佝偻病或发育不良,某补钙剂的说明书如图所示,请回答下列问题:
 (1)、碳酸钙的相对分子质量是;(2)、碳酸钙中钙元素的质量分数是;(3)、按照说明书用量服用,每天补充的钙元素的质量是;(4)、每片补钙剂中碳酸钙的质量分数是多少?(写出计算过程)
(1)、碳酸钙的相对分子质量是;(2)、碳酸钙中钙元素的质量分数是;(3)、按照说明书用量服用,每天补充的钙元素的质量是;(4)、每片补钙剂中碳酸钙的质量分数是多少?(写出计算过程)