湖北省武汉市青山区2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-01-20 类型:期中考试
一、单选题
-
1. 为有效阻断新型冠状病毒的传播,公众改变了许多生活习惯。下列做法主要涉及化学反应的是( )A、用医用酒精杀菌消毒 B、保持社交距离 C、改变握手拥抱礼节 D、出门配戴口罩2. 垃圾分类是新时尚。按照垃圾分类“四分法”,废弃的易拉罐和塑料瓶属于A、
 B、
B、 C、
C、 D、
D、 3. 下列实验操作正确的是( )A、加热液体
3. 下列实验操作正确的是( )A、加热液体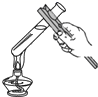 B、俯视读数
B、俯视读数  C、倾倒液体
C、倾倒液体  D、检查气密性
D、检查气密性 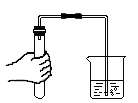 4. 下列说法正确的是()A、分子是化学变化中的最小粒子 B、不同元素的本质区别是电子数不同 C、原子核由电子和质子构成 D、墙内开花墙外香说明分子在不断运动5. 下列物质中,属于纯净物的是( )A、澄清的石灰水 B、清新的空气 C、臭氧 D、无色透明的雪碧饮料6. 下列物质中含氧分子的是( )A、空气 B、氯酸钾 C、过氧化氢 D、高锰酸钾7. 下列对实验现象的描述错误的是A、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 B、蜡烛在空气中燃烧,生成二氧化碳和水 C、硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体 D、氢气在空气中燃烧,产生淡蓝色火焰8. 下列关于水的叙述错误的是A、保持水化学性质的最小粒子是水分子 B、电解水得到氢气与氧气的质量比为1:8 C、江河湖泊的水经沉淀、过滤、消毒、杀菌后,可供人们生活使用 D、硬水是含有可溶性钙、镁化合物的水,软水是不含可溶性钙、镁化合物的水9. 在化学反应前后,下列各项中肯定没有变化的是
4. 下列说法正确的是()A、分子是化学变化中的最小粒子 B、不同元素的本质区别是电子数不同 C、原子核由电子和质子构成 D、墙内开花墙外香说明分子在不断运动5. 下列物质中,属于纯净物的是( )A、澄清的石灰水 B、清新的空气 C、臭氧 D、无色透明的雪碧饮料6. 下列物质中含氧分子的是( )A、空气 B、氯酸钾 C、过氧化氢 D、高锰酸钾7. 下列对实验现象的描述错误的是A、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 B、蜡烛在空气中燃烧,生成二氧化碳和水 C、硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体 D、氢气在空气中燃烧,产生淡蓝色火焰8. 下列关于水的叙述错误的是A、保持水化学性质的最小粒子是水分子 B、电解水得到氢气与氧气的质量比为1:8 C、江河湖泊的水经沉淀、过滤、消毒、杀菌后,可供人们生活使用 D、硬水是含有可溶性钙、镁化合物的水,软水是不含可溶性钙、镁化合物的水9. 在化学反应前后,下列各项中肯定没有变化的是原子数目 分子数目 元素种类 物质种类 原子种类 元素的化合价
A、 B、 C、 D、10. 化学概念在逻辑上存在如图所示几种关系。则对下列概念的说法中,正确的是( ) A、混合物与纯净物属于包含关系 B、物理性质与化学性质属于交叉关系 C、化学反应与分解反应属于并列关系 D、氧化反应与化合反应属于交叉关系11. 景德镇的高岭土(主要成分:Al2(Si2O5)(OH)n)是制造陶瓷器的优良原料。经分析,其中铝、氧元素质量比为3∶8,则( )A、n=1 B、n=2 C、n=3 D、n=412. 酒精检测仪检测酒驾的反应原理为: ,红色的 转变为绿色的化合物X,表明涉嫌酒驾。下列说法错误的是A、X化学式为 B、医疗上常用 的酒精水溶液消毒 C、 和 都属于氧化物 D、喝酒的人会散发酒味,说明微粒在不断运动13. 如图是与水有关的3个实验,关于该实验,有如下几种说法,其中正确的是( )
A、混合物与纯净物属于包含关系 B、物理性质与化学性质属于交叉关系 C、化学反应与分解反应属于并列关系 D、氧化反应与化合反应属于交叉关系11. 景德镇的高岭土(主要成分:Al2(Si2O5)(OH)n)是制造陶瓷器的优良原料。经分析,其中铝、氧元素质量比为3∶8,则( )A、n=1 B、n=2 C、n=3 D、n=412. 酒精检测仪检测酒驾的反应原理为: ,红色的 转变为绿色的化合物X,表明涉嫌酒驾。下列说法错误的是A、X化学式为 B、医疗上常用 的酒精水溶液消毒 C、 和 都属于氧化物 D、喝酒的人会散发酒味,说明微粒在不断运动13. 如图是与水有关的3个实验,关于该实验,有如下几种说法,其中正确的是( )
实验A和实验B都能验证质量守恒定律;
只有实验B能证明水是由氢元素和氧元素组成的;
实验A中烧瓶里加碎瓷片是为了防止出现暴沸;
用带火星的木条可检验实验B中试管a、b中产生的气体;
实验C中小卵石、石英沙的作用是过滤;
实验A和实验C得到的水都是纯净物。
A、 B、 C、 D、14. 如图所示,下列图象反应的对应关系错误的是(图中均为反应时间)( )A、 通电分解水
B、
通电分解水
B、 一定质量的镁在氧气中烧
C、
一定质量的镁在氧气中烧
C、 加热氯酸钾与二氧化锰的固体混合物
D、
加热氯酸钾与二氧化锰的固体混合物
D、 碳在盛有氧气的密闭集气瓶内燃烧
15. 制造口罩时,常用环氧乙烷(C2H4O)灭菌。常温下,环氧乙烷和乙烯(C2H4)按一定质量比混合的气体中碳元素的质量分数是72%。下列有关该混合气体的说法错误的是( )A、碳元素与氢元素的质量之比是6∶1 B、氢元素的质量分数是12% C、氧元素的质量分数是28% D、环氧乙烷与乙烯的分子数之比是1∶216. 常用燃烧法测定某些物质的组成,现取 某物质R在足量的氧气中完全燃烧,生成了 和 。对该物质R的组成和结构有下列推断:
碳在盛有氧气的密闭集气瓶内燃烧
15. 制造口罩时,常用环氧乙烷(C2H4O)灭菌。常温下,环氧乙烷和乙烯(C2H4)按一定质量比混合的气体中碳元素的质量分数是72%。下列有关该混合气体的说法错误的是( )A、碳元素与氢元素的质量之比是6∶1 B、氢元素的质量分数是12% C、氧元素的质量分数是28% D、环氧乙烷与乙烯的分子数之比是1∶216. 常用燃烧法测定某些物质的组成,现取 某物质R在足量的氧气中完全燃烧,生成了 和 。对该物质R的组成和结构有下列推断:一定含C、H元素
可能含氧元素
一定含氧元素
每个分子中H、O的原子个数比为6:1
每个分子中C、H的原子个数比为4:1
每个分子中C、H的原子个数比为1:3
该物质中C、O、H的元素质量比为12:3:8
其中正确的是
A、 B、 C、 D、二、填空题
-
17. 用化学用语或序号填空。(1)、3个氨分子;(2)、2个铝离子;(3)、锰酸钾中锰元素显 价;(4)、如图表示的微粒中,化学性质相似的原子是 填序号 。
 18. 从下列概念中选择正确的序号填入括号中
18. 从下列概念中选择正确的序号填入括号中A.物理变化 B.化学变化 C.物理性质 D.化学性质
(1)、0℃时水结成冰(2)、汽油可以燃烧(3)、块状胆矾变成粉末状胆矾(4)、酒精易挥发(5)、煤气燃烧(6)、鸡蛋发臭19. 空气和水是二种宝贵的自然资源。回答下列问题:(1)、目前计入空气污染指数的项目中除了可吸入颗粒物外,还包括 填序号 。①二氧化硫
②二氧化碳
③氮气
④氧气
(2)、鱼虾能在水中生存是因为在水中有易溶于水的氧气,这种说法 填“正确”或“不正确” 。(3)、夏天,盛放冰棒的杯子外壁上附有一层水珠,说明空气中有。(4)、自来水厂抽取河水进行净化的过程中,可加入除去水中异味。(5)、实验室中,一般用的方法除去水中不溶性杂质;水变成水蒸气的过程中,不发生变化的是 填字母序号 。A分子质量
B分子种类
C分子间隔
D分子大小
20. “微观 宏观 符号”是化学独特的表示物质及其变化的方法。 (1)、构成物质的粒子之间的关系如图1所示。
(1)、构成物质的粒子之间的关系如图1所示。甲是。
在氮气、金刚石、硫酸铜、铁、氧气、氯化钠六种物质中,由分子构成的物质是 , 由离子构成的物质是。
(2)、根据如图2所示的信息判断,元素Ⅰ的最外层电子数为 , 元素Ⅱ的相对原子质量是。(3)、相同质量的金属镁和铝,所含原子个数较多的是。21. 宏观、微观和符号之间建立联系是学习化学的重要思维方法。下图是某汽车尾气处理过程中发生的一个反应,请回答下列问题。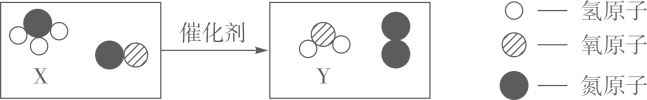 (1)、图示中的物质,属于单质的是(填化学式);(2)、该反应中,参加反应的X与生成的Y的分子个数最简整数比是;(3)、该反应前后,化合价发生了变化的元素是(填元素符号),该元素在图示相关物质中的最低化合价是。
(1)、图示中的物质,属于单质的是(填化学式);(2)、该反应中,参加反应的X与生成的Y的分子个数最简整数比是;(3)、该反应前后,化合价发生了变化的元素是(填元素符号),该元素在图示相关物质中的最低化合价是。三、综合题
-
22. 如图1、图2、图3所示的测定装置都可以用来测定空气成分,请回答问题:
 (1)、图1中发生反应的化学方程式为。(2)、图2装置可用于测定空气中氧气的含量,步骤为:①打开 、 ,从导管a向瓶A中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭 、 。此时进入量筒B中水的体积为200mL,观察到瓶A中的白磷燃烧。②待装置冷却一段时间后,打开 ,如果观察到 , 说明空气中氧气的体积分数约占五分之一。(3)、如图3所示装置也能测定空气中氧气的含量,实验过程中反复推拉两端注射器的活塞,其目的是 , 一段时间后,最终注射器内气体的体积约为mL。(4)、按图4所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂 其中辅助成分不干扰实验 ,利用铁锈蚀原理测定空气中氧气的体积分数 铁生锈消耗空气中的氧气和水蒸气 。
(1)、图1中发生反应的化学方程式为。(2)、图2装置可用于测定空气中氧气的含量,步骤为:①打开 、 ,从导管a向瓶A中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭 、 。此时进入量筒B中水的体积为200mL,观察到瓶A中的白磷燃烧。②待装置冷却一段时间后,打开 ,如果观察到 , 说明空气中氧气的体积分数约占五分之一。(3)、如图3所示装置也能测定空气中氧气的含量,实验过程中反复推拉两端注射器的活塞,其目的是 , 一段时间后,最终注射器内气体的体积约为mL。(4)、按图4所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂 其中辅助成分不干扰实验 ,利用铁锈蚀原理测定空气中氧气的体积分数 铁生锈消耗空气中的氧气和水蒸气 。①连接数字传感器,测得图1、图4中氧气的体积分数随时间变化的关系分别如图5、图6所示。依据图5、图6信息, 选填“图1”或“图4” 的测定方法更准确,猜想其原因是。
②与燃烧红磷法相比,用除氧剂测定空气中氧气含量有优点,也有缺点,缺点是。
23. 实验室常用高锰酸钾制取氧气,可能用到的装置如图所示。 (1)、本实验可选用的发生和收集装置为 填字母 。(2)、①写出高锰酸钾分解制氧气的化学方程式:。
(1)、本实验可选用的发生和收集装置为 填字母 。(2)、①写出高锰酸钾分解制氧气的化学方程式:。②上述反应的理论产氧率为 产氧率 ,结果精确到 。
取一定量的高锰酸钾固体,充分加热,发现实际产氧率高于上述数值,则可能的原因有 测定过程中产生的误差可忽略 。
(3)、实验室也可用双氧水制氧气。某同学为研究 粉末用量对双氧水分解速率的影响,做了以下实验:采用不同质量的 粉末做催化剂,每次均用 的双氧水 其他实验条件均相同 ,测定收集500mL氧气所用的时间,结果如表:序号
1
2
3
4
5
6
7
8
9
用量
所用时间
17
8
6
3
2
2
2
2
2
写出上述反应的化学方程式:。
该实验可得出的结论是。
24. 某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验: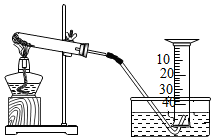
编号
KClO3质量/g
催化剂
催化剂质量/g
收集50mLO2所需时间/s
实验1
5
-
-
171
实验2
5
MnO2
0.5
49
实验3
5
Fe2O3
0.5
58
实验4
5
KCl
0.5
154
(1)、设置实验1的目的是(2)、表中所列3种催化剂的催化效果最佳的是(3)、写出KClO3分解的化学方程式:(4)、由实验1和实验4可知,KCl(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2 , 所需时间明显少于171s,解释原因:(5)、要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内25. 新型冠状病毒蔓延期间,为做好自我防护我们需要经常消毒,过氧乙酸是常用的消毒剂之一。其化学式为 ,请计算:(1)、过氧乙酸相对分子质量。(2)、过氧乙酸中各元素的质量比为。(3)、过氧乙酸中氧元素的质量为。