河南省新乡市2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-01-20 类型:期中考试
一、单选题
-
1. 下列各组物质的变化中,前者属于化学变化,后者属于物理变化的是( )A、冰雪融化,由空气制氧气 B、钢铁生锈,纸的燃烧 C、蜡烛燃烧,蜡烛融化 D、汽油挥发,食物腐烂2. 下列有关实验现象的描述错误的是( )A、氢气在空气中燃烧,发出淡蓝色火焰 B、硫在空气中燃烧发出淡蓝色火焰 C、细铁丝在空气中燃烧剧烈,火星四射生成黑色固体 D、红磷在空气中燃烧产生大量白烟3. 下列物质属于纯净物的是( )A、冰水共存物 B、医用生理盐水 C、加热高锰酸钾制氧气后的剩余物 D、清洁的空气4. 下列实验操作正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、 往试管中加入锌粒
C、
往试管中加入锌粒
C、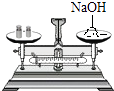 称量氢氧化钠
D、
称量氢氧化钠
D、 收集氧气
5. 下列各选项中,解释与事实不吻合的是( )
收集氧气
5. 下列各选项中,解释与事实不吻合的是( )选项
事实
解释
A
春天,远远的闻到花的香味
分子在不停地运动
B
加压条件下,空气液化后体积变小
加压条件下,分子的体积都变小
C
水在通电条件下,可分解为氧气和氢气
化学反应中分子是可分的
D
水和双氧水组成元素相同,但化学性质有很大的差异
分子的构成不同
A、A B、B C、C D、D6. 如图是高温下某反应的微观过程.下列说法中正确的是() A、该反应属于分解反应 B、该反应中元素的化合价没有变化 C、图中的两种化合物都属于氧化物 D、该反应所得生成物的质量比为1:17. 下列做法符合操作规范的是( )A、用排水法制取氧气结束时,应先熄灭酒精灯,然后把导管移出水面。 B、为了节约药品,可将实验用剩的药品倒回原试剂瓶中。 C、给试管里的液体加热时,液体量可占试管容积的。 D、给试管里的固体加热时,试管口应略向下倾斜。8. 下列各组物质中,都由分子构成的一组是( )A、金和金刚石 B、水和氨气 C、汞和氯化钠 D、干冰和硫酸铜9. 将16克高锰酸钾在试管里加热,过一段时间后,撤去酒精灯,称的剩余固体是14.4克,通过计算确定剩余固体的成分是( )A、高锰酸钾 B、高锰酸钾、锰酸钾、二氧化锰 C、锰酸钾、二氧化锰 D、锰酸钾10. 二甲醚(C2H6O)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。有关说法正确的是( )
A、该反应属于分解反应 B、该反应中元素的化合价没有变化 C、图中的两种化合物都属于氧化物 D、该反应所得生成物的质量比为1:17. 下列做法符合操作规范的是( )A、用排水法制取氧气结束时,应先熄灭酒精灯,然后把导管移出水面。 B、为了节约药品,可将实验用剩的药品倒回原试剂瓶中。 C、给试管里的液体加热时,液体量可占试管容积的。 D、给试管里的固体加热时,试管口应略向下倾斜。8. 下列各组物质中,都由分子构成的一组是( )A、金和金刚石 B、水和氨气 C、汞和氯化钠 D、干冰和硫酸铜9. 将16克高锰酸钾在试管里加热,过一段时间后,撤去酒精灯,称的剩余固体是14.4克,通过计算确定剩余固体的成分是( )A、高锰酸钾 B、高锰酸钾、锰酸钾、二氧化锰 C、锰酸钾、二氧化锰 D、锰酸钾10. 二甲醚(C2H6O)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。有关说法正确的是( ) A、二甲醚的相对分子质量为48 B、二甲醚属于氧化物 C、二甲醚由2个碳原子、6个氢原子和1个氧原子构成 D、二甲醚中碳元素与氢元素的质量比为4:111. 硝酸铜受热分解会产生一种污染空气的有毒气体,该气体可能是( )A、N2 B、NO2 C、NH3 D、SO212. 元素周期表中钠元素的信息如图所示,对图中信息理解错误的是 ( )
A、二甲醚的相对分子质量为48 B、二甲醚属于氧化物 C、二甲醚由2个碳原子、6个氢原子和1个氧原子构成 D、二甲醚中碳元素与氢元素的质量比为4:111. 硝酸铜受热分解会产生一种污染空气的有毒气体,该气体可能是( )A、N2 B、NO2 C、NH3 D、SO212. 元素周期表中钠元素的信息如图所示,对图中信息理解错误的是 ( ) A、质子数为11 B、核外电子数为22.99 C、元素符号为Na D、元素名称为钠13.
A、质子数为11 B、核外电子数为22.99 C、元素符号为Na D、元素名称为钠13.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
 A、固体中氧元素的质量 B、生成O2的质量 C、固体中MnO2的质量 D、固体中钾元素的质量14. 某工厂制取漂白液的化学原理为:Cl2+2NaOH=NaCl+NaClO+H2O,在该反应中,氯元素没有呈现出的化合价是( )A、+2 B、+1 C、0 D、﹣1
A、固体中氧元素的质量 B、生成O2的质量 C、固体中MnO2的质量 D、固体中钾元素的质量14. 某工厂制取漂白液的化学原理为:Cl2+2NaOH=NaCl+NaClO+H2O,在该反应中,氯元素没有呈现出的化合价是( )A、+2 B、+1 C、0 D、﹣1二、填空题
-
15. 空气中体积分数最大的物质是(用化学式表示),除去水中不溶性杂质的方法是。16. 配制农药波尔多液所用硫酸铜的构成粒子是(填化学符号)。葡萄糖在人体组织中缓慢氧化放出热量,这是人类生命活动所需要的重要来源之一、葡萄糖的化学式为C6H12O6 , 从这个化学式所表示的意义中你能总结出哪条信息:。17. 如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空:
 (1)、A,B,C,D四种粒子中,属于同种元素的是(填序号),C粒子的符号为。硒的相对原子质量为。(2)、由C元素和B元素形成的化合物的化学式为。18. 研究人员利用金属钉催化剂将从空中捕获的二氧化碳转化为甲醇。该反应的微观示意图如下:
(1)、A,B,C,D四种粒子中,属于同种元素的是(填序号),C粒子的符号为。硒的相对原子质量为。(2)、由C元素和B元素形成的化合物的化学式为。18. 研究人员利用金属钉催化剂将从空中捕获的二氧化碳转化为甲醇。该反应的微观示意图如下: (1)、该反应中单质与甲醇的质量比为。(2)、取4.8 g的甲醇(CH3OH)和6.4 g O2在密闭容器中点燃,恰好完全反应,生成4.4 g CO2 , 5.4 g H2O和物质CO请写出该反应的化学方程式。19. 在一密闭容器中,有X、O2、CO2、H2O四种物质,在一定条件下发生某种反应,反应一段时间后,测得反应前后各物质的质量如下表。
(1)、该反应中单质与甲醇的质量比为。(2)、取4.8 g的甲醇(CH3OH)和6.4 g O2在密闭容器中点燃,恰好完全反应,生成4.4 g CO2 , 5.4 g H2O和物质CO请写出该反应的化学方程式。19. 在一密闭容器中,有X、O2、CO2、H2O四种物质,在一定条件下发生某种反应,反应一段时间后,测得反应前后各物质的质量如下表。物质
X
O2
CO2
H2O
反应前的质量/g
19
34
6
2
反应后的质量/g
11
待测
28
20
表中的待测值为 , X中一定含有元素,反应中CO2和H2O的质量比为。
20. 下面是某化学反应前后的微观模拟图(反应条件省略),请根据图示回答: (1)、该化学反应中,参加反应的“
(1)、该化学反应中,参加反应的“ ”和“
”和“  ”与反应后生成的“
”与反应后生成的“  ”各粒子间的个数比为; (2)、如图中反应后容器内的物质属于(填“纯净物”或“混合物”);结合上图,从原子、分子的角度分析,在化学反应过程中不变。
”各粒子间的个数比为; (2)、如图中反应后容器内的物质属于(填“纯净物”或“混合物”);结合上图,从原子、分子的角度分析,在化学反应过程中不变。三、综合题
-
21. 某同学按右图装置对质量守恒定律进行实验探究,结果观察到反应后天平不平衡,由此得出这个化学反应不遵守质量守恒定律的结论。这个结论是否正确?为什么?
 22. 用微粒的观点解释下列事实(1)、温度计内汞柱液面上升的原因。(2)、固体碘和碘蒸汽都能使淀粉变蓝。23. 用质量守恒定律解释:铁丝在氧气中生成物的质量比参加铁丝的质量大。
22. 用微粒的观点解释下列事实(1)、温度计内汞柱液面上升的原因。(2)、固体碘和碘蒸汽都能使淀粉变蓝。23. 用质量守恒定律解释:铁丝在氧气中生成物的质量比参加铁丝的质量大。四、实验题
-
24. 根据下图装置回答下列问题。
 (1)、实验室里用装置A可以制取某种氧气,写出制取氧气的化学反应方程式。(2)、若用装置C收集氧气,应从(填“a”或“b”)端进气。检验用装置C收集满氧气的方法是什么?(3)、写出实验室选择B装置制取气体的依据?(4)、把装置B的长颈漏斗换成分液漏斗有什么优点?25.(1)、某同学利用如图微型装置进行实验探究。请回答:
(1)、实验室里用装置A可以制取某种氧气,写出制取氧气的化学反应方程式。(2)、若用装置C收集氧气,应从(填“a”或“b”)端进气。检验用装置C收集满氧气的方法是什么?(3)、写出实验室选择B装置制取气体的依据?(4)、把装置B的长颈漏斗换成分液漏斗有什么优点?25.(1)、某同学利用如图微型装置进行实验探究。请回答:
单球管中发生反应的化学方程式是;制取的气体收集在集气管中,将红磷在酒精灯上加热后迅速放进集气管,塞紧塞子,观察到的现象是 , 冷却后出现的现象。反应的化学方程式为。
(2)、制取氧气的方法很多,可以用过氧化钠(Na2O2)与水来制取,除了生成氧气外还有一种物质氢氧化钠,写出化学方程式。收集氧气可以排水法和向上排空气法收集说明氧气具有、的性质。五、计算题
-
26. 将30.9 g 氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却、称量,可以得到21.3 g 固体物质。请计算原固体混合物中氯酸钾的质量。