江苏省扬州市高邮市2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-01-18 类型:期中考试
一、单选题
-
1. 今年世界环境日的主题是“关爱自然, 刻不容缓”。 下列做法符合这一主题的是( )A、焚烧垃圾,净化环境 B、垃圾分类,保护环境 C、禁用农药,保护水源 D、露天烧烤,享受生活2. 下列过程中,发生了化学变化的是( )A、干冰变成CO2气体 B、从含SiO2的沙子中提炼高纯Si C、海水晒盐 D、从潮湿空气中分离出水3. 下列物质由分子构成的是( )A、金刚石 B、氯化钠 C、干冰 D、金属镁4. 下列物质中,含有氧分子的是( )A、空气 B、CO2 C、H2O2 D、MnO25. 空气是一种宝贵的自然资源,下列说法中错误的是( )A、工业上常利用氮气与氧气的沸点不同,分离液态空气获得氧气 B、少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 C、按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1% D、空气是一种组成相对稳定的混合物,各成分能保持其自身的化学性质6. 表示“禁止燃放烟花爆竹”的标志是( )A、
 B、
B、 C、
C、 D、
D、 7. 下列有关化学学科观念的说法错误的是( )A、结构观:构成水和过氧化氢的分子结构不同,化学性质也不同 B、元素观:金刚石和石墨均由碳元素组成 C、守恒观:化学反应前后,元素的种类不变 D、微粒观:水是由两个氢原子和一个氧原子构成的8. 利用蒸发、冷凝的方法可以从海水中获取淡水,下列叙述正确的是( )A、蒸发时,水分子的运动速率加快 B、蒸发时,海水的质量变大 C、冷凝时,水分子之间的间隔不变 D、冷凝时,淡水的体积不变9. 下列观点中你认为错误的是( )A、物质本身并无优劣之分,但应用的方法和目的却存在差别 B、物质的性质与用途之间存在着密切联系 C、随着仿真实验室和数字处理技术的发展,研究的结论可不必通过实验来证明 D、化学变化中所说的“新物质”就是在组成或结构上与变化前不同的物质10. 世卫组织(WHO)发表声明称,地塞米松(C22H29FO3)可挽救新冠肺炎重症患者生命。下列关于地塞米松的说法正确的是( )A、地塞米松属于氧化物 B、地塞米松由 4 种元素组成 C、地塞米松中碳、氧元素的质量比为 22:3 D、地塞米松中氢元素的质量分数最大11. 如图为某反应的微观示意图,“
7. 下列有关化学学科观念的说法错误的是( )A、结构观:构成水和过氧化氢的分子结构不同,化学性质也不同 B、元素观:金刚石和石墨均由碳元素组成 C、守恒观:化学反应前后,元素的种类不变 D、微粒观:水是由两个氢原子和一个氧原子构成的8. 利用蒸发、冷凝的方法可以从海水中获取淡水,下列叙述正确的是( )A、蒸发时,水分子的运动速率加快 B、蒸发时,海水的质量变大 C、冷凝时,水分子之间的间隔不变 D、冷凝时,淡水的体积不变9. 下列观点中你认为错误的是( )A、物质本身并无优劣之分,但应用的方法和目的却存在差别 B、物质的性质与用途之间存在着密切联系 C、随着仿真实验室和数字处理技术的发展,研究的结论可不必通过实验来证明 D、化学变化中所说的“新物质”就是在组成或结构上与变化前不同的物质10. 世卫组织(WHO)发表声明称,地塞米松(C22H29FO3)可挽救新冠肺炎重症患者生命。下列关于地塞米松的说法正确的是( )A、地塞米松属于氧化物 B、地塞米松由 4 种元素组成 C、地塞米松中碳、氧元素的质量比为 22:3 D、地塞米松中氢元素的质量分数最大11. 如图为某反应的微观示意图,“ ”、“
”、“  ”各表示一种原子,下列说法错误的是( )
”各表示一种原子,下列说法错误的是( )  A、反应物是两种单质 B、反应物有剩余 C、该反应为化合反应 D、该反应生成了多种产物12. 原子是构成物质的一种微粒,下列关于原子的说法正确的是( )A、原子的质量主要集中在原子核上 B、相同的原子无法构成不同的分子 C、温度计内汞柱液面上升说明汞原子体积变大 D、原子呈电中性是因为原子中质子数与中子数相等13. 安全高于一切,下列做法正确的是( )A、电线老化着火,立即用水浇灭 B、夜晚天然气泄露,立即开灯查找原因 C、煤炉上放一壶水防止CO中毒 D、不小心碰倒酒精灯,洒出的酒精在桌上燃烧起来,应立即用湿抹布扑灭14. 下列说法中错误的是( )A、二氧化碳与水反应不一定生成碳酸 B、带正电的微粒不一定是阳离子 C、由同种元素组成的纯净物不一定是单质 D、灭火时不一定要将温度降到着火点以下15. 节能减排中“减排”的关键是减少 CO2 的排放,而“减排”的重要手段是合理利用 CO2。科学家利用 CO2为原料制取炭黑的流程如图。下列说法错误的是( )
A、反应物是两种单质 B、反应物有剩余 C、该反应为化合反应 D、该反应生成了多种产物12. 原子是构成物质的一种微粒,下列关于原子的说法正确的是( )A、原子的质量主要集中在原子核上 B、相同的原子无法构成不同的分子 C、温度计内汞柱液面上升说明汞原子体积变大 D、原子呈电中性是因为原子中质子数与中子数相等13. 安全高于一切,下列做法正确的是( )A、电线老化着火,立即用水浇灭 B、夜晚天然气泄露,立即开灯查找原因 C、煤炉上放一壶水防止CO中毒 D、不小心碰倒酒精灯,洒出的酒精在桌上燃烧起来,应立即用湿抹布扑灭14. 下列说法中错误的是( )A、二氧化碳与水反应不一定生成碳酸 B、带正电的微粒不一定是阳离子 C、由同种元素组成的纯净物不一定是单质 D、灭火时不一定要将温度降到着火点以下15. 节能减排中“减排”的关键是减少 CO2 的排放,而“减排”的重要手段是合理利用 CO2。科学家利用 CO2为原料制取炭黑的流程如图。下列说法错误的是( ) A、过程 1 和过程 2 的变化都属于分解反应 B、过程 2 的变化中太阳能转化为化学能 C、此流程中有炭黑生成,还有氧气生成 D、获取炭黑还需要解决炭黑和 Fe3O4 的分离16. 下列加热高锰酸钾制取氧气的部分操作示意图中正确的是( )A、
A、过程 1 和过程 2 的变化都属于分解反应 B、过程 2 的变化中太阳能转化为化学能 C、此流程中有炭黑生成,还有氧气生成 D、获取炭黑还需要解决炭黑和 Fe3O4 的分离16. 下列加热高锰酸钾制取氧气的部分操作示意图中正确的是( )A、 检查气密性,先将导管放入水中
B、
检查气密性,先将导管放入水中
B、 一点燃酒精灯,立即收集气体
C、
一点燃酒精灯,立即收集气体
C、 集满气体后,按图示移出集气瓶
D、
集满气体后,按图示移出集气瓶
D、 实验结束,先熄灭酒精灯
17. 下列实验方案设计错误的是( )A、观察颜色区分铁片和铜片 B、闻气味区分氧气和二氧化硫气体 C、尝味道区分厨房中的蔗糖和食盐 D、燃着的木条区分氮气和二氧化碳18. 金属钴(Co)的氧化物有多种,将 9.3g Co(OH)2 在空气中加热至 290℃时完全分解,得到一种钴的氧化物和水,测得该氧化物的质量为 8.3g,该氧化物的化学式是( )A、CoO B、CoO3 C、Co2O3 D、Co3O4
实验结束,先熄灭酒精灯
17. 下列实验方案设计错误的是( )A、观察颜色区分铁片和铜片 B、闻气味区分氧气和二氧化硫气体 C、尝味道区分厨房中的蔗糖和食盐 D、燃着的木条区分氮气和二氧化碳18. 金属钴(Co)的氧化物有多种,将 9.3g Co(OH)2 在空气中加热至 290℃时完全分解,得到一种钴的氧化物和水,测得该氧化物的质量为 8.3g,该氧化物的化学式是( )A、CoO B、CoO3 C、Co2O3 D、Co3O4二、多选题
-
19. 物质的性质决定物质的用途。下列对应关系错误的是( )A、石墨具有导电性,可用于生产铅笔芯 B、酒精具有可燃性,可作燃料 C、氮气常温下无色无味,可用作粮食、瓜果的保护气 D、镁燃烧能产生耀眼的强光,可用于制作照明弹20. 利用如图装置验证了空气中氧气的含量。下列叙述错误的是( )
 A、实验前需检查装置气密性 B、读数时需要将导管从量筒中取出 C、最终量筒中液面约降至 40mL 刻度线处 D、若试管未完全冷却就读数,则所测氧气含量偏小
A、实验前需检查装置气密性 B、读数时需要将导管从量筒中取出 C、最终量筒中液面约降至 40mL 刻度线处 D、若试管未完全冷却就读数,则所测氧气含量偏小三、综合题
-
21. 某品牌奶粉标签如图,请回答下列问题。
 (1)、该奶粉是 (填“纯净物”或“混合物”)。(2)、硫酸亚铁的化学式为 , 其中铁元素的质量分 数为 (计算结果保留小数点后一位),亚铁离 子的符号为 。(3)、结合图 2 铁元素在元素周期表中的信息,铁的原子序数为 , 相对原子质量为。(4)、奶粉中碳酸钙可适量补钙,标出碳酸钙中碳元素的化合价 , 钙 (填“是”或“不是”)人体 所需的微量元素,儿童缺钙易患有病。(5)、计算:该奶粉中钙元素的质量是g,含钙元素的质量分数为;若该奶粉中仅碳酸钙含钙元素, 则其中碳酸钙的质量分数为。(6)、标签中(填符号)元素的单质可用作烟幕弹。22. 水是宝贵的自然资源。(1)、水的组成
(1)、该奶粉是 (填“纯净物”或“混合物”)。(2)、硫酸亚铁的化学式为 , 其中铁元素的质量分 数为 (计算结果保留小数点后一位),亚铁离 子的符号为 。(3)、结合图 2 铁元素在元素周期表中的信息,铁的原子序数为 , 相对原子质量为。(4)、奶粉中碳酸钙可适量补钙,标出碳酸钙中碳元素的化合价 , 钙 (填“是”或“不是”)人体 所需的微量元素,儿童缺钙易患有病。(5)、计算:该奶粉中钙元素的质量是g,含钙元素的质量分数为;若该奶粉中仅碳酸钙含钙元素, 则其中碳酸钙的质量分数为。(6)、标签中(填符号)元素的单质可用作烟幕弹。22. 水是宝贵的自然资源。(1)、水的组成“电解法”证明水的组成(装置如图 1 所示,电极不与水及生成的气体反应)
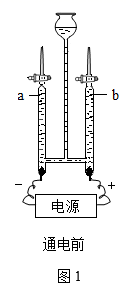
①实验时需向水中加入适量稀 H2SO4或 NaOH,其目的是。
②通电时发生反应的符号表达式为。
③a、b 两管产生气体的体积比是。
④下列关于电解水的说法中正确的是(填字母)。
a实验后,a 管产生的气体能燃烧
b该实验中水分子本身不变,改变的是水分子间的间隙
c该反应属于分解反应
d反应后氢、氧元素的化合价均发生改变
(2)、水的净化①自来水厂净水的过程中不包括的净水方法是。
a沉降 b吸附 c蒸馏 d消毒
②河水中的难溶性杂质,可通过过滤的方法除去。用下图装置对河水水样进行过滤,下列关于过滤的说法中正确的有(填字母)。
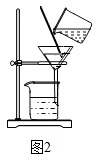
a实验中用玻璃棒在漏斗中轻轻搅动以加快过滤速度
b滤纸边缘需低于漏斗边缘
c漏斗下端尖嘴需紧靠烧杯内壁
d若滤纸与漏斗间留有气泡,则会使过滤所得的液体浑浊
e利用过滤操作,可以将河水中的色素分离出来
③若要检验过滤后的液体是否为硬水,可以取样于试管中加入搅拌后,观察现象。家庭中常用方法将硬水转化为软水,该方法会使家中水壶中产生水垢,家庭中可用(填一种调味品名称)除去水壶内壁上的水垢。
(3)、水的保护①天然水污染的来源有(请任写一种)。
②保护水资源是我们全人类义不容辞的责任。作为一名中学生,我们能为保护水资源作出的努力有(请任写一种具体做法)。
(4)、水的用途水在生产、生活、科研中存在有广泛的用途。 请写出水在实验中的一种用途(请任写一种)。23. 下图为实验室制取气体的常见装置,请据图回答有关问题: (1)、写出序号为①、②的仪器名称:①;②;(2)、实验室常选用选用 A 装置,加热氯酸钾制备氧气,请写出该反应的符号表达式;
(1)、写出序号为①、②的仪器名称:①;②;(2)、实验室常选用选用 A 装置,加热氯酸钾制备氧气,请写出该反应的符号表达式;①实验室可选用 D 装置收集 O2的原因是 , 氧气收集满的现象是;
②集满 O2的集气瓶应正放在实验桌上,原因是;
(3)、实验室制取二氧化碳的符号表达式为 ;①若选用 E 装置收集 CO2 , 则气体从端通入(填“a”或“b”),验满的操作是;
②若用该装置检验 CO2 , 瓶中需装入(填名称),气体从端通入(填“a”或“b”), 如果含有 CO2 , 则发生反应的符号表达式为。
(4)、实验室可用锌粒与稀硫酸在常温下反应制取氢气,若需控制液体药品的滴加速度以获得平稳的氢气流,则图中最合适的发生装置是;氢气具有可燃性,是一种非常理想的绿色能源,为防止氢气在点燃时发生爆炸,点燃前一定要进行的操作。24. 实验室常用双氧水和二氧化锰为原料制备氧气。为探究影响双氧水分解速率的因素,某研究小组设计了如下对比实验,并记录了收集一集气瓶(125mL)氧气所需时间。实验序号
双氧水溶度
双氧水体积(mL)
温度(℃)
MnO2 用量(g)
收集时间(s)
①
5%
20
20
0.2
11
②
30%
20
20
0.2
2
③
30%
20
40
0
148
④
30%
20
90
0
82
(1)、实验室用双氧水和二氧化锰为原料制备氧气的符号表达式为。(2)、通过实验①和②对比,可以得出的结论是。(3)、通过实验③和(填序号)对比,可知相同条件下,温度越高,双氧水分解速率越快。(4)、上述最适合用于实验室制取氧气的是实验(填序号),理由是。(5)、小明认为要想探究“二氧化锰的使用与否对双氧水分解速率的影响”,还需在上表实验①的基础上再增加一组对比实验,小华认为无需增加,将实验②、④进行对比也可得出结论。你的观点是 (填“需要”或“不需要”)增加,理由是。
25. 燃烧是人类利用的较古老的化学反应之一。兴趣小组同学对燃烧展开系列探究。 (1)、探究一、燃烧的发生
(1)、探究一、燃烧的发生兴趣小组同学按图 1 所示装置进行实验。待蜡烛燃烧熄灭后,向上抽动燃烧匙,使白磷露出水面,白磷立即燃烧。写出白磷燃烧的符号表达式 , 白磷露出水面后才燃烧,请分析原因。
(2)、已知:白磷的着火点约为 40℃,熔点约为 44℃,实验条件下的液态白磷密度大于水的 密度且难以透过滤纸,尝试分析:燃烧匙底部打孔并垫上滤纸的原因 。(3)、反思:蜡烛燃烧熄灭后的密闭钟罩内,白磷仍能燃烧,从“物质燃烧所需氧气的最低浓度” 的角度可得出的结论是。(4)、探究二、火灾的逃生知识回顾:图 2 所示实验中,观察到烧杯内低处蜡烛先熄灭,则 CO2具有的性质是。
(5)、按图 3 装置模拟建筑火灾现场,在封盖容器底部放置 2 根高低不同的蜡烛,在烛芯附近 放置 O2传感器(见 a1、a2)和 CO2 传感器(见 b1、b2)。点燃蜡烛后迅速封盖,采集相关 数据,实验结果如图 4、图 5 所示。
①由图 4 可知:蜡烛熄灭时容器各处 O2含量均未降至 0,由此你对“燃烧”的新认识是。
②由图 5 可知:温度较高时,高处 CO2的浓度较大,其主要原因是。因此,建筑火灾中, 下列逃生方法较合理的是。
a匍匐前进
b直立行走