安徽省合肥市庐阳区合肥市第四十二中2019-2020学年九年级上学期化学期中考试试卷
试卷更新日期:2021-01-18 类型:期中考试
一、单选题
-
1. 以下对自然资源利用的过程中只发生物理变化的是( )A、
 铝土矿炼铝
B、
铝土矿炼铝
B、 天然气燃烧
C、
天然气燃烧
C、 木材制桌椅
D、
木材制桌椅
D、 海水提取镁
2. 2019年“世界环境日”中国确定的主题是“蓝天保卫战,我是行动者”。下列做法与之相违背的是()A、秸秆露天焚烧 B、废气达标排放 C、工地洒水除尘 D、禁放烟花爆竹3. 硒被誉为“抗癌大王”。根据右图提供的硒的有关信息,下列说法中,正确的是( )
海水提取镁
2. 2019年“世界环境日”中国确定的主题是“蓝天保卫战,我是行动者”。下列做法与之相违背的是()A、秸秆露天焚烧 B、废气达标排放 C、工地洒水除尘 D、禁放烟花爆竹3. 硒被誉为“抗癌大王”。根据右图提供的硒的有关信息,下列说法中,正确的是( )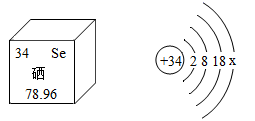 A、硒属于金属元素 B、硒的原子序数是34 C、硒的原子结构示意图中x=4 D、硒的相对原子质量是78.96 g4. 如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )
A、硒属于金属元素 B、硒的原子序数是34 C、硒的原子结构示意图中x=4 D、硒的相对原子质量是78.96 g4. 如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( ) A、S、P在氧气中燃烧均会产生大量白烟 B、Ⅰ、Ⅱ两类反应均体现了氧气的可燃性 C、Fe在Ⅰ、Ⅱ两类反应中的产物不相同 D、Ⅰ类反应放出热量,Ⅱ类反应吸收热量5. 下列实验操作正确的是( )A、
A、S、P在氧气中燃烧均会产生大量白烟 B、Ⅰ、Ⅱ两类反应均体现了氧气的可燃性 C、Fe在Ⅰ、Ⅱ两类反应中的产物不相同 D、Ⅰ类反应放出热量,Ⅱ类反应吸收热量5. 下列实验操作正确的是( )A、 过滤
B、
过滤
B、 氢气验纯
C、
氢气验纯
C、 收集氧气
D、
收集氧气
D、 塞紧橡皮塞
6. 科学家发现,利用催化剂可有效消除室内装修材料释放的有害气体甲醛(CH2O),其反应的微观示意图如下。下列说法中,错误的是( )
塞紧橡皮塞
6. 科学家发现,利用催化剂可有效消除室内装修材料释放的有害气体甲醛(CH2O),其反应的微观示意图如下。下列说法中,错误的是( ) A、乙的化学式是O2 B、该反应属于分解反应 C、通常状况下,丁是一种液态物质 D、可解决甲醛带来的室内空气污染问题7. 分类是研究物质的常用方法.下图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
A、乙的化学式是O2 B、该反应属于分解反应 C、通常状况下,丁是一种液态物质 D、可解决甲醛带来的室内空气污染问题7. 分类是研究物质的常用方法.下图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( ) A、红磷 B、洁净的空气 C、氯酸钾 D、水8. 下列由事实得出的结论正确的是( )
A、红磷 B、洁净的空气 C、氯酸钾 D、水8. 下列由事实得出的结论正确的是( )编号
事实
结论
A
某气体使燃着的木条熄灭
该气体一定是氮气
B
干冰升华为气体
二氧化碳分子变大
C
稀有气体的性质稳定
其原子已达到相对稳定结构
D
某物质组成中只含有一种元素
该物质一定是单质
A、A B、B C、C D、D9. “中水”是城市污水处理设施深度净化处理后的水,因为水质介于自来水(上水)与排入管道的污水(下水)之间,故名为“中水”。下列有关“中水”的说法中,错误的是( )A、“中水”不能作为引用水泥 B、将生活污水处理成“中水”的过成要用到过滤、吸附等方法 C、“中水”中水分子与蒸馏水中水分子的构成不同 D、利用“中水”有利于节约水资源10. 如图为实验室用等质量的高锰酸钾和氯酸钾(另加少量的二氧化锰),分别制取氧气的数据分析示意图.下列依据图示信息所得出的分析错误的是( ) A、同时开始加热,先收集到氧气的是高锰酸钾 B、制取较多量的氧气是氯酸钾,是因为加入了少量的二氧化锰 C、反应时间较短的是高锰酸钾 D、加热氯酸钾制氧气可以加入少量的高锰酸钾来加快反应速度
A、同时开始加热,先收集到氧气的是高锰酸钾 B、制取较多量的氧气是氯酸钾,是因为加入了少量的二氧化锰 C、反应时间较短的是高锰酸钾 D、加热氯酸钾制氧气可以加入少量的高锰酸钾来加快反应速度二、填空题
-
11. 小凯参观了科技馆,其中“物质之妙”展区蕴含着丰富的化学知识。
 (1)、A展示了水的微观结构模型,保持其化学性质的基本粒子是;(2)、B介绍了14C测年法,14C是质子数为6,中子数为8的碳原子,该原子中核外电子数为;(3)、C介绍了化学家门捷列夫及元素周期表,如图所示是元素周期表中某一周期元素的原子结构示意图:
(1)、A展示了水的微观结构模型,保持其化学性质的基本粒子是;(2)、B介绍了14C测年法,14C是质子数为6,中子数为8的碳原子,该原子中核外电子数为;(3)、C介绍了化学家门捷列夫及元素周期表,如图所示是元素周期表中某一周期元素的原子结构示意图:
①表中氟原子的原子结构示意图中x为 , 上述元素在周期表中为于同一周期的原因是 , ②镁原子的结构示意图为
 ,上图中与其化学性质相似的元素是。12. 学习第二单元氧气,同学们进行如下探究:
,上图中与其化学性质相似的元素是。12. 学习第二单元氧气,同学们进行如下探究: (1)、氧气是人类无法离开的物质,在不同的生活、生产环境中对氧气浓度的要求不同,人类常采用不同的方法制取氧气。
(1)、氧气是人类无法离开的物质,在不同的生活、生产环境中对氧气浓度的要求不同,人类常采用不同的方法制取氧气。①工业上一般采用甲路径分离净化后的液态空气制取氧气,在生产中应控制温度的范围是;(已知在1.01×105Pa时,O2的沸点为-183℃,N2的沸点为-196℃)
②食盐水常通过乙、丙、丁三种路径来制取氧气,写出装置B中a仪器的名称;若用路径戊,应选择的发生装置是(填序号);若用路径丙发生反应的文字表达式是;
(2)、许多物质在氧气中能剧烈燃烧。同学们对铁丝在氧气中燃烧的实验进行了改进,用适量10%的过氧化氢溶液和二氧化锰代替原实验集气瓶中的水(如图所示),其优点除了能使实验简便且保证安全,还有;铁燃烧实验现象是;交流反思:控制反应条件可以促进或抑制化学反应,请写出促进可燃物燃烧的方法(写出一种);
13. 下表中的内容摘自安徽省水环境监测中心发布的“安徽省地表水资源质量状况”:编号
河段
水质类别
主要污染指标
质量状况
①
长江芜湖弋矶山河段
Ⅱ
良好
②
裕溪河裕溪闸段
Ⅳ
汞
一般
③
南淝河合肥新港河段
劣Ⅴ
总磷、氨氮
很差
(1)、主要污染指标中,涉及的污染元素有N、等(填元素符号);(2)、属于重金属污染的河段是(填编号)(3)、水中的蓝藻等生物生长繁殖过快能导致水质恶化,上述河段中最可能出现蓝藻等生物大量繁殖的是。(填编号)(4)、“藻/水在线分离磁捕平台”能将水体中的藻泥送压滤机压成“藻饼”,并流出清澈的水。这一过程类似的化学操作是。另外,五氯酚钠也是杀菌灭藻剂,如表信息,五氯酚钠保存时应注意。 (5)、怎样判断各河段中的水是硬水还是软水?14. 美国普度大学研发出一种利用金属铝和金属镓的混合物纸杯氢气的新工艺,流程如图所示:
(5)、怎样判断各河段中的水是硬水还是软水?14. 美国普度大学研发出一种利用金属铝和金属镓的混合物纸杯氢气的新工艺,流程如图所示: (1)、氢气被称为“绿色能源”的主要原因是;(2)、步骤①中发生反应的文字表达式是(不填条件) , 其中镓的作用是;(3)、上述过程中,涉及到的非金属单质有(写出符号);(4)、Mg17Al12是一种储氢材料。该合金完全吸氢后得到MgH2和Al,则“储氢过程”属于(填“物理”或“化学”)变化。该合金通常选择真空熔炼而非空气中熔炼的原因是。
(1)、氢气被称为“绿色能源”的主要原因是;(2)、步骤①中发生反应的文字表达式是(不填条件) , 其中镓的作用是;(3)、上述过程中,涉及到的非金属单质有(写出符号);(4)、Mg17Al12是一种储氢材料。该合金完全吸氢后得到MgH2和Al,则“储氢过程”属于(填“物理”或“化学”)变化。该合金通常选择真空熔炼而非空气中熔炼的原因是。三、科学探究题
-
15. 化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究:
(提出问题)呼出气体中有哪些主要成分,它们的含量是多少?
(假设与猜想)呼出气体中N2、O2、CO2、水蒸气等
(查阅资料)氢氧化钠(NaOH)溶液可以充分吸收CO2
(实验1)验证含有水蒸气
(1)、操作方法: , 根据实验现象判断呼出气体含有水蒸气(2)、(实验2)确定呼出气体中O2、CO2、氮气的含量(稀有气体含量忽略不计)。在老师的指导下他们设计了如图实验装置

实验操作
主要实验现象
实验结论及解释
①
检查装置气密性冰箱装置中加药品
略
略
②
打开a、b,向B中缓慢压入500mL呼出气体后关闭a
B中液体沿导管流入C中,C中液体为475mL
呼出气体中二氧化碳为mL
③
关闭a、b,用凸透镜聚光引燃白磷
白磷燃烧产生大量白烟放出大量热
呼出气体中仍然含有
④
待白磷熄灭并冷却到室温,打开b
C中液体到吸入B瓶中,C中剩余液体为400mL
呼出气体中N2的体积分数为%
(3)、(实验反思)该实验设计依据的N2性质有(填序号)
A 难溶于水 B 不能和NaOH溶液反应 C 无色无味的气体 D 不能燃烧,也不支持燃烧
(4)、实验④操作中,若C中气体未完全冷却就打开b并读数,则所测O2体积分数(“偏大”“偏小”)。16. 小林看到在伤口处涂抹过氧化氢溶液产生了小气泡,很好奇。进行如下探究:(提出问题)为什么过氧化氢溶液涂到伤口上,分解就加快了呢?
(提出猜想)猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(1)、(查阅资料)人体存在过氧化氢酶。(酶是生物催化剂,体温37℃催化效果最高,温度升降,生物活性降低)可以催化过氧化氢分解,写出该反应文字表达式。(2)、(进行实验)序号
实验步骤
实验现象
实验结论
①

用如图装置分两次进行实验,均注入5mL过氧化氢溶液。第一次在常温下进行,第二次将试管浸在37℃的温水中。
量筒中2分钟收集到的气体体积均为mL
猜想1不正确
②
用图甲装置分两次进行实验。第一次将装有过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液,第二次。
第一次,量筒中2分钟收集到的气体体积为56mL;第二次,量筒中2分钟收集到的气体体积为5mL。
(3)、(实验反思)①小林反思上述实验设计的缺陷(具体说明);
②要证明过氧化氢酶是该反应催化剂,还需证明其在反应前后和不变。
(4)、(实验拓展)为比较二氧化锰和过氧化氢酶的催化能力,小林按图乙所示装置进行实验。①取1.5毫克过氧化氢酶加入容器中,搅拌后塞紧橡皮塞。
②用注射器A从容器中抽出2毫升装置中空气,用注射器B将2毫升H2O2溶液注入容器中采集数据。直至反应结束。
③用3.1毫克、5.6毫克过氧化氢酶及3.1毫克、5.6毫克、10.7毫克相同颗粒大小的二氧化锰重复上述实验,获取数据如图丙。

①步骤②中“”操作目的是。
②小林分析相关数据,得出“相同条件下,过氧化氢酶对过氧化的催化能力比二氧化锰强”这一结论,其依据是。
③小林推测:过氧化氢酶质量过大,可能导致实验过程中过氧化氢分解突然变慢。请说明其理由。