初中化学九年级下册第十单元课题2酸和碱的中和反应
试卷更新日期:2020-12-28 类型:同步测试
一、单选题
-
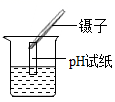
1. 下列图示的实验操作中正确的是( )


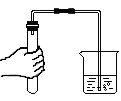
A.熄灭酒精灯
B.用滴管滴加液体
C.检查装置的气密性
D.测定溶液的pH
A、A B、B C、C D、D2. 如图所示为生活中常见物质的pH,下列说法正确的是( )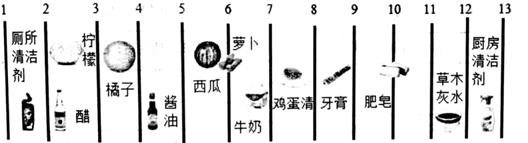 A、花盆内的土壤显酸性,可加草木灰中和其酸性 B、酱油是显碱性的食品 C、肥皂液和厕所清洗剂的混合液--定能使石蕊试液变红 D、胃酸过多的人可多吃柠檬和橘子3. 往稀盐酸里面滴加氢氧化钠溶液,如图表示该反应前后溶液中存在的主要离子,下列说法不正确的是( )
A、花盆内的土壤显酸性,可加草木灰中和其酸性 B、酱油是显碱性的食品 C、肥皂液和厕所清洗剂的混合液--定能使石蕊试液变红 D、胃酸过多的人可多吃柠檬和橘子3. 往稀盐酸里面滴加氢氧化钠溶液,如图表示该反应前后溶液中存在的主要离子,下列说法不正确的是( ) A、
A、 表示Na+
B、
表示Na+
B、 表示Cl-
C、向反应后的溶液中加入硝酸银溶液产生白色沉淀
D、向反应后的溶液中加入紫色石蕊试剂后溶液呈红色
4. 我市有些滩涂地区的土壤被称为"盐碱地",当地农民常用引进内河淡水浸泡再排水的方法改良土壤。若以土壤pH为纵坐标,浸泡水次数(m)为横坐标,下列能正确表示土壤pH变化的图像的是( )A、
表示Cl-
C、向反应后的溶液中加入硝酸银溶液产生白色沉淀
D、向反应后的溶液中加入紫色石蕊试剂后溶液呈红色
4. 我市有些滩涂地区的土壤被称为"盐碱地",当地农民常用引进内河淡水浸泡再排水的方法改良土壤。若以土壤pH为纵坐标,浸泡水次数(m)为横坐标,下列能正确表示土壤pH变化的图像的是( )A、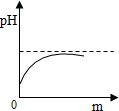 B、
B、 C、
C、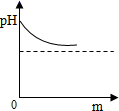 D、
D、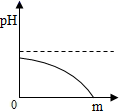 5. 如图,把质量与浓度都相同的盐酸与氢氧化钠溶液充分混合,则下列判断正确的是( )
5. 如图,把质量与浓度都相同的盐酸与氢氧化钠溶液充分混合,则下列判断正确的是( ) A、混合后溶液的pH=7 B、混合前后H2O的数目不变 C、混合后滴入紫色的石蕊溶液可变红 D、混合后得氯化钠溶液的溶质质量分数为16%6. 下表是人体内一些液体的正常pH范围,其中酸性最强的是( )
A、混合后溶液的pH=7 B、混合前后H2O的数目不变 C、混合后滴入紫色的石蕊溶液可变红 D、混合后得氯化钠溶液的溶质质量分数为16%6. 下表是人体内一些液体的正常pH范围,其中酸性最强的是( )名称
胃液
唾液
胰液
胆汁
pH
0.9-1.5
6.6-7.1
7.5-8.0
7.1-7.3
A、胃液 B、唾液 C、胰液 D、胆汁7. 推理是一种重要的化学思维方法。以下推理合理的是( )A、铝比铁活泼,所以铝制品更易腐蚀 B、许多物质能在氧气中燃烧,所以氧气可以作燃料 C、水通电生成氢气和氧气,所以水由氢气和氧气组成 D、常温下碱溶液的 ,所以该温度下 的溶液一定显碱性8. 下列饮品显碱性的是( )饮品
柠檬汁
橘子汁
牛奶
豆浆
pH
2.2~3.5
3.1~4.2
6.3~6.6
7.4~7.9
A、柠檬汁 B、橘子汁 C、牛奶 D、豆浆9. 利用推理、归纳的方法得出以下结论,其中正确的是( )A、金刚石、石墨是组成元素相同的单质,所以化学性质相似 B、氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物 C、碱溶液pH>7,所以pH>7的溶液均为碱溶液 D、铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀10. 下列用数轴表示的化学知识,错误的是( )A、生活中常见物质的pH: B、人类重要金属材料的使用史:
B、人类重要金属材料的使用史: 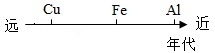 C、生铁与钢的区分:
C、生铁与钢的区分:  D、20℃时固体溶解度的相对大小:
D、20℃时固体溶解度的相对大小: 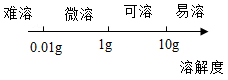 11. 图像能直观体现化学中的各种变化关系,加深对化学知识的理解。下列图像不能正确反映对应关系的是( )A、
11. 图像能直观体现化学中的各种变化关系,加深对化学知识的理解。下列图像不能正确反映对应关系的是( )A、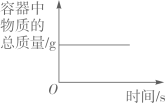 在密闭的容器中加热汞得到氧化汞
B、
在密闭的容器中加热汞得到氧化汞
B、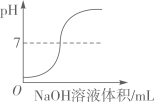 向一定量的稀盐酸中滴加氢氧化钠溶液
C、
向一定量的稀盐酸中滴加氢氧化钠溶液
C、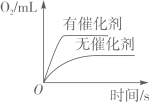 两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气
D、
两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气
D、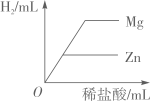 向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸
向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸
二、填空题
-
12. 某兴趣小组用稀硫酸中和含氢氧化钠的废碱液。将稀硫酸逐滴滴入到 100mL含氢氧化钠的废液中,反应过程中 pH 变化如图所示。
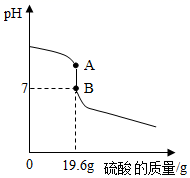 (1)、氢氧化钠的俗称是(写出一种),氢氧化钠固体敞放在空气中,变质后生成的物质的阴离子符号为。(2)、A点时溶液显性,B点时溶液中的溶质是(填化学式)。(3)、根据化学方程式计算100mL该碱性废液中含有氢氧化钠的质量。13. 宏观辨识和微观探析是化学核心素养之一。根据下列微观示意图回答。
(1)、氢氧化钠的俗称是(写出一种),氢氧化钠固体敞放在空气中,变质后生成的物质的阴离子符号为。(2)、A点时溶液显性,B点时溶液中的溶质是(填化学式)。(3)、根据化学方程式计算100mL该碱性废液中含有氢氧化钠的质量。13. 宏观辨识和微观探析是化学核心素养之一。根据下列微观示意图回答。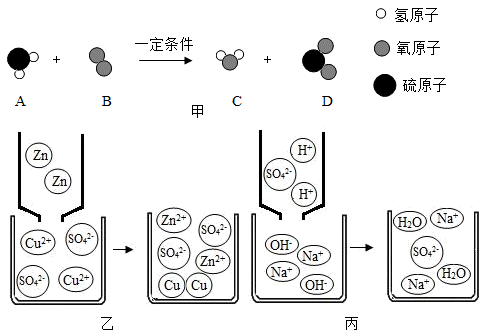 (1)、如图甲所示,物质A由元素组成,一个D分子由构成。(2)、图乙是锌粒与硫酸铜溶液恰好完全反应的微观示意图,写出反应后溶液中所有粒子的符号 , 该反应属于(填基本反应类型)。(3)、从微观的角度说明图丙的反应实质是。若想证明两种物质是否恰好完全反应,可在反应后的溶液中加入适量的试剂,该试剂是(填序号)。
(1)、如图甲所示,物质A由元素组成,一个D分子由构成。(2)、图乙是锌粒与硫酸铜溶液恰好完全反应的微观示意图,写出反应后溶液中所有粒子的符号 , 该反应属于(填基本反应类型)。(3)、从微观的角度说明图丙的反应实质是。若想证明两种物质是否恰好完全反应,可在反应后的溶液中加入适量的试剂,该试剂是(填序号)。A、BaCl2溶液
B、酚酞溶液
C、石蕊溶液
D、Na2CO3溶液
三、计算题
-
14. 实验室中稀硫酸因标签破损,需测定其质量分数。某化学兴趣小组的同学取该稀硫酸样品50g,逐滴加入质量分数为16%的NaOH溶液,溶液的pH随加入NaOH溶液质量的变化如图所示。
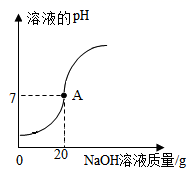 (1)、图中A点时溶液中溶质的化学式是。(2)、求稀硫酸中溶质的质量分数(写出计算过程,计算结果精确到0.01%)
(1)、图中A点时溶液中溶质的化学式是。(2)、求稀硫酸中溶质的质量分数(写出计算过程,计算结果精确到0.01%)四、实验探究题
-
15. 某化学兴趣小组的同学在进行微专题复习时,围绕酸、碱中和反应这一主题展开了深度学习。请你参与其中,按要求回答问题和开展探究。(1)、下列选项的应用与中和反应的原理无关的是____。A、使用浓硫酸干燥CO2气体 B、使用熟石灰改良酸性土壤 C、服用含有Al(OH)3的药物治疗胃酸过多症 D、利用氢氧化钠溶液洗涤石油产品中的残余硫酸(2)、某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液80g,洗涤后的溶液呈中性。这一定量石油产品中含硫酸的质量是g。(3)、做酸碱中和反应实验时,向烧杯内的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂。因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究。
(提出问题)该烧杯中溶液的溶质是什么?
(猜想)猜想一:只含有CaCl2
猜想二:含有CaCl2、HCl和Ca(OH)2
猜想三:含有CaCl2和Ca(OH)2
猜想四:含有。
同学们讨论后一致认为猜想二不合理,理由是。
(查阅资料)氯化钙溶液呈中性。
(进行实验)同学们设计了如下不同的实验方案,证明猜想四是成立的。
请帮他们填写有关实验步骤和实验现象。
方案
实验步骤
实验现象
一
取少量烧杯中的溶液于试管中,滴加几滴紫色石蕊溶液。
二
将一颗生锈铁钉放入另一支试管中,取一定量烧杯中的溶液加入其中。
三
另取少量烧杯中的溶液于第三支试管中,加入
产生气泡
(反思与拓展)①要使烧杯内溶液的溶质只含有CaCl2 , 需要除去杂质,其中的一种方法是向烧杯中加入过量的某种物质,然后过滤,该除杂原理用化学方程式表示为。
②为了验证猜想三中不含有Ca(OH)2 , 小智的方案是:取少量烧杯中溶液于试管中,滴入几滴酚酞溶液,振荡,观察到酚酞溶液不变色,即说明猜想三不正确。你还有什么方案,请说出一种:。
③结合下图,分析HCl和NaOH反应的实质:。
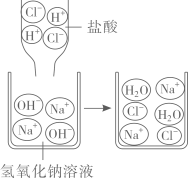
五、综合题
-
16. 覆铜板是制作印刷线路板的基本材料。
覆铜板中的金属Sn占2-10%,Cu占90-98%。简易工艺流程如
 (1)、将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是的性质(填字母代号)。
(1)、将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是的性质(填字母代号)。a、溶解性不同 b、密度不同 c、沸点不同
(2)、步骤④中涉及的分离操作是(填操作名称)。(3)、通过步骤⑤和⑥所得洗涤液的pH7(填“>”、“<”、“=”)。(4)、设计步骤⑦的主要目的是。(5)、步骤⑨中涉及的主要化学方程式为。六、推断题
-
17. 如图所示,A~H是初中化学常见的物质,已知A中含有两种元素,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂。Y为单质。
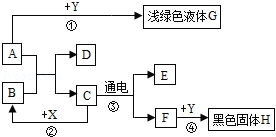
请根据图示回答下列问题:
(1)、H的化学式为(2)、A和B反应的化学方程式为。
-
-
-