初中化学人教版九年级下册第九单元课题3溶质的质量分数
试卷更新日期:2020-12-15 类型:同步测试
一、单选题
-
1. 如图是A、B两种物质的溶解度曲线,下列有关说法错误的是( )
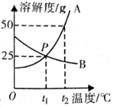 A、P点表示A,B物质在t1℃时溶解度相等 B、若B物质的溶液中混有少量A物质,可通过升温结晶的方法提纯B物质 C、t2℃时,将75gA物质的饱和溶液稀释成质量分数为20%的溶液,需加水50g D、t2℃时,将等质量A,B物质配成饱和溶液,所得溶液的质量A>B2. 现有t2℃时的溶液I、II各100g,溶液I中含物质甲50g,溶液II是物质乙的饱和溶液。物质甲、乙(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A、P点表示A,B物质在t1℃时溶解度相等 B、若B物质的溶液中混有少量A物质,可通过升温结晶的方法提纯B物质 C、t2℃时,将75gA物质的饱和溶液稀释成质量分数为20%的溶液,需加水50g D、t2℃时,将等质量A,B物质配成饱和溶液,所得溶液的质量A>B2. 现有t2℃时的溶液I、II各100g,溶液I中含物质甲50g,溶液II是物质乙的饱和溶液。物质甲、乙(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )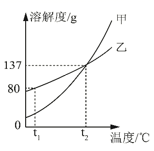 A、t2℃时,溶液I是甲的饱和溶液 B、t2℃时,溶液I中甲的质量分数为50% C、t2℃时,溶液II中含乙37g D、从t2℃降温至t1℃时,乙不会从溶液II中析出3. 如图是KNO3和NH4Cl的溶解度曲线,下列叙述错误的是( )
A、t2℃时,溶液I是甲的饱和溶液 B、t2℃时,溶液I中甲的质量分数为50% C、t2℃时,溶液II中含乙37g D、从t2℃降温至t1℃时,乙不会从溶液II中析出3. 如图是KNO3和NH4Cl的溶解度曲线,下列叙述错误的是( ) A、t1℃时,KNO3的溶解度与NH4Cl的溶解度相等 B、t2℃时,KNO3饱和溶液中溶质的质量分数是37.5% C、t1℃时,NH4Cl的不饱和溶液降温,肯定无晶体析出 D、t2℃时,KNO3饱和溶液中溶质的质量分数大于NH4Cl饱和溶液中溶质的质量分数4. 甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )
A、t1℃时,KNO3的溶解度与NH4Cl的溶解度相等 B、t2℃时,KNO3饱和溶液中溶质的质量分数是37.5% C、t1℃时,NH4Cl的不饱和溶液降温,肯定无晶体析出 D、t2℃时,KNO3饱和溶液中溶质的质量分数大于NH4Cl饱和溶液中溶质的质量分数4. 甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )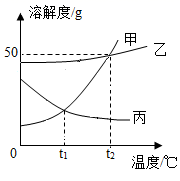 A、t1℃时,甲和丙的溶解度相等 B、降低温度可使丙的不饱和溶液变成饱和溶液 C、甲中含有少量乙时,可采用降温结晶的方法提纯甲 D、t2℃时,向80g水中加入20g甲,溶解后其溶质质量分数为20%5. NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )
A、t1℃时,甲和丙的溶解度相等 B、降低温度可使丙的不饱和溶液变成饱和溶液 C、甲中含有少量乙时,可采用降温结晶的方法提纯甲 D、t2℃时,向80g水中加入20g甲,溶解后其溶质质量分数为20%5. NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )温度/℃
0
20
40
60
NaCl的溶解度/g
35.7
36.0
36.6
37.3
KNO3的溶解度/g
13.3
31.6
63.9
110
A、20℃时,100gH2O最多能溶解36.0gNaCl B、40℃时,KNO3饱和溶液的溶质质量分数小于63.9% C、可用冷却海水的方法获取大量食盐 D、其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液6. 盐水选种是把种子放在一定浓度的盐水里,利用浮力把好坏种子分开来。20℃时,技术员将一包氯化钠(20℃,S(NaCl)=36g)放入容器中,分三次加入水,充分搅拌,记录情况如下:次数
第一次
第二次
第三次
加水质量
1000g
1000g
1000g
烧杯内NaCl晶体剩余情况
有
无
无
则第三次加水后,烧杯中所得NaCl溶液的溶质质量分数ω的范围是( )
A、10.71%<ω≤19.35% B、12%<ω≤24% C、10.71%≤ω<21.43% D、12%≤ω<24%二、填空题
-
7. 硝酸钾的溶解度曲线如图所示。回答下列问题:
 (1)、30℃时,硝酸钾的溶解度是g。(2)、60℃时,在100g水中加入60g硝酸钾固体,充分搅拌,所得溶液是(填“饱和”或“不饱和”)溶液。(3)、将(2)中所得的溶液从60℃降温至30℃,可析出硝酸钾晶体g,此时溶液的溶质质量分数45.8%(填“>”“<”或“=”)。8. 请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。
(1)、30℃时,硝酸钾的溶解度是g。(2)、60℃时,在100g水中加入60g硝酸钾固体,充分搅拌,所得溶液是(填“饱和”或“不饱和”)溶液。(3)、将(2)中所得的溶液从60℃降温至30℃,可析出硝酸钾晶体g,此时溶液的溶质质量分数45.8%(填“>”“<”或“=”)。8. 请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。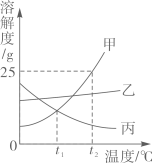 (1)、在℃时,甲、丙两种物质的溶解度相等;(2)、在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为;(3)、若乙物质中混有少量甲物质,最好采用(填"降温结晶''或“蒸发结晶")的方法提纯;(4)、t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是。9. 溶液及物质的溶解性对我们的生产生活有重要意义。如图是三种物质的溶解度曲线,请回答:
(1)、在℃时,甲、丙两种物质的溶解度相等;(2)、在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为;(3)、若乙物质中混有少量甲物质,最好采用(填"降温结晶''或“蒸发结晶")的方法提纯;(4)、t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是。9. 溶液及物质的溶解性对我们的生产生活有重要意义。如图是三种物质的溶解度曲线,请回答: (1)、三种物质中,的溶解度受温度影响最大。(2)、80℃时硝酸钠的溶解度是g。(3)、将70℃时三种物质的饱和溶液分别降温至30℃,所得溶液为不饱和溶液的是溶液。(4)、硝酸钾属于复合肥料,所含营养元素有 , 溶质质量分数为3%的硝酸钾溶液常用作无土栽培的营养液,配制这种营养液150kg,需要硝酸钾固体的质量是kg。
(1)、三种物质中,的溶解度受温度影响最大。(2)、80℃时硝酸钠的溶解度是g。(3)、将70℃时三种物质的饱和溶液分别降温至30℃,所得溶液为不饱和溶液的是溶液。(4)、硝酸钾属于复合肥料,所含营养元素有 , 溶质质量分数为3%的硝酸钾溶液常用作无土栽培的营养液,配制这种营养液150kg,需要硝酸钾固体的质量是kg。三、综合题
-
10. 为测定氯化钠和碳酸钠混合物的组成情况,某研究小组进行了如下实验。
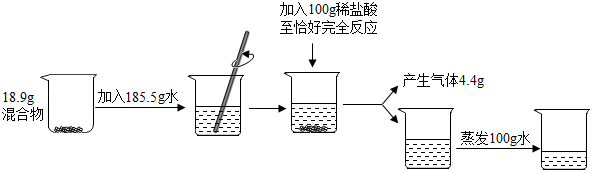 (1)、实验中发生反应的化学方程式为。(2)、求解混合物中发生反应物质的质量(x)的比例式为。(3)、混合物中氯化钠和碳酸钠质量的最简整数比为。(4)、蒸发后所得溶液的溶质质量分数为。(5)、若用36.5%的浓盐酸配制实验所用的稀盐酸,需加水的质量。(6)、上述稀释操作中,需要用到的实验仪器有量筒、烧杯、。11. 溶液与人类生产、生活密切相关。(1)、把少量下列物质分别放入水中,充分搅拌,能得到溶液的是___________(填序号)。A、硝酸钾 B、植物油 C、面粉(2)、下列有关溶液的说法中,正确的是_________(填序号)。A、凡是均一的、稳定的液体一定是溶液 B、溶液是均一的、稳定的混合物 C、溶液一定是无色的,且溶剂一定是水(3)、如图为甲、乙、丙三种固体物质的溶解度曲线。
(1)、实验中发生反应的化学方程式为。(2)、求解混合物中发生反应物质的质量(x)的比例式为。(3)、混合物中氯化钠和碳酸钠质量的最简整数比为。(4)、蒸发后所得溶液的溶质质量分数为。(5)、若用36.5%的浓盐酸配制实验所用的稀盐酸,需加水的质量。(6)、上述稀释操作中,需要用到的实验仪器有量筒、烧杯、。11. 溶液与人类生产、生活密切相关。(1)、把少量下列物质分别放入水中,充分搅拌,能得到溶液的是___________(填序号)。A、硝酸钾 B、植物油 C、面粉(2)、下列有关溶液的说法中,正确的是_________(填序号)。A、凡是均一的、稳定的液体一定是溶液 B、溶液是均一的、稳定的混合物 C、溶液一定是无色的,且溶剂一定是水(3)、如图为甲、乙、丙三种固体物质的溶解度曲线。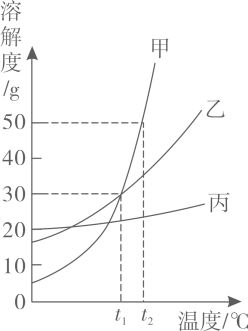
①t1℃时,甲、乙两种物质的溶解度(填“相等”或“不相等”)。
②t2℃时,甲物质饱和溶液中溶质与溶剂的质量比为(填最简比)。
③现有t1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是(填序号)。
A.甲>乙>丙
B.甲=乙<丙
C.甲=乙>丙
(4)、用固体氯化钠和蒸馏水配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠的质量为g。若用已配好的50g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为g。四、计算题
-
12. 铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如右图所示,计算:
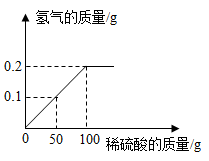 (1)、充分反应后生成氢气的质量为g。(2)、合金样品中锌的质量为。(3)、恰好完全反应时,所得溶液溶质的质量分数为。(结果保留一位小数)13. 为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:
(1)、充分反应后生成氢气的质量为g。(2)、合金样品中锌的质量为。(3)、恰好完全反应时,所得溶液溶质的质量分数为。(结果保留一位小数)13. 为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:第1次
第2次
第3次
第4次
第5次
滴入稀硫酸的质量/g
25
25
25
25
25
生成气体的总质量/g
0.05
m
0.15
0.20
0.20
请完成下列问题:
(1)、表中m的值为;(2)、银、锌合金中银的质量分数为;(3)、所用稀硫酸的溶质质量分数是多少?(写出具体计算过程)14. 实验室用硫酸铜(不含结晶水)作过氧化氢溶液制取氧气的催化剂。现在2.0g硫酸铜中加入34.0g过氧化氢溶液,充分反应后,实验的相关数据如图。(不考虑反应过程中水分的蒸发),请计算:
(1)、制得氧气的质量为g。(2)、过氧化氢溶液中溶质的质量分数为多少?(写出计算过程)。(3)、反应后所得硫酸铜溶液的溶质质量分数为(精确到0.1%)。
15. 过氧化氢溶液俗称双氧水,是一种常见消毒剂。实验员用以下方法制取了少量过氧化氢溶液,在低温下,向56.4g某浓度的稀硫酸中逐渐加入一定量的过氧化钡(BaO2),发生的化学反应为BaO2+H2SO4=BaSO4↓+H2O2,当恰好完全反应时生成23.3g沉淀。计算:(1)、加入BaO2的质量。(2)、反应后所得溶液中溶质质量分数。(3)、医用双氧水常为溶质质量分数为3%的过氧化氢溶液,如果将(2)中所得溶液稀释到医用双氧水浓度,计算需加入水的质量(结果精确到0.1g)。