初中化学人教版九年级下册第八单元课题2 金属的化学性质
试卷更新日期:2020-12-01 类型:同步测试
一、单选题
-
1. 北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是( )A、“烹胆矾则成铜”是物理变化 B、胆矾可用于配制波尔多液 C、“熬之则成胆矾”是蒸发结晶过程 D、“熬胆矾铁釜,久之亦化为铜”发生反应2. 把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )A、Y>X>Z B、Y>Z>X C、X>Z>Y D、Z>X>Y3. 已知A,B,C,D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应;相同条件下,C,D能与稀盐酸反应产生H2,且D比C反应剧烈。则四种金属的活动性由强到弱的顺序是( )A、D>C>A>B B、A>B>C>D C、B>A>C>D D、D>C>B>A4. 除去下列物质中的少量杂质(括号内为杂质),其操作错误的是( )A、Cu粉(Fe粉)------用磁铁吸引 B、N2(O2)-------将混合气体通过灼热的铜丝网 C、CO(CO2)------将混合气体通过灼热的氧化铁粉末 D、MnO2(KCl)------将混合物溶解于水、过滤、洗涤、干燥5. 为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是( )A、MgCl2溶液、Cu、Sn B、Mg、Cu、SnCl2溶液 C、Mg、Sn、Cu、盐酸 D、MgCl2溶液、Sn、CuCl2溶液6. 将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )A、滤液中一定含有Mg2+和Fe3+ B、滤液中含有Mg2+和Ag+ C、滤渣中一定含有Ag D、滤渣中可能含有Mg7. 某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有:( )A、4个 B、3个 C、2个 D、1个8. 在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系如图。综合以上信息得到以下结论,合理的是( )
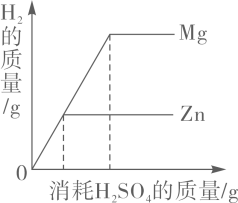 A、从图象可以看出,金属镁比金属锌的活动性强 B、若两种金属都有剩余,二者得到的氢气质量相同 C、若硫酸有剩余,二者得到氢气的质量相同 D、若两种金属完全溶解,二者消耗硫酸的质量相同9. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A、从图象可以看出,金属镁比金属锌的活动性强 B、若两种金属都有剩余,二者得到的氢气质量相同 C、若硫酸有剩余,二者得到氢气的质量相同 D、若两种金属完全溶解,二者消耗硫酸的质量相同9. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )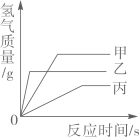 A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙10. 验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法错误的是( )
A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙10. 验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法错误的是( )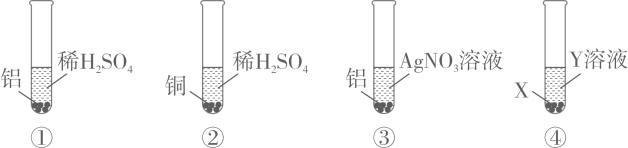 A、通过①②实验,可以证明金属活动性Al>Cu B、通过①②③实验,可以证明金属活动性Al>Cu>Ag C、若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液 D、若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液11. 现有一包由2.4g镁、6.5g锌、1.6g碳混合而成的粉末,把它加入到一定量的硝酸银溶液中,反应结束后,经过滤、洗涤、干燥,测得滤渣含有三种物质。则滤渣的质量可能是( )A、10.5g B、35.6g C、44.8g D、45.8g
A、通过①②实验,可以证明金属活动性Al>Cu B、通过①②③实验,可以证明金属活动性Al>Cu>Ag C、若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液 D、若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液11. 现有一包由2.4g镁、6.5g锌、1.6g碳混合而成的粉末,把它加入到一定量的硝酸银溶液中,反应结束后,经过滤、洗涤、干燥,测得滤渣含有三种物质。则滤渣的质量可能是( )A、10.5g B、35.6g C、44.8g D、45.8g二、实验探究题
-
12. 小雨同学为验证镁、铁、锌三种金属的活动性,进行了下图所示实验:
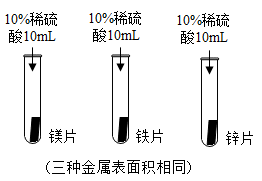
①实验中,小雨观察到的现象是 , 由此得出三种金属的活动性:镁>锌>铁;
②小明还补充了铁片与硫酸铜溶液反应的实验,实验中观察到的现象是 , 有关反应的化学方程式为。由此得出铁、铜两种金属的活动性:铁铜(填“>”“=”“<”)。
三、综合题
-
13. 从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:
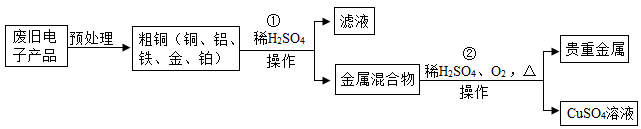 (1)、图中“操作”的名称是 。(2)、写出所得贵重金属中任意一种成分的化学式。(3)、写出①中发生的化学反应方程式(任写一种);该反应的基本类型为 。(4)、写出②中发生的化学反应方程式。14. 金属材料广泛应用于生产、生活中。(1)、用铜作导线,利用了铜的延展性和性。(2)、镁是一种活泼的金属,请写出镁与稀盐酸反应的化学方程式。(3)、将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是 , 相对原子质量最大的是。
(1)、图中“操作”的名称是 。(2)、写出所得贵重金属中任意一种成分的化学式。(3)、写出①中发生的化学反应方程式(任写一种);该反应的基本类型为 。(4)、写出②中发生的化学反应方程式。14. 金属材料广泛应用于生产、生活中。(1)、用铜作导线,利用了铜的延展性和性。(2)、镁是一种活泼的金属,请写出镁与稀盐酸反应的化学方程式。(3)、将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是 , 相对原子质量最大的是。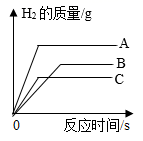 (4)、向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是(填字母序号)。
(4)、向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是(填字母序号)。A若滤渣只含一种金属,则滤液中的溶质只有三种
B若滤液中含有两种金属离子,则滤渣中的固体只有两种
C若最终得到的滤渣质量仍为mg,则滤液中溶质最多有两种
D若向滤渣中加入稀盐酸,有气泡产生,则滤液中的溶质最多有两种
四、计算题
-
15. 生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数
加盐酸前
第1次
第2次
第3次
第4次
第5次
加入稀盐酸的质量(g)
0
20
20
20
20
20
锥形瓶内物质的总质量(g)
11.5
31.4
m
71.2
91.1
111.1
(查阅资料)碳不与稀盐酸反应。
请回答下列问题:
(1)、根据质量守恒定律,该反应中生成气体的总质量为。(2)、实验数据表中m的值为。(3)、请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
-