山东省潍坊市临朐县2019-2020学年九年级上学期化学期末考试试卷
试卷更新日期:2020-11-16 类型:期末考试
一、单选题
-
1. 丝绸之路将我国古代的方面与技术传送到了国外。下列我国古代生产工艺中没有发生化学变化的是( )A、烧制瓷器 B、湿法炼铜 C、高梁酿酒 D、纺纱织布2. 下列实验基本操作正确的是( )A、称量固体药品
 B、倾倒液体
B、倾倒液体  C、检查气密性
C、检查气密性  D、给液体加热.
D、给液体加热.  3. 2019年6月5日世界环境日大会在中国举行,世界各国达成共识:全力改善环境质量,全推动绿色发展。下列做法符合绿色发展理念的是()A、垃圾分类回收,增强节约意识 B、鼓励开私家车,带动经济发展 C、大量使用化肥,提高粮食产量 D、燃放烟花爆竹,增添节日气氛4. 下列有关物质性质与用途对应关系正确的是()A、CO2能与水反应,可用于灭火 B、铜有金属光泽,可用于制造电线 C、常温下N2很稳定,可用作粮食保护气 D、石墨具有导电性,可用于生产铅笔芯5. 下列物质按照混合物、氧化物、单质顺序排列的是( )A、空气、二氧化锰、氧气 B、海水、氯酸钾、氢气 C、氧化铁、锰酸钾、水 D、硫酸铜、高锰酸钾、二氧化碳6. 化学的学习使我们学会了从微观角度认识宏观现象。下列对宏观现象的解释正确的是()A、热胀冷缩﹣﹣温度升高,微粒变大;温度降低,微粒变小 B、电解水分子分解,生成了氢分子和氧分子 C、在一定条件下,CO2气体会变成固体﹣﹣﹣此时,CO2分子停止运动 D、金刚石和石墨的物理性质存在很大差异是构成它们的原子不同7. 2019 中国水周主题:“坚持节水优先,强化水资源管理”。下列认识正确的是( )A、生活中常用煮沸的方法降低水的硬度 B、过滤可以除去水中所有的杂质 C、电解水实验说明水由氢气和氧气组成 D、明矾可促进浑浊水中不溶性杂质的沉降8. 下列化学符号中关于数字“2”的意义说法错误的是( )A、2CO-表示2个一氧化碳分子 B、NO2-表示二氧化氮中含有2个氧原子 C、Ca2+-表示1个钙离子带2个单位的正电荷 D、 -表示氧化汞中汞元素的化合价为+2价9. 《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。这句话说明合金具有的特性是()A、合金的熔点一般比其组分低 B、合金的硬度一般比其组分大 C、合金的抗腐蚀性一般比其组分强 D、合金的耐磨性一般比其组分好10. 丙烷(C3H8)是液化石油气的主要成分之一,燃烧前后分子种类变化的微观示意图如下。下列说法正确的是()
3. 2019年6月5日世界环境日大会在中国举行,世界各国达成共识:全力改善环境质量,全推动绿色发展。下列做法符合绿色发展理念的是()A、垃圾分类回收,增强节约意识 B、鼓励开私家车,带动经济发展 C、大量使用化肥,提高粮食产量 D、燃放烟花爆竹,增添节日气氛4. 下列有关物质性质与用途对应关系正确的是()A、CO2能与水反应,可用于灭火 B、铜有金属光泽,可用于制造电线 C、常温下N2很稳定,可用作粮食保护气 D、石墨具有导电性,可用于生产铅笔芯5. 下列物质按照混合物、氧化物、单质顺序排列的是( )A、空气、二氧化锰、氧气 B、海水、氯酸钾、氢气 C、氧化铁、锰酸钾、水 D、硫酸铜、高锰酸钾、二氧化碳6. 化学的学习使我们学会了从微观角度认识宏观现象。下列对宏观现象的解释正确的是()A、热胀冷缩﹣﹣温度升高,微粒变大;温度降低,微粒变小 B、电解水分子分解,生成了氢分子和氧分子 C、在一定条件下,CO2气体会变成固体﹣﹣﹣此时,CO2分子停止运动 D、金刚石和石墨的物理性质存在很大差异是构成它们的原子不同7. 2019 中国水周主题:“坚持节水优先,强化水资源管理”。下列认识正确的是( )A、生活中常用煮沸的方法降低水的硬度 B、过滤可以除去水中所有的杂质 C、电解水实验说明水由氢气和氧气组成 D、明矾可促进浑浊水中不溶性杂质的沉降8. 下列化学符号中关于数字“2”的意义说法错误的是( )A、2CO-表示2个一氧化碳分子 B、NO2-表示二氧化氮中含有2个氧原子 C、Ca2+-表示1个钙离子带2个单位的正电荷 D、 -表示氧化汞中汞元素的化合价为+2价9. 《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。这句话说明合金具有的特性是()A、合金的熔点一般比其组分低 B、合金的硬度一般比其组分大 C、合金的抗腐蚀性一般比其组分强 D、合金的耐磨性一般比其组分好10. 丙烷(C3H8)是液化石油气的主要成分之一,燃烧前后分子种类变化的微观示意图如下。下列说法正确的是() A、甲中碳、氢元素质量比为3:8 B、乙和丙的元素组成相同 C、44g甲完全燃烧至少需160g乙 D、生成的丙与丁的分子个数比为1:111. 据西安电子科技大学芜湖研究所介绍,国内5G通信芯片用氮化镓材料制成。如图是氮元素在元素周期表中的信息以及镓原子的结构示意图。下列说法错误的是( )
A、甲中碳、氢元素质量比为3:8 B、乙和丙的元素组成相同 C、44g甲完全燃烧至少需160g乙 D、生成的丙与丁的分子个数比为1:111. 据西安电子科技大学芜湖研究所介绍,国内5G通信芯片用氮化镓材料制成。如图是氮元素在元素周期表中的信息以及镓原子的结构示意图。下列说法错误的是( ) A、氮原子核内质子数为7 B、图中x=18 C、镓原子核内中子数为31 D、氮原子的相对原子质量为14.0112. 接近毒品就是走向死亡,摇头丸是一种新型毒品,吸食后对身体有严重的危害,其主要成分是MDMA(化学式为C11H15NO2),下列说法错误的是()A、MDMA由4种元素组成 B、一个MDMA分子中含有29个原子 C、MDMA的相对分子质量为193g D、MDMA中氢,氮元素的质量比为15:1413. 密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
A、氮原子核内质子数为7 B、图中x=18 C、镓原子核内中子数为31 D、氮原子的相对原子质量为14.0112. 接近毒品就是走向死亡,摇头丸是一种新型毒品,吸食后对身体有严重的危害,其主要成分是MDMA(化学式为C11H15NO2),下列说法错误的是()A、MDMA由4种元素组成 B、一个MDMA分子中含有29个原子 C、MDMA的相对分子质量为193g D、MDMA中氢,氮元素的质量比为15:1413. 密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( ) A、该反应属于分解反应 B、丁一定是该反应的催化剂 C、若消耗3g乙,则生成17g丙 D、反应前甲、乙的质量之和一定等于生成丙的质量14. 下列关于化学学科基本观念的说法正确的是( )A、能量观一一生石灰与水反应是放热反应 B、转化观一一铁与盐酸反应可以一步转化为氯化铁 C、微粒观一一氯化钠由分子构成 D、守恒观一一化学反应前后分子的种类不变15. 草酸亚铁晶体(FeC2O4﹒2H2O)受热分解的化学方程式为: 。通过如图装置吸收或验证该反应得到的气体产物,其说法错误的是( )
A、该反应属于分解反应 B、丁一定是该反应的催化剂 C、若消耗3g乙,则生成17g丙 D、反应前甲、乙的质量之和一定等于生成丙的质量14. 下列关于化学学科基本观念的说法正确的是( )A、能量观一一生石灰与水反应是放热反应 B、转化观一一铁与盐酸反应可以一步转化为氯化铁 C、微粒观一一氯化钠由分子构成 D、守恒观一一化学反应前后分子的种类不变15. 草酸亚铁晶体(FeC2O4﹒2H2O)受热分解的化学方程式为: 。通过如图装置吸收或验证该反应得到的气体产物,其说法错误的是( ) A、①中装有氧化钙固体,可吸收气体产物中的水蒸气 B、②中固体由黑色变红色,可验证原气体产物中有一氧化碳 C、③中石灰水变浑浊,可验证原气体产物中有二氧化碳 D、③中尾气进行点燃,可防止尾气造成污染16. 分析推理是学习化学的一种重要方法, 以下分析推理正确的是( )A、蜡烛燃烧后质量减小,所以蜡烛燃烧不遵循质量守恒定律 B、一氧化碳和二氧化碳的分子构成不同,所以化学性质不同 C、溶液具有均一性、稳定性,所以具有均一性和稳定性的液体一定是溶液 D、原子核由质子和中子构成,则原子中都含有质子和中子17.
A、①中装有氧化钙固体,可吸收气体产物中的水蒸气 B、②中固体由黑色变红色,可验证原气体产物中有一氧化碳 C、③中石灰水变浑浊,可验证原气体产物中有二氧化碳 D、③中尾气进行点燃,可防止尾气造成污染16. 分析推理是学习化学的一种重要方法, 以下分析推理正确的是( )A、蜡烛燃烧后质量减小,所以蜡烛燃烧不遵循质量守恒定律 B、一氧化碳和二氧化碳的分子构成不同,所以化学性质不同 C、溶液具有均一性、稳定性,所以具有均一性和稳定性的液体一定是溶液 D、原子核由质子和中子构成,则原子中都含有质子和中子17.下列实验操作能够达到目的是( )
A
B
C
D

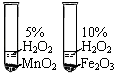


测定空气中氧气
含量
比较MnO2和Fe2O3
的催化效果
收集氧气并测量
氧气的体积
探究可燃物燃烧的
条件
A、A B、B C、C D、D18. 某学生将锌粒放入CuSO4溶液中, 发现锌粒表面有红色物质析出,同时还有少量无色无味气泡产生。对于产生气泡的“异常现象”,同学们对“放出气体”这一异常现象进行猜想、实验。其中没有价值的是( )A、猜想产生的气体可能是CO2并检验 B、猜想产生的气体可能是H2并检验 C、CuSO4溶液中可能含有少量的某种酸 D、认为试剂变质,更换后再实验19. 下图是三种常见固体物质的溶解度曲线,下列说法正确的是( ) A、t1℃时,A和C的饱和溶液中含有相同质量的溶质 B、欲除去A溶液中少量的B物质,常采用蒸发结晶的方法 C、t1℃时,将80gA的饱和溶液稀释为质量分数为20%的溶液,需要加水的质童为70g D、t2℃时,将A,B,C的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为:B>A=C20. 数形结合能对化学反应进行定量描述,下列图象能正确反映对应变化关系的是()A、
A、t1℃时,A和C的饱和溶液中含有相同质量的溶质 B、欲除去A溶液中少量的B物质,常采用蒸发结晶的方法 C、t1℃时,将80gA的饱和溶液稀释为质量分数为20%的溶液,需要加水的质童为70g D、t2℃时,将A,B,C的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为:B>A=C20. 数形结合能对化学反应进行定量描述,下列图象能正确反映对应变化关系的是()A、 一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
B、
一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
B、 等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
C、
等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
C、 等质量的铁粉和锌粉分别与足量溶质质量分数相同的稀硫酸反应
D、
等质量的铁粉和锌粉分别与足量溶质质量分数相同的稀硫酸反应
D、 高温条件下一氧化碳还原氧化铁
高温条件下一氧化碳还原氧化铁
二、填空题
-
21. 化学改变世界,科技改变生活。请回答:
 (1)、我国自主研发的“复兴号”动车组列车,领跑世界,其制造材料有铝合金等,在空气中铝制品耐腐蚀的原因是。(用化学方程式表示)(2)、我国在氢能源汽车研发领域取得重大突破,采用了第四代以氢为燃料的电池技术。氢气作为理想能源前景广阔,氢能源的优点是:。(3)、汽车上有多种化学材料。汽车的许多部件是金属合金,它属于材料。(4)、汽车用铜线作为充电的导线。我国古代将赤铜(Cu2O) 和木炭分混合加热到800℃得到铜。反应的化学方程式是:。(5)、扫描二维码可以租用“共享汽车”,二维码的制作材料一般是用 PVC不干胶贴纸。PVC[化学式(C2H3Cln]中碳元素和氢元素的质量比为。22. 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。(1)、填写有关含碳物质的对应特性。
(1)、我国自主研发的“复兴号”动车组列车,领跑世界,其制造材料有铝合金等,在空气中铝制品耐腐蚀的原因是。(用化学方程式表示)(2)、我国在氢能源汽车研发领域取得重大突破,采用了第四代以氢为燃料的电池技术。氢气作为理想能源前景广阔,氢能源的优点是:。(3)、汽车上有多种化学材料。汽车的许多部件是金属合金,它属于材料。(4)、汽车用铜线作为充电的导线。我国古代将赤铜(Cu2O) 和木炭分混合加热到800℃得到铜。反应的化学方程式是:。(5)、扫描二维码可以租用“共享汽车”,二维码的制作材料一般是用 PVC不干胶贴纸。PVC[化学式(C2H3Cln]中碳元素和氢元素的质量比为。22. 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。(1)、填写有关含碳物质的对应特性。物质用途
金刚石切割玻璃
石墨作电极
对应特征
①
②
(2)、在440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C) 和碳酸钠,该反应的化学方程式为。(3)、“ 碳海绵”是已知最轻的固体材料,由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是(填字母序号)。A 具有吸附性
B 可重复使用
C 可处理海上石油泄漏.
(4)、液态二氧化碳灭火器可用于扑救档案资料发生的火灾,下列说法错误的有。A液态二氧化碳气化后不会污染档案资料
B 二氧化碳可覆盖燃烧物表面,隔绝空气
C 液态二氧化碳气化时吸热,降低了可燃物的着火点
23. 金属材料在生产生活中有着广泛的应用,人类生产和生活都离不开金属。(1)、新型材料纳米级铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如图所示,写出制备工艺的化学方程式: , 其反应类型是:。反应前需向反应器中通入氮气,目的是。 (2)、如图为Mn和CuSO4溶液反应的示意图,回答下列问题:
(2)、如图为Mn和CuSO4溶液反应的示意图,回答下列问题:
①实际与Mn反应的粒子是。
②反应中失去电子的粒子是。
③由反应可知金属的活泼性: MnCu (填“>”或“<”)。
④该反应中化合价没有改变的元素或根是(填对应选项的字母)。
A 锰元素
B 铜元素
C 硫酸根
(3)、工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中反应的化学方程式为:。(4)、小童要用其它方法验证铜、铁、镁的活动性顺序,他选择了打磨过的铁丝,你认为他还需选的另外两种溶液是溶液和溶液。24. 溶液与人们的生活息息相关。(1)、下列少量物质分别放入水中,充分搅拌,可以得到溶液的是 (填字母) 。A 高锰酸钾
B 汽油.
C 面粉
(2)、在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度升高。这种物质是(填字母)。A硝酸铵
B氢氧化钠
C氯化钠
(3)、水是一种常见的溶剂,如图是硝酸钾、氯化钾的溶解度曲线。请回答下列问题:
①t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定 形成饱和溶液的是 , 其溶液的溶质质量分数为(结果精确到0.1%)。
②图2是硝酸钾溶液的实验情况。若保持溶液的质量不变,操作I为。
③下列有关说法错误的是。
A ①与②的溶质质量可能相等
B ②与③的溶质质量分数一定相等
C 等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D 等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
三、实验题
-
25. 化学是一门以实验为基础的科学。请根据下图实验装置完成有关问题:
 (1)、检查装置A气密性的方法是夹紧止水夹, , 则气密性良好。(2)、用H2O2制取氧气,选择的发生装置为 (填字母), 反应方程式为。(3)、用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为 , 在F中气体应从导管(填“b”或“c”)端通入。(4)、实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。选择的发生装置为(填字母)。用装置E收集甲烷,利用了甲烷的物理性质;用装置C而不用装置D收集甲烷,原因是。
(1)、检查装置A气密性的方法是夹紧止水夹, , 则气密性良好。(2)、用H2O2制取氧气,选择的发生装置为 (填字母), 反应方程式为。(3)、用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为 , 在F中气体应从导管(填“b”或“c”)端通入。(4)、实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。选择的发生装置为(填字母)。用装置E收集甲烷,利用了甲烷的物理性质;用装置C而不用装置D收集甲烷,原因是。四、综合应用题
-
26. 镁铝合金强度大、密度小,合金表面易上色,常用作笔记本电脑的外壳。(1)、Ⅰ.形状大小相同的铝和镁,分别放入同样的盐酸溶液中,下列说法错误的是(填序号)。
A 两者都发生反应 B 镁比铝反应剧烈 C 铝不与盐酸溶液反应
(2)、镁与氢氧化钠溶液不反应,而金属铝能与氢氧化钠、水共同作用生成易溶于水的钠盐(用化学式NaAlO2表示)和H2 , 写出该反应的化学方程式:。(3)、Ⅱ.三位同学通过进行如下途径探究,来推算某铝镁合金(假设不含其它杂质)中铝的质量分数。方案一:镁铝合金与氧气反应,测定参与反应的氧气体积。如图所示,称量一定量镁铝合金粉末,在足量的氧气中充分燃烧,冷却至室温,打开止水夹。参与反应的氧气体积与相等。
 (4)、方案二:铝镁合金与盐酸反应,测定生成气体的体积。装置如图所示。
(4)、方案二:铝镁合金与盐酸反应,测定生成气体的体积。装置如图所示。
①通过排水法测定所收集到的氢气体积,装置导管口a、b、c、d的连接顺序是:a→→→
②反应结束,冷却至室温。烧瓶内还留有气体,对实验结果(填“有”或“没有”)影响。
(5)、方案三:铝镁合金与氢氧化钠溶液反应,测定剩余固体质量。称取8g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,反应过程如下图:
①实验中所加的氢氧化钠溶液应过量,其目的是。
②从上图数据可知,该合金中镁元素与铝元素的质量比为。
(反思与拓展)利用铝镁合金中铝与氢氧化钠溶液反应反应和方案二装置,通过测定体积,也可得出合金中铝的质量。
五、计算题
-
27. 石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中的碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200克,平均分成4份,进行实验,结果如下:
实验
1
2
3
4
加入样品的质量(克)
5
10
15
20
生成CO2的质量(克)
1.76
3.52
4.4
m
(1)、哪几次反应中矿石有剩余?(2)、上表中m的数值是多少?(3)、试计算这种石灰石中碳酸钙的质量分数。
-
-