福建省福州市2019-2020学年九年级上学期化学期末考试试卷
试卷更新日期:2020-11-10 类型:期末考试
一、单选题
-
1. 雾炮车向空中喷水净化空气,主要除去的污染物是( )A、固体颗粒物 B、一氧化碳 C、二氧化碳 D、臭氧2. 下列物质用途主要由其物理性质决定的是( )A、氮气作保护气 B、氢气作高能燃料 C、氖气管通电会发红光 D、墨汁作画久不变色3. 从微观角度解释“干冰升华”现象,下列叙述正确的是( )A、分子体积增大 B、分子数目增多 C、分子间距离变大 D、分 子种类改变4. 实验室制取二氧化碳的部分操作如下图,其中错误的是( )A、
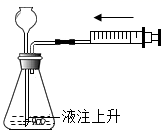 查漏
B、
查漏
B、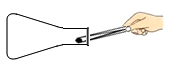 装药
C、
装药
C、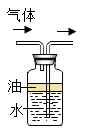 收集
D、
收集
D、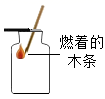 验满
5. 石墨烯是由碳原子构成的单层片状结构的新材料(如下图),即极薄的石墨;中国天才少年曹原把两层石墨烯扭转一个“ 魔角(1.1°)”后,产生神奇的低温超导效应。下列有关说法正确的是( )
验满
5. 石墨烯是由碳原子构成的单层片状结构的新材料(如下图),即极薄的石墨;中国天才少年曹原把两层石墨烯扭转一个“ 魔角(1.1°)”后,产生神奇的低温超导效应。下列有关说法正确的是( )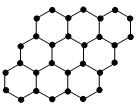 A、石墨烯属于化合物 B、单层和两层石墨烯均有导电性 C、石墨烯叠加过程有新物质产生 D、单层石墨烯中每个碳原子跟4个碳原子相连6. 故宫博物院收藏的《千里江山图》所采用的颜料有:朱砂(含HgS)、赭石(含Fe2O3)、砗磲(含CaCO3)和孔雀石[含Cu2(OH)2CO3]等。下列分析正确的是( )A、朱砂是白色固体 B、Fe2O3中铁元素的质量分数为70% C、CaCO3中碳元素化合价为+2价 D、Cu2(OH)2CO3中氢、氧元素质量比为2:57. 有关物质的组成、结构、性质和变化规律的叙述正确的是( )A、钢的含碳量高于生铁,所以钢的性能优于生铁 B、水通电生成氢气和氧气,说明水由氧气和氢气组成 C、金的化学性质不活泼,金在自然界中以单质形式存在 D、一氧化碳和二氧化碳中碳原子排列方式不同,所以性质不同8. 用如图所示装置(气密性良好)测定空气中氧气的含量,加热粗铜丝一段时间后,白磷燃烧。下列说法正确的是( )
A、石墨烯属于化合物 B、单层和两层石墨烯均有导电性 C、石墨烯叠加过程有新物质产生 D、单层石墨烯中每个碳原子跟4个碳原子相连6. 故宫博物院收藏的《千里江山图》所采用的颜料有:朱砂(含HgS)、赭石(含Fe2O3)、砗磲(含CaCO3)和孔雀石[含Cu2(OH)2CO3]等。下列分析正确的是( )A、朱砂是白色固体 B、Fe2O3中铁元素的质量分数为70% C、CaCO3中碳元素化合价为+2价 D、Cu2(OH)2CO3中氢、氧元素质量比为2:57. 有关物质的组成、结构、性质和变化规律的叙述正确的是( )A、钢的含碳量高于生铁,所以钢的性能优于生铁 B、水通电生成氢气和氧气,说明水由氧气和氢气组成 C、金的化学性质不活泼,金在自然界中以单质形式存在 D、一氧化碳和二氧化碳中碳原子排列方式不同,所以性质不同8. 用如图所示装置(气密性良好)测定空气中氧气的含量,加热粗铜丝一段时间后,白磷燃烧。下列说法正确的是( )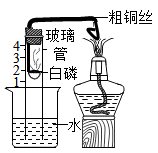 A、白磷燃烧产生大量白色烟雾 B、该实验过程只发生一个化学变化 C、玻璃管中液面从实验开始持续上升至约“刻度1”处 D、氮气不与磷反应且难溶于水是设计该实验的依据之一9. 下列实验方案不能达到实验目的的是( )
A、白磷燃烧产生大量白色烟雾 B、该实验过程只发生一个化学变化 C、玻璃管中液面从实验开始持续上升至约“刻度1”处 D、氮气不与磷反应且难溶于水是设计该实验的依据之一9. 下列实验方案不能达到实验目的的是( )选项
实验目的
实验方案
A
鉴别氮气和二氧化碳
使用紫色石蕊溶液
B
除去氯化钾中混有少量的氯酸钾
充分加热固体至质量不再减少
C
验证Fe、Cu、Ag的金属活泼性
将铜分别伸入硫酸亚铁溶液和硝酸银溶液
D
探究甲烷中仅含碳元素和氢元素
点燃甲烷,检验到有水和二氧化碳生成
A、A B、B C、C D、D10. 胆矾(CuSO4﹒5H2O相对分子质量为250)完全脱水的化学方程式为: 。加热25.0g胆矾过程中,测得固体质量随温度变化曲线如图,下列分析正确的是( )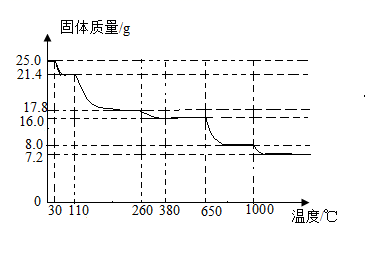 A、胆矾属于混合物 B、胆矾失水的温度范围为30℃~380℃ C、1000℃时,得到固体物质的化学式为CuSO4 D、开始加热至完全脱水,胆矾经历5次脱水过程
A、胆矾属于混合物 B、胆矾失水的温度范围为30℃~380℃ C、1000℃时,得到固体物质的化学式为CuSO4 D、开始加热至完全脱水,胆矾经历5次脱水过程二、流程题
-
11. 垃圾分类、人人有责。某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下图:

[资料]铁锈的主要成分是氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水。
(1)、牛奶盒属于 (填标号)。A 厨余垃圾
B 有害垃圾
C 其他垃圾
D 可回收垃圾
(2)、铁锈蚀主要是铁与空气中的发生化学反应。(3)、①“归中反应”是指同种元素组成的不同物质间发生反应,元素的两种化合价向中间价态靠拢。硫酸铁与(填物质)反应生成硫酸亚铁,即是归中反应。②溶解步骤中,产生氢气的反应(写化学方程式)。
三、实验题
-
12. 模拟自来水生产过程的装置如图。
 (1)、检验天然水是否为硬水,使用的试剂是。(2)、明矾[KAl(SO4)2﹒12H2O] 溶于水,溶液中含有钾离子、硫酸根离子、铝离子等,写出其中一种金属离子的符号:。(3)、装置C中填充的材料有①活性炭、②粗沙、③细沙、④棉花(每种材料之间都用纱布隔开) ,填充材料由上到下的顺序是 ( 填序号);其中活性炭的作用是;若用滤纸(孔径为30~ 50μm)代替纱布,某杂质颗粒的直径约为10μm,该颗粒(填“能”或“不能”)透过滤纸。(4)、消毒剂的制备原理为: ,则物质X的化学式为。(5)、上述生产过程未涉及的净水方法是(填标号)。
(1)、检验天然水是否为硬水,使用的试剂是。(2)、明矾[KAl(SO4)2﹒12H2O] 溶于水,溶液中含有钾离子、硫酸根离子、铝离子等,写出其中一种金属离子的符号:。(3)、装置C中填充的材料有①活性炭、②粗沙、③细沙、④棉花(每种材料之间都用纱布隔开) ,填充材料由上到下的顺序是 ( 填序号);其中活性炭的作用是;若用滤纸(孔径为30~ 50μm)代替纱布,某杂质颗粒的直径约为10μm,该颗粒(填“能”或“不能”)透过滤纸。(4)、消毒剂的制备原理为: ,则物质X的化学式为。(5)、上述生产过程未涉及的净水方法是(填标号)。A 吸附
B 蒸馏
C 沉降
D 过滤
13. 木炭燃烧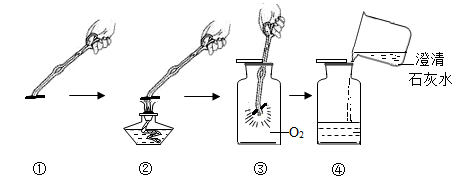 (1)、从“燃烧条件”分析,实验①中木炭没有燃烧的原因是。(2)、对比实验 ( 填序号)可证明氧气浓度越大,木炭燃烧越剧烈。(3)、实验④中反应的化学方程式为。14. 用高锰酸钾制取较纯净的氧气
(1)、从“燃烧条件”分析,实验①中木炭没有燃烧的原因是。(2)、对比实验 ( 填序号)可证明氧气浓度越大,木炭燃烧越剧烈。(3)、实验④中反应的化学方程式为。14. 用高锰酸钾制取较纯净的氧气 (1)、图中仪器G的名称是。(2)、制取氧气的化学方程式为。用图中的仪器组装其发生和收集装置,不需要的仪器是(填标号)。(3)、实验结束发现收集的氧气不纯净,可能的不正确操作是(写一点)。
(1)、图中仪器G的名称是。(2)、制取氧气的化学方程式为。用图中的仪器组装其发生和收集装置,不需要的仪器是(填标号)。(3)、实验结束发现收集的氧气不纯净,可能的不正确操作是(写一点)。四、填空题
-
15. 在化工生产和科学实验中,催化剂皆大显身手。氧化铟可作为催化剂。铟离子(In3+)的结构示意图如图。下列说法错误的是 ( 填标号)。

A 铟元素属于金属元素
B 铟原子的核外有4个电子层
C 铟原子在化学反应中易失电子
D 氧化铟的化学式为In2O3
16. 二氧化锰在分解过氧化氢溶液反应中的催化原理为: ; 。取不同制备方法的二氧化锰与5 mL 10%过氧化氢溶液反应,测得实验数据如下表:二氧化锰制备方法
高温分解法
电解法(市售)
水热法
比表面积/ m2﹒g-1
0.468
49.3
223.274
催化剂的质量/mg
3
3
a
平均催化速率/mL﹒s-1
0.1
0.4
0.6
30 s内产生氧气的体积/mL
3
12
b
(1)、根据催化原理,你对催化剂的一种新的认识是。(2)、根据上表数据分析:a=;b=。若使催化剂的催化速率最大,要尽可能增大。17. 科学家成功研制出用新型催化剂合成甲醇( CH3OH)的新工艺,其反应的微观示意图如下: (1)、该反应中反应物的分子个数比为。(2)、若有8 g氧气参加反应,理论上生成甲醇的质量为g。(3)、该化学反应中最小的微粒有 (填名称)。18. 追随科学家的足迹,溯源求真。燃素说——可燃物中含有气态“燃素”,燃烧时被释放出,则物质燃烧后质量减轻。(1)、请举例说明“燃素说”是错误的:。(2)、在一密闭的容器中,12 g炭粉与64 g氧气点燃后充分反应,容器内各相关量与时间(从反应开始计时)的对应关系如下图所示,其中正确的有(填标号)。
(1)、该反应中反应物的分子个数比为。(2)、若有8 g氧气参加反应,理论上生成甲醇的质量为g。(3)、该化学反应中最小的微粒有 (填名称)。18. 追随科学家的足迹,溯源求真。燃素说——可燃物中含有气态“燃素”,燃烧时被释放出,则物质燃烧后质量减轻。(1)、请举例说明“燃素说”是错误的:。(2)、在一密闭的容器中,12 g炭粉与64 g氧气点燃后充分反应,容器内各相关量与时间(从反应开始计时)的对应关系如下图所示,其中正确的有(填标号)。 19. 为探究原子内部结构,1906年卢瑟福进行了著名的α粒子散射实验:让一束平行的带正电且质量比电子大许多的α粒子穿过极薄的金箔时,发现有少数α粒子改变了原来的直线射程,而发生不同程度的偏转;极少数(约万分之一)α粒子,像遇到某种不能穿透的坚实东西而被折回。该实验不能说明的观点是(填标号)。
19. 为探究原子内部结构,1906年卢瑟福进行了著名的α粒子散射实验:让一束平行的带正电且质量比电子大许多的α粒子穿过极薄的金箔时,发现有少数α粒子改变了原来的直线射程,而发生不同程度的偏转;极少数(约万分之一)α粒子,像遇到某种不能穿透的坚实东西而被折回。该实验不能说明的观点是(填标号)。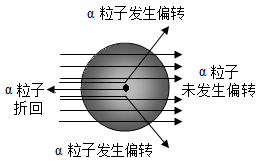 A、原子核带正电 B、原子核体积小、质量大 C、原子核由质子和中子构成 D、相对于原子核,核外空间很大20. 根据下列元素周期表的部分信息判断:某原子中质子、中子和电子共有49个,其中不带电的微粒有17个,则该原子为(填名称)。
A、原子核带正电 B、原子核体积小、质量大 C、原子核由质子和中子构成 D、相对于原子核,核外空间很大20. 根据下列元素周期表的部分信息判断:某原子中质子、中子和电子共有49个,其中不带电的微粒有17个,则该原子为(填名称)。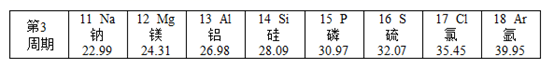 21. 某化学小组利用金属化学性质开展探究实验。镁在空气中燃烧。某同学称量镁条和石棉网的质量(如图),而后在空气中点燃镁条,反应结束后将所得物质与石棉网一起再次称量,发现质量减轻。
21. 某化学小组利用金属化学性质开展探究实验。镁在空气中燃烧。某同学称量镁条和石棉网的质量(如图),而后在空气中点燃镁条,反应结束后将所得物质与石棉网一起再次称量,发现质量减轻。 (1)、镁条点燃后,剧烈燃烧发出白光、放热、生成白色粉末且伴有白烟散逸。该反应的化学方程式为。(2)、根据质量守恒定律:生成的氧化镁质量(填“大于”或“等于”)参加反应的镁条质量;实验事实却非如此,原因是。22. 不同金属与酸反应:某同学利用压强传感器,绘得形状相同的不同金属与等浓度足量的稀盐酸反应时,气压的变化曲线如图。
(1)、镁条点燃后,剧烈燃烧发出白光、放热、生成白色粉末且伴有白烟散逸。该反应的化学方程式为。(2)、根据质量守恒定律:生成的氧化镁质量(填“大于”或“等于”)参加反应的镁条质量;实验事实却非如此,原因是。22. 不同金属与酸反应:某同学利用压强传感器,绘得形状相同的不同金属与等浓度足量的稀盐酸反应时,气压的变化曲线如图。 (1)、根据曲线①判断:镁与稀盐酸反应属于(填“吸热”或“放热”)反应。(2)、铝与稀盐酸的反应速率先慢后快,原因是。(3)、曲线⑤中气压不变的原因是。
(1)、根据曲线①判断:镁与稀盐酸反应属于(填“吸热”或“放热”)反应。(2)、铝与稀盐酸的反应速率先慢后快,原因是。(3)、曲线⑤中气压不变的原因是。五、推断题
-
23. 如图是一个“化学沙漏”,珠子A-F分别代表6种物质:氧气、单质碳、碳的氧化物、铁、氧化铁、硫酸铜。珠子漏下的规则为:含元素种类最多的珠子第一个漏下;依次漏下的珠子与上一颗能发生反应,从而实现按“A-B-C-D-E-F”的顺序下漏。
 (1)、物质A为 (填化学式)。(2)、证明B与C发生反应的现象是。(3)、若.上述“碳的氧化物”对应的珠子是F
(1)、物质A为 (填化学式)。(2)、证明B与C发生反应的现象是。(3)、若.上述“碳的氧化物”对应的珠子是F①写出“E-F”反应的化学方程式:。
②珠子(填标号)间的反应属于置换反应。
a. A-B
b. B-C .
c.C-D
d. D-E
③将该“碳的氧化物”对应的珠子F与珠子 ( 填标号)对换,珠子仍可顺利漏完。
六、科学探究题
-
24. 同学发现镁与稀盐酸反应的实验中出现灰白色沉淀,该同学对灰白色沉淀的成分进行如下探究:
[提出假设]假设一:含有氯化镁 假设二:含有镁 假设三:含有 氢氧化镁 假设四.....
[查阅资料]①氯化镁易溶于水;②氢氧化镁与稀盐酸反应生成氯化镁和水
[设计并进行实验]
(1)、将灰白色沉淀与液体分离的操作名称是。(2)、各取少量灰白色沉淀加入2支试管中进行如下实验:编号
实验操作
实验现象
结论
试管1
,
假设一不成立
试管2
加入适量稀盐酸
沉淀全部溶解,没有气泡产生
假设二(填“成立”或“不成立”)假设三可能成立。
(3)、[实验反思]通过该同学的实验没有获得确切的结论,同学们继续查阅资料,得知该灰白色固体为碱式氯化镁[ Mg(OH)Cl]。某同学取少量碱式氯化镁加入适量稀盐酸,固体全部溶解且没有气泡产生,得到氯化镁的水溶液。碱式氯化镁与稀盐酸反应的化学方程式为。
七、计算题
-
25. 在煤中添加石灰石作为脱硫剂,可以吸收煤燃烧产生的二氧化硫,该反应的原理为: 。已知1 t的某种煤燃烧会产生0.02 t的二氧化硫,计算:(1)、128 t这种煤燃烧会生成t的二氧化硫。(2)、理论上需要加入多少吨含碳酸钙80%的石灰石,才能完全吸收128t煤燃烧产生的二氧化硫?(写出计算过程)
-
-
-