高中化学人教版(新课标)必修1 第三章第三节 用途广泛的金属材料
试卷更新日期:2020-10-30 类型:同步测试
一、单选题
-
1. 丝绸之路贸易中的下列商品,主要成分属于合金的是( )A、青铜器皿
 B、陶瓷
B、陶瓷  C、丝绸
C、丝绸  D、中草药
D、中草药  2. 下列有关金属材料的说法错误的是( )A、铁有良好的导热性,常用来制作炊具 B、铜的化学性质不活泼,因此可用于制导线 C、废旧电池中汞的回收可减少对环境的污染 D、钛合金与人体有很好的相容性,因此可用来制造人造骨3. 下列说法不正确的是( )A、Al2O3熔点很高,可用作高级耐火材料 B、Na2O可作呼吸面具中的供氧剂 C、镁铝合金被大量用于高铁建设 D、苯可萃取碘水中的碘单质4. 下列说法不正确的是( )A、钠在空气中燃烧时,先熔化,再燃烧,发出黄色火焰,生成过氧化钠 B、青铜是我国使用最早的合金,钢是用量最大、用途最广的合金 C、铝是地壳里含量最多的金属元素,在常温下,铝不能与氧气反应 D、铁在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属5. 镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,错误的是( )A、此合金的熔点比镁和铝的熔点都低 B、此合金能全部溶解于足量稀盐酸中 C、此合金能全部溶解于足量氢氧化钠溶液中 D、此合金的硬度比镁和铝的硬度都大6. 下列有关铁及其化合物的说法正确的是( )A、铁的氧化物有FeO、Fe2O3、Fe3O4 , 它们都是黑色的固体 B、铁的氢氧化物Fe(OH)2、Fe(OH)3的混合物可能是灰绿色 C、鉴别Fe2+中混有Fe3+ , 可先加入Cl2水,再加入KSCN溶液 D、铁的合金生铁比纯铁硬度大,熔点高。7. 下列有关合金的性质的说法正确的是( )
2. 下列有关金属材料的说法错误的是( )A、铁有良好的导热性,常用来制作炊具 B、铜的化学性质不活泼,因此可用于制导线 C、废旧电池中汞的回收可减少对环境的污染 D、钛合金与人体有很好的相容性,因此可用来制造人造骨3. 下列说法不正确的是( )A、Al2O3熔点很高,可用作高级耐火材料 B、Na2O可作呼吸面具中的供氧剂 C、镁铝合金被大量用于高铁建设 D、苯可萃取碘水中的碘单质4. 下列说法不正确的是( )A、钠在空气中燃烧时,先熔化,再燃烧,发出黄色火焰,生成过氧化钠 B、青铜是我国使用最早的合金,钢是用量最大、用途最广的合金 C、铝是地壳里含量最多的金属元素,在常温下,铝不能与氧气反应 D、铁在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属5. 镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,错误的是( )A、此合金的熔点比镁和铝的熔点都低 B、此合金能全部溶解于足量稀盐酸中 C、此合金能全部溶解于足量氢氧化钠溶液中 D、此合金的硬度比镁和铝的硬度都大6. 下列有关铁及其化合物的说法正确的是( )A、铁的氧化物有FeO、Fe2O3、Fe3O4 , 它们都是黑色的固体 B、铁的氢氧化物Fe(OH)2、Fe(OH)3的混合物可能是灰绿色 C、鉴别Fe2+中混有Fe3+ , 可先加入Cl2水,再加入KSCN溶液 D、铁的合金生铁比纯铁硬度大,熔点高。7. 下列有关合金的性质的说法正确的是( )①合金与各成分金属相比较,具有许多优良的物理、化学或机械性能
②相同金属元素形成的合金、元素的含量有可能不同,但其性能是相同的
③镁铝合金在盐酸中不能完全溶解
④合金具有各成分金属性质之和
A、①② B、①③ C、① D、③④8. 下列说法正确的是()A、铝合金的熔点比纯铝高 B、铜具有良好的导电性,常用来制作印刷电路板 C、镁在空气中或纯净的氧气中燃烧,产物一定只有MgO D、钠在敞口容器中长期存放或在空气中燃烧,产物一定是Na2O2二、填空题
-
9. 生铁和钢是含 不同的两种 合金,生铁的含碳量为 ,钢的含碳量为 .10. 某铝合金中含有镁、铜、硅,为了测定研究它的抗腐蚀性能和测定合金中铝的含量,某研究性学习小组设计了如下实验:
(一)探究铝合金的抗腐蚀性能
①向一只小烧杯里加入20mL0.5mol/LCuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝片取出,观察铝片表面的现象
②取1只试管,加入10mL2mol/LNaOH溶液,将一块铝片放入NaOH溶液里,片刻取出后,用蒸馏水冲洗后浸入CuSO4溶液里.1~2分钟后将铝片取出,观察铝片表面的现象
实验①铝片没有变化,实验②铝片表面的现象是
发生此现象的原因是
(二)测定铝合金中的铝的百分含量
①取该样品a克,将样品溶于足量的稀盐酸中,过滤;
②在滤液中加入过量的氢氧化钠溶液,过滤;
③往第②步的滤液中通入足量的CO2 , 过滤,将沉淀用蒸馏水洗涤后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为b克.
回答下列问题:
(1)在第①步操作中溶解所使用的玻璃仪器为玻璃棒、 ,滤液中主要含有Mg2+、Na+、 和Cl﹣离子;
(2)在第②步操作中氢氧化钠溶液需要过量的原因是 ,写出该步骤中生成沉淀的离子方程式
(3)第③步灼烧过程中可在下列哪种仪器中进行
A.烧杯 B.试管 C.坩埚 D.蒸发皿
(4)第③步灼烧后得到的固体是
(5)合金中铝的质量分数是 .
三、综合题
-
11. 某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子,有人设计了图中的工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜(图中标号处只利用工业生产中的常用的酸、碱和废铁屑).
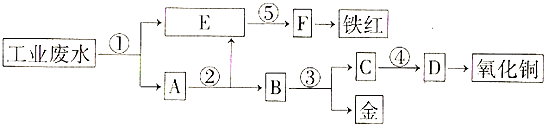 (1)、图中标号处需加入的相应物质分别是①、②、③、④、⑤;(2)、写出①处所有可能发生的离子方程式(3)、写出③处发生反应的化学方程式;(4)、铁红的化学式为;写出铁红在工业上的一种主要用途 .12. 某工业废液里含有FeCl2、CuCl2和FeCl3 . 为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程:
(1)、图中标号处需加入的相应物质分别是①、②、③、④、⑤;(2)、写出①处所有可能发生的离子方程式(3)、写出③处发生反应的化学方程式;(4)、铁红的化学式为;写出铁红在工业上的一种主要用途 .12. 某工业废液里含有FeCl2、CuCl2和FeCl3 . 为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程: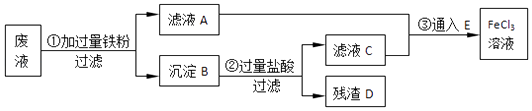 (1)、A的化学式为 , E的化学式为 .(2)、B的化学成分 , 回收的铜是(填A、B、C、D或E).(3)、根据图示,反应②的化学方程式为 .
(1)、A的化学式为 , E的化学式为 .(2)、B的化学成分 , 回收的铜是(填A、B、C、D或E).(3)、根据图示,反应②的化学方程式为 .