专题25:炔烃
试卷更新日期:2020-10-22 类型:一轮复习
一、单选题
-
1. 下列分子中各原子不处于同一平面内的是( )A、乙烷 B、乙烯 C、乙炔 D、苯2. 2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如图所示),其特殊的电子结构将有望广泛应用于电子材料领域。下列说法错误的是( )
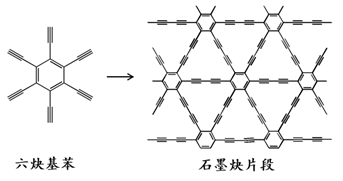 A、六炔基苯的化学式为C18H6 B、六炔基苯和石墨炔都具有平面型结构 C、六炔基苯和石墨炔都可发生加成反应 D、六炔基苯合成石墨炔属于加聚反应3. 含有一个三键的炔烃,氢化后的产物结构简式如图,此炔烃可能的结构简式有( )
A、六炔基苯的化学式为C18H6 B、六炔基苯和石墨炔都具有平面型结构 C、六炔基苯和石墨炔都可发生加成反应 D、六炔基苯合成石墨炔属于加聚反应3. 含有一个三键的炔烃,氢化后的产物结构简式如图,此炔烃可能的结构简式有( )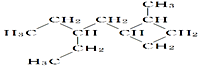 A、1种 B、2种 C、3种 D、4种4. 将乙炔通入银氨溶液,产生白色沉淀,通过该实验可以区分乙炔和乙烯。化学方程式为:HC≡CH+2[Ag(NH3)2]+ →AgC≡CAg↓+2NH4++2NH3。乙炔银遇酸可放出乙炔。下列分析或推测不正确的是( )A、乙炔与银氨溶液的反应不是氧化还原反应 B、乙炔中C-H键的活性比乙烯中C-H键的活性强 C、乙炔通入AgNO3溶液中也能发生类似反应 D、2-丁炔不能与银氨溶液发生类似反应5. 下列实验操作能达到实验目的的是( )
A、1种 B、2种 C、3种 D、4种4. 将乙炔通入银氨溶液,产生白色沉淀,通过该实验可以区分乙炔和乙烯。化学方程式为:HC≡CH+2[Ag(NH3)2]+ →AgC≡CAg↓+2NH4++2NH3。乙炔银遇酸可放出乙炔。下列分析或推测不正确的是( )A、乙炔与银氨溶液的反应不是氧化还原反应 B、乙炔中C-H键的活性比乙烯中C-H键的活性强 C、乙炔通入AgNO3溶液中也能发生类似反应 D、2-丁炔不能与银氨溶液发生类似反应5. 下列实验操作能达到实验目的的是( )实验操作
实验目的
A
将饱和食盐水滴加到电石中,将产生的气体通入溴水中
验证乙炔可与 Br2 发生了加成反应
B
乙醇与浓硫酸加热至 170℃,将产生的气体先通入NaOH 溶液,再通入 Br2 的 CCl4 溶液
检验产生的乙烯
C
将溴乙烷与 NaOH 乙醇溶液共热,将产生的气体通入酸性 KMnO4 溶液
检验产生的乙烯
D
向纯碱中滴加醋酸,将产生的气体通入苯酚钠浓溶液
证明酸性:醋酸>碳酸>苯酚
A、A B、B C、C D、D6. 下列实验方案设计合理且能达到实验目的的是( )A、检验乙炔发生加成反应:将电石制得的气体直接通入溴水,溴水褪色 B、提纯含少量苯酚的苯:加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水 C、制备少量乙酸乙酯:向乙醇中缓慢加入浓硫酸和冰醋酸,用NaOH溶液吸收乙酸乙酯,除去乙醇和乙酸 D、验证有机物X是否含有醛基:向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再加入0.5 mL有机物X,加热煮沸7. 与H2反应生成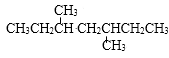 的单炔烃有( ) A、1种 B、2种 C、4种 D、8种8. 下列物质中,在一定条件下既能起加成反应,也能起取代反应,但不能使酸性KMnO4溶液褪色的是( )A、乙烷 B、苯 C、乙烯 D、乙炔9. 下列说法中,正确的是( )A、向溴乙烷中加入NaOH溶液,加热,充分反应,再加入AgNO3溶液,产生淡黄色沉淀,证明溴乙烷中含有溴元素 B、实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下 C、在乙炔的制备实验中为加快反应速率可用饱和食盐水代替水 D、制备新制Cu(OH)2悬浊液时,将4~6滴2%的NaOH溶液滴入2 mL2%的CuSO4溶液中,边滴边振荡10. 0.5mol 气态烃A 最多和1 mol HCl加成,生成氯代烷B,1mol B与4 mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )A、C2H4 B、C2H2 C、C3H4 D、C4H6
的单炔烃有( ) A、1种 B、2种 C、4种 D、8种8. 下列物质中,在一定条件下既能起加成反应,也能起取代反应,但不能使酸性KMnO4溶液褪色的是( )A、乙烷 B、苯 C、乙烯 D、乙炔9. 下列说法中,正确的是( )A、向溴乙烷中加入NaOH溶液,加热,充分反应,再加入AgNO3溶液,产生淡黄色沉淀,证明溴乙烷中含有溴元素 B、实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下 C、在乙炔的制备实验中为加快反应速率可用饱和食盐水代替水 D、制备新制Cu(OH)2悬浊液时,将4~6滴2%的NaOH溶液滴入2 mL2%的CuSO4溶液中,边滴边振荡10. 0.5mol 气态烃A 最多和1 mol HCl加成,生成氯代烷B,1mol B与4 mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )A、C2H4 B、C2H2 C、C3H4 D、C4H6二、实验探究题
-
11. 实验室中可用如图制备乙炔,回答下列问题
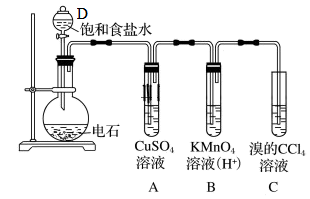 (1)、仪器D名称。(2)、制取乙炔的化学方程式。(3)、试管A观察到的现象。(4)、写出C发生的化学方程式。(5)、若没有A装置,观察到B褪色,且有浅黄色浑浊,请写出生成浅黄色浑浊的离子方程式。12. 实验室用乙醇制取乙烯,用电石(主要成分为CaC2 , 含少量CaS)制取乙炔。(1)、实验室制取乙烯的化学方程式为 , 可用于制取乙烯的发生装置是。(选填编号)
(1)、仪器D名称。(2)、制取乙炔的化学方程式。(3)、试管A观察到的现象。(4)、写出C发生的化学方程式。(5)、若没有A装置,观察到B褪色,且有浅黄色浑浊,请写出生成浅黄色浑浊的离子方程式。12. 实验室用乙醇制取乙烯,用电石(主要成分为CaC2 , 含少量CaS)制取乙炔。(1)、实验室制取乙烯的化学方程式为 , 可用于制取乙烯的发生装置是。(选填编号)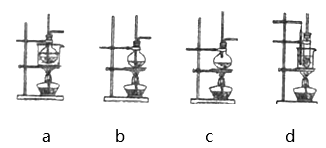 (2)、制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是。
(2)、制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是。a 吸水性 b 脱水性 c 强氧化性 d 酸性
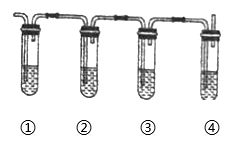
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
① , ② , ③ , ④。
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
(3)、实验室制备乙炔的化学反应方程式为。实验室制乙炔时为避免电石和水反应过于激烈,除用分液漏斗控制滴速外,通常还可用代替水。为除去乙炔中混有的少量硫化氢杂质,可将气体通过(选填编号)。a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
13. 某同学欲证明乙炔能与高锰酸钾酸性溶液反应,实验方案如下:将电石与水反应生成的气体通入高锰酸钾酸性溶液,溶液褪色,证明二者发生了反应.请回答:(1)、制备乙炔的反应的化学方程式是。(2)、该同学的实验方案存在的问题是。(3)、为了解决上述问题,需重新选择实验装置,备选装置如图所示.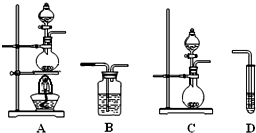
①将装置编号按顺序填在横线上→B→。
②B装置中所盛放的试剂是。
三、综合题
-
14. A(C2H2)是基本有机化工原料。由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线(部分反应条件略去)如下所示:
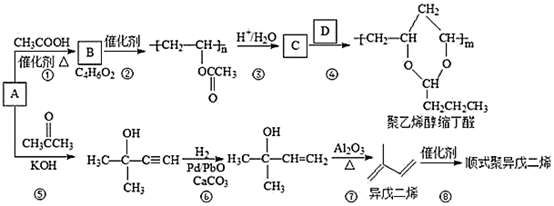
回答下列问题:
(1)、A的名称是 , B含有的官能团是。(2)、①的反应类型是 , ⑦的反应类型是。(3)、C和D的结构简式分别为、。(4)、异戊二烯分子中最多有个原子共平面,顺式聚异戊二烯的结构简式为。(5)、写出与A具有相同官能团的异戊二烯的所有同分异构体(填结构简式)。(6)、参照异戊二烯的上述合成路线,设计一条由A和乙醛为起始原料制备1,3-丁二烯的合成路线。15. 烃A标准状况下的密度为1.16 g·L-1 , 以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。F为有浓郁香味,不易溶于水的油状液体。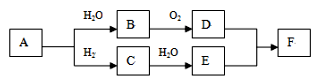
请回答:
(1)、A的结构简式。(2)、D+E→F的反应类型是。(3)、有机物A转化为B的化学方程式是。(4)、下列说法正确的是_________。A、有机物E与金属钠反应比水与金属钠反应要剧烈。 B、有机物E与金属钠反应的产物可以与水反应重新生成E。 C、有机物D,E,F可用饱和Na2CO3溶液鉴别。 D、上述转化关系图中共涉及3次加成反应。16. 以苯和乙炔为原料合成化工原料E的路线如下: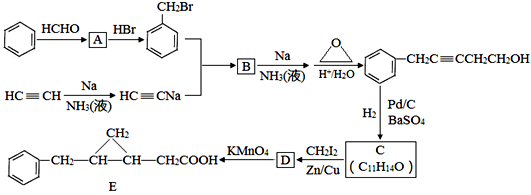
回答下列问题:
(1)、以下有关苯和乙炔的认识正确的是。a.苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
b.苯和乙炔在空气中燃烧都有浓烟产生
c.苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
d.聚乙炔是一种有导电特性的高分子化合物
(2)、A的名称。(3)、生成B的化学方程式为 , 反应类型是。(4)、C的结构简式为 , C的分子中一定共面的碳原子最多有个。(5)、与D同类别且有二个六元环结构(环与环之间用单键连接)的同分异构体有4种,请写出其中2种同分异构体的结构简式:。(6)、参照上述合成路线,设计一条以乙炔和必要试剂合成环丙烷的路线:。