初中化学九年级上学期期中考试复习专题:06 原子、分子、离子、元素
试卷更新日期:2020-10-22 类型:复习试卷
一、单选题
-
1. 下列关于分子和原子的说法,错误的是( )A、分子比原子大 B、分子和原子都不显电性 C、分子和原子都在不断运动 D、分子和原子都是构成物质的基本粒子2. 下列依据证据得出的结论,错误的是( )
选项
证据
结论
A
1滴水约含1.67×1021个水分子
水分子体积很小
B
Cu与AgNO3溶液反应生成Ag和Cu(NO3)2
Cu的金属活动性比Ag的强
C
向某固体中加入稀盐酸,有气体产生
该固体一定是Na2CO3
D
白磷在热水中不燃烧,通入氧气后燃烧
氧气能支持白磷燃烧
A、A B、B C、C D、D3. 在“宏观--微观--符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是( )
 A、硅单质是制造芯片的重要材料,图①是硅原子的结构示意图 B、硅元素与氯元素的本质区别是质子数不同 C、若图③中x的值为8,则其粒子符号为O2- D、图②④对应元素组成的化合物是由分子构成的4. 下列关于微观粒子的说法,正确的是( )A、带电的粒子一定是离子 B、在干冰中,分子因相互作用而静止不动 C、所有原子都由原子核和核外电子构成 D、并不是所有分子都是由原子构成的5. 下列说法正确的是( )A、微粒得到或失去电子变成离子 B、在同一种物质中,同种元素的化合价可能不相同 C、由同一种元素组成的物质一定是单质,不可能是化合物 D、已知铁原子核内质子数为26,相对原子质量为56,可以求出核外电子数,无法求出其核内中子数6. 元素X的核电荷数为a,它的阳离子
A、硅单质是制造芯片的重要材料,图①是硅原子的结构示意图 B、硅元素与氯元素的本质区别是质子数不同 C、若图③中x的值为8,则其粒子符号为O2- D、图②④对应元素组成的化合物是由分子构成的4. 下列关于微观粒子的说法,正确的是( )A、带电的粒子一定是离子 B、在干冰中,分子因相互作用而静止不动 C、所有原子都由原子核和核外电子构成 D、并不是所有分子都是由原子构成的5. 下列说法正确的是( )A、微粒得到或失去电子变成离子 B、在同一种物质中,同种元素的化合价可能不相同 C、由同一种元素组成的物质一定是单质,不可能是化合物 D、已知铁原子核内质子数为26,相对原子质量为56,可以求出核外电子数,无法求出其核内中子数6. 元素X的核电荷数为a,它的阳离子 与元素Y的阴离子
与元素Y的阴离子  的电子层结构相同,则元素Y的核电荷数是( ) A、
的电子层结构相同,则元素Y的核电荷数是( ) A、 B、
B、 C、
C、 D、
D、 7. 不合格家用花岗岩石材中常含有放射性元素氡。一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( )A、50 B、136 C、86 D、2228. 下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是( )A、O B、2H C、2O2 D、Hg9. 奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源,这里的“钙”指( )A、钙离子 B、钙原子 C、钙元素 D、钙单质10. 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是最小的粒子,不可再分 D、氯化钠是由钠离子和氯离子构成的
7. 不合格家用花岗岩石材中常含有放射性元素氡。一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( )A、50 B、136 C、86 D、2228. 下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是( )A、O B、2H C、2O2 D、Hg9. 奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源,这里的“钙”指( )A、钙离子 B、钙原子 C、钙元素 D、钙单质10. 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是最小的粒子,不可再分 D、氯化钠是由钠离子和氯离子构成的二、填空题
-
11. 用化学符号填空:(1)、地壳中含量最多的元素;(2)、2个氢原子;(3)、锌离子;(4)、8个硫原子构成的单质分子;12. 用微粒的观点回答下列问题:(1)、水的构成粒子是① , 铁的构成粒子是②。(2)、水(H2O)通电分解生成氢气(H2)和氧气(O2)的过程中,发生变化的是① , 不变的微粒是②。13.(1)、下图是一种处理汽车尾气的反应微观示意图,回答下列问题。
①从微观上看,该化学变化中发生改变的粒子是(填“分子”或“原子”),反应前后原子的数目(填“有”或“没有”)增减。
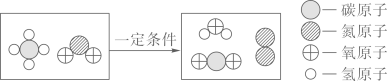
②参加反应的
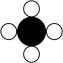 和
和 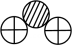 的分子个数比为 , 该反应中涉及到的单质的化学式为。(2)、下图是A、B、C、D四种粒子的结构示意图
的分子个数比为 , 该反应中涉及到的单质的化学式为。(2)、下图是A、B、C、D四种粒子的结构示意图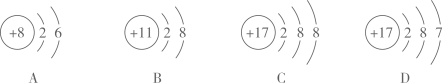
①图中共有种元素。
②C粒子的符号为 , 由B、C两种粒子构成的化合物的化学式为。
三、综合题
-
14. 元素周期表是学习和研究化学的重要工具。请分析图中的信息并回答下列问题。
 (1)、第16号元素属于元素(填“金属”或“非金属”),它在化学反应中容易(填“得到”或“失去”)电子。(2)、元素的化学性质与原子结构中的数关系密切。(3)、在同一族中,各元素的原子结构呈现的规律有(任写一点);(4)、研究表明: 第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是。(5)、1869年,科学家发现了元素周期律和元素周期表。15. 科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据图所示按要求回答问题:
(1)、第16号元素属于元素(填“金属”或“非金属”),它在化学反应中容易(填“得到”或“失去”)电子。(2)、元素的化学性质与原子结构中的数关系密切。(3)、在同一族中,各元素的原子结构呈现的规律有(任写一点);(4)、研究表明: 第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是。(5)、1869年,科学家发现了元素周期律和元素周期表。15. 科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据图所示按要求回答问题: (1)、图(甲)是氯元素在元素周期表中的部分信息,氯元素的相对原子质量是。(2)、图(乙)是某原子的结构示意图,则X的数值是 , 该原子形成的阳离子符号是 , 该元素与氯元素组成的化合物的化学式是。(3)、图(丙)是某化学反应的微观示意图,请写出该反应的化学方程式。16. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)、图(甲)是氯元素在元素周期表中的部分信息,氯元素的相对原子质量是。(2)、图(乙)是某原子的结构示意图,则X的数值是 , 该原子形成的阳离子符号是 , 该元素与氯元素组成的化合物的化学式是。(3)、图(丙)是某化学反应的微观示意图,请写出该反应的化学方程式。16. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。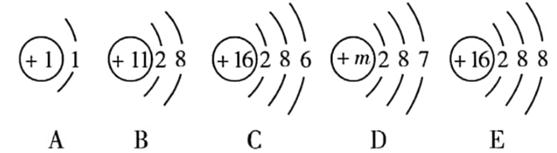 (1)、图D中m的值为 , 该粒子在化学反应中易(填“得到”或“失去”)电子。(2)、图中共有种元素。(3)、图中属于阳离子的是(填离子符号)。(4)、图C表示某元素的粒子,该元素在元素周期表中位于第周期,它的化学性质与下列元素中的(填序号)化学性质相似。
(1)、图D中m的值为 , 该粒子在化学反应中易(填“得到”或“失去”)电子。(2)、图中共有种元素。(3)、图中属于阳离子的是(填离子符号)。(4)、图C表示某元素的粒子,该元素在元素周期表中位于第周期,它的化学性质与下列元素中的(填序号)化学性质相似。①N②O③F④Ar